第一章 溶液
溶液是由两种或多种组分所组成的均匀体系。溶液对于科学研究、生命现象都具有重要意义。人的体液多是溶液,医疗用药亦多以溶液的形式或在体液内溶解后形成溶液而发挥其效应。可见溶液与医学的联系是极其密切的。所以,对于学习医学的人来说,了解有关溶液的物理和化学性质是非常必要的。
本章主要讨论有关溶液的概念、溶液的组成量度及渗透压。
第一节 溶解度
在一定条件(温度、压力)下,一定量的溶剂溶解溶质达饱和时,所含溶质的量称为溶解度。任何一种表示浓度的单位都可用来作为溶解度的单位。因此,根据工作需要,溶解度可以有各种不同的表示法,通常用一定温度下,100克溶剂形成饱和溶液时所溶解溶质的质量(单位为克)表示。
物质溶解度的大小与很多因素有关,主要决定于溶质和溶剂的本性以及外界的温度和压力。
一、 固体在液体中的溶解度
温度对固体物质溶解度的影响,可以通过实验绘成的溶解度曲线来表示。图1-1是几种固体盐类在水中的溶解度曲线。
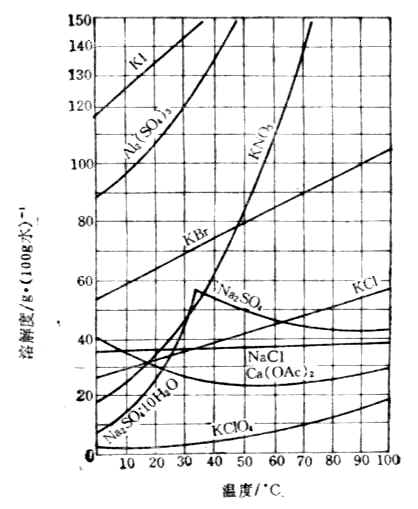
图1-1 溶解度曲线
从图1-1中可以看出,大多数固体物质的溶解度随温度升高而增大。个别物质如醋酸钙的溶解度,随温度的升高反而减小。还可看到硫酸钠的溶解度曲线,在32.4℃时出现了一个转折点。这是因为32.4℃左右时,硫酸钠的存在形式不同。在32.4℃以下,与饱和溶液呈平衡的固体是含结晶水的硫酸钠Na2SO4·10H2O,随温度升高溶解度增大。在32.4℃以上,与饱和溶液呈平衡的固体是无水硫酸钠Na2SO4,随温度上升而溶解度减小。
利用在不同温度下物质的溶解度不同这一性质,可以进行物质的提纯以除去其中杂质。在实际工作中,常将要是纯的物质先加热溶解于适当的溶剂中,使其成为饱和或接近饱和溶液,趁热滤去不溶性杂质,然后将溶液冷却,这时因物质的溶解度减小,势必从溶液中析出结晶,而可溶性杂质由于含量少,远未达到饱和而留在母液中。最后过滤,使析出的结晶与母液分离而得到较纯物质。这种操作称为重结晶。
值得注意的是有些物质在温度降低时,溶液中所含溶质的量虽超过了该温度下饱和溶液所含溶质的量,溶质也不析出,这种溶液称为过饱和溶液。过饱和溶液是不稳定的体系,稍一振荡或投入一小颗粒结晶,多余的溶质立即从溶液中析出而成为饱和溶液。
二、气体在液体中的溶解度
气体的溶解平衡是指在密闭容器中,溶解在液体中的气体分子与液体上面的气体分子保持平衡。溶解达平衡时,气体在液体中的浓度就是气体的溶解度。通常用1体积液体中所能溶解气体的体积表示。表1-1是一些气体在水中的溶解度。
表1-1 一些气体在水中的溶解度
| 温度/℃ | O2 | H2 | N2 | CO2 | HCL | NH3 |
| 0.0489 | 0.0215 | 0.0235 | 1.713 | 507 | 1176 | |
| 20 | 0.0310 | 0.0182 | 0.0155 | 0.878 | 442 | 702 |
| 30 | 0.0261 | 0.0170 | 0.0134 | 0.665 | 413 | 586(28℃) |
| 35 | 0.0244 | 0.0167 | 0.0126 | 0.592 | —— | —— |
从表1-1中可以明显地看出,温度升高,气体的溶解度减小。也可以看出,不同的气体在水中的溶解度相差很大,这与气体及溶剂的本性有关。H2,O2,N2等气体在水中的溶解度较小,因为这些气体在溶解过程中不与水发生化学反应,称为物理溶解。而CO2,HCL,NH3等气体在水中的溶解度较大,因为这些气体在溶解过程中与水发生了化学反应,称为化学溶解。
气体在液体中的溶解,除与气体的本性、温度有关外,压力对气体的溶解度的影响也比较大。压力和分压的单位是帕(或帕斯卡,符号Pa),通常用千帕(符号kPa)表示。101.325kPa(或101325Pa)相当于过去1atm(1大气压),133.32Pa相当于1mmHg,作为非国际单位制的atm和mmHg本书不再使用。
(一)分压定律
混合气体的总压力等于各组分气体分压力之和。这一定律称为分压定律。这种关系可用数学式表示。
p=p1+p2+p3+…
式中,p是混合气体的总压力,p1,p2,p3等是各组分气体的分压力。
混合气体中每一种气体的分压力,可由总压力和该气体在混合气体中所占的体积百分数或摩尔分数的乘积来计算:
p1=p×(%V1)
或 p1=p×x1
式中,p为气体总压力,%V1为气体1的体积百分数,x1为气体1的摩尔分数。
例1 人的肺泡气总压力为101.325kPa,37℃时,它的组成用体积百分数表示分别为:O2为13.4%,CO2为5.3%,N2为75%,H2O(蒸汽)为6.3%,试求各气体在肺泡中的分压。
解:po2=101.325kPa×13.4%=13.6kPa
pCO2=101.325kPa×5.3%=5.4kPa
pN2=101.325kPa×75%=76.0kPa
pH2O=101.325kPa×6.3%=6.4kPa
(二)亨利定律
1803年亨利(Henry)从实验中总结出一条规律,其内容是:“在一定温度下,气体溶解达到平衡时,气体在液体中的溶解度和气相中该气体的分压成正比。”这一规律称为亨利定律。可用数学式表示:
c=Kp (1-1)
式中,c为气体在液体中溶解度,一般是指1kg水中溶解气体的质量(克);p为液面上气体的平衡分压;K为常数,是该气-液体系的特征常数。
必须注意,亨利定律只适用于压力不大(一般为202.3~303.9kPa)和溶解度很小的气体。温度越高或压力越低,在稀溶液中应用亨利定律能得到较准确的结果。另外,亨利定律只适用于不与溶剂发生化学反应的气体,即溶质在气相和液相中的分子状态必须是相同的。
例2 在0℃,平衡压力为303.9kPa。氧气的溶解度为0.2085g/1000g水。求在同温度、平衡压力为202.6kPa下氧气的溶解度。
解:由式(1-1)先求K值:
K=c/p=0.2085/303.9=0.000686(g/1000g水•kPa)
对于一定气体和溶剂,在一定温度下,K是一个常数,与气体的压力无关.在平衡压力为202.6kPa时,将K值代入式(1-1),则得在水中溶解度为:
c=Kp=0.000686×202.6=0.139(g/1000g水)
亨利定律在医学上有许多应用实例。例如,使用麻醉气体时,气体的分压越大,则它在血液中的溶解度就越大。高压氧气舱的压力为202.6-253.25kPa,比常压为大,因此溶于病人血液的氧气就越多.利用亨利定律还可以解释人在呼吸过程中O2和CO2的交换等。
(三)气体吸收系数
由于气体的体积比质量容易测定,所以气体的溶解度以溶解气体的体积表示比较方便。为了表示各种气体在不同温度和分压下的溶解度,规定将不同状态下所溶解气体的体积,均换算成标准状况下的体积数。
气体吸收系数(a)是指在一定温度下,1体积的液体在该气体分压为101.3kPa下,所能溶解气体的体积.气体体积如果不是标准状况(0℃,101.3kPa),一般要换算为标准状况.如在20℃和氢气分压为101.3kPa下,1L水能溶解氢气0.0195L.根据查理(Charles J.A.C.)定律可将其换算为标准状况下的体积:
0.0195L×273K/(273+20)K=0.0182(L)
0.0182即是在20℃时,101.3kPa下,氢气在水中的吸收系数。
与医学有关的气体在水和血浆中的吸收系数列于表1-2。
表1-2 37℃时气体在水和血浆中的吸收系数
| 气体 | 在水中的吸收系数 | 在血浆中的吸收系数 |
| O2 | 0.0239 | 0.0214 |
| CO2 | 0.567 | 0.515 |
| N2 | 0.0123 | 0.0118 |
从表1-2可以看出,当水中含有其他杂质时,气体的溶解度减少,尤其是有盐类存在时.由于盐类离子与水分子形成水合离子,这时影响则更大.血浆中含有盐类和蛋白质等,故气体在血浆中的溶解度比在水中要小.
利用表1-2的吸收系数,根据肺泡中O2,CO2,N2的分压,就能算出它们溶解在血浆中的体积百分数.
已知肺泡气体中Po2=13.6kPa,Pco2=5.3kPa.PN2=76.0kPa.因此,100mL血浆中所溶解的三种气体的体积百分数为:
O2%=0.0214×13.6/101.3×100=0.287(mL/100mL血浆)
CO2%=0.515×5.3/101.3×100=2.69(mL/100mL血浆)
N2%=0.0118×76/101.3×100=0.885(mL/100mL血浆)
三、液体在液体中的溶解度
一种液体在另一种液体中的溶解有三种情况:第一种是两种液体完全互溶,如乙醇与水、甘油与水等。第二种是两种液体部分互溶,如乙醚与水等。第三种是两种液体完全不溶,如苯与水、四氯化碳与水等。
将两种互不混溶的液体放在同一容器中,就会分成两相,密度大的一相的在下层,密度小的一相在上层。在一定温度下,一种溶质在相互接触的两种互不混溶的溶剂中,溶解达平衡时,溶质在两相中的浓度比是一个常数,这一定律称为分配定律。可表示如下式:
CA/CB=K (1-2)
式中CA、CB分别表示溶质在溶剂A、B中的浓度;常数K称为分配系数,它与溶质和溶剂的本性、温度及压力有关。
例如,将水和四氯化碳放在一起,加入少量碘,碘微溶于水、溶于四氯化碳。
在这两种液体中的溶解度差别很大。当温度一定时,水中碘的浓度与四氯化碳中碘的浓度比是一个常数。表1-3是碘在四氯化碳和水中分配情况。
| CB(I2在CCl4中)/mol.L-1 | CA(I2在H2O中)/mol.L-1 | CA/CB=K |
| 0.02 | 0.00023 | 0.0115 |
| 0.04 | 0.00046 | 0.0115 |
| 0.06 | 0.000702 | 0.0117 |
| 0.08 | 0.000928 | 0.0116 |
根据分配定律的原理,利用同一溶质在互不混溶的两种溶剂中溶解度的差别,可以选取适当溶剂,从另一溶液中将溶质提取出来。这个过程称为萃取。
萃取是一种有效的提纯、分离技术。为了充分使用一定量的萃取剂以提高萃取效率,采取每次少量,多次萃取的方法,要比一次用完萃取的效果好得多。反复多次萃取,萃取就可接近完全。
第二节 溶液的组成量度
溶液的组成量度旧称溶液的浓度.从1983年7月1日开始贯彻实施国家法定计量单位以后,单独使用”浓度”一词已有它特定的含义,它不能再作为一般的概念使用,应改称为溶液的组成量度。
溶液是由溶质和溶剂组成的,溶液的性质常常与溶液中溶质和溶剂的相对含量有关。给病人输液或用药时,必须规定药液的量度和用量。因为药液过稀,就不会产生明显的疗效,但药液过浓反而对人体有害,甚至会危及病员的生命安全。
一、溶液的组成量度表示法
物质的量和质量是国际单位制(SI)规定的基本量中的两个物理量,质量的SI单位为千克(kg),而质量的量的SI单位是摩尔(符号为mol)。SI规定:“一摩尔任何物质所含的基本单元数与0.012kg12C的原子相等.”已知,0.012kg12C中含有的原子数为阿佛加德罗常数NA约为6.023×1023mol-1.也就是说,一摩尔任何物质均含有NA个基本单元.在使用摩尔时应指明基本单元.它可以是原子、分子、离子、电子或其他粒子、或是这些粒子的特定组合。因此,物质的量和质量完全属于两个不同的概念。
溶液的组成量度,表示在一定量溶液或溶剂中所含溶质的量.在医学界过去根据不同的需要,曾用物质的量浓度、质量摩尔浓度、当量浓度、比例浓度和百分比浓度等表示。现在应使用法定的计量单位,世界卫生组织建议:①凡是已知相对分子质量的物质在人体内的含量,都应当用物质的量浓度单位取代旧单位制所表示的质量浓度单位。②人体体液中有少数物质的相对分子质量还未精确测得,因之不能用物质的量浓度表示其在人体内的含量,可以仍暂用质量浓度表示。③统一用升(L)作为单位的分母,以避免过去用其它作不同分母时的混乱,更不宜使用计量单位的“%”来表示每百毫升(/dl))。
(一)物质的量浓度
溶液中某溶质B的物质的量浓度,简称B的浓度,用符号cB或表示。它的定义是
cB=nB/V
式中nB是溶质B物质的量,其单位是摩尔(mol);V是溶液的体积,单位用升(L)表示。在说明cB时,也应同时指明基本单元。例如,H2SO4的量浓度c(H2SO4)=0.1mol•L-1;c(H+)或[H+]=0.1mol•L-1。又如,c(1/2H2SO4)=0.1mol•L-1等。括号中的符号表示物质的基本单元。
必须注意,凡是说到溶质B的浓度就是专指B的物质的量浓度。
(二)质量摩尔浓度
溶液中某溶质B的物质的量除以溶剂的质量,称为该溶质的质量摩尔浓度。单位为mol•kg-1,符号为mB。
mB=nB/W
式中W为该溶剂的质量,以千克(kg)作单位;nB是溶质B的物质的量,以摩尔作单位。
质量摩尔浓度的优点是不受温度的影响。对于极稀的水溶液来说,其物质的量浓度与质量摩尔浓度的数值几乎相等。
(三)百分浓度
百分浓度不是法定的计量单位,应避免使用,但至今在国内外书刊中仍然大量使用百分浓度。现行的百分浓度可有三种表示方法:小数表示法、质量体积表示法与物质的量浓度表示法。
1.当百分浓度表示相同单位相对含量,即为W/W,V/V百分含量时,应用小数表示成相应质量分数和体积分数。
例如,NaCL在水中的质量百分浓度为25%,可改成NaCL在水中的质量分数为0.25或W(NaCL)=0.25.。
又如,乙醇在水中体积百分浓度为75%,或改成乙醇在水中的体积分数为0.75或V(C2H5OH)=0.75.
2.当百分浓度表示的是质量体积(W/V)不同单位的相对含量,且被测物质为未知确切化学结构者或混合物时,应用质量体积浓度表示.如总蛋白,某些激素百分浓度,可用g•L-1,mg·L-1,μg·L-1,ng·L-1等表示.
3.对于已知结构的物质,如葡萄糖、钾、钠等,其相对分子质量或相对原子质量是已知的,这类物质的质量体积百分浓度,应表示为物质的量浓度,即用mol·L-1,mmol·-1,umol·L-1等表示。
二、 溶液的配制
配制某物质的具有一定组成量度的溶液,可由某纯物质加入溶剂,或将其溶液稀释,也可用不同组成量度的溶液相混合。无论用哪一种方法,都应遵守“配制前后溶质的量不变”的原则。主要公式有:
m/M×1000=cBv (1-3)
c1V1=c2V2(1-4)
式中m为溶质的质量;M为溶质的摩尔质量(g·mol-1);cB为溶质的量浓度mol·L-1;V为溶液的体积(mL);c1.c2分别为溶液稀释前后的组成量度;V1、V2为稀释前后的体积。
例3 配制0.1mol·L-1Na2CO3溶液500mL,应称取Na2CO3多少克?
解:设称取Na2CO3为mg,则
m/106×1000=0.1×500
m=5.30(g)
例4 现有在水中的体积分数为0。95的乙醇,若需1L体积分数为0.75的消毒酒精,应如何配制?
解:设所需体积分数为0.95的乙醇为VmL,则
0.95V=0.75×1000
V=789.5(mL)
配制方法是:准确量取体积分数为0.95的乙醇789.5mL,加水稀释至1000mL,即可制得体积分数为0.75的消毒酒精。
例5 配制0.1mol·L-1CuSO4溶液100ML,需称取CuSO4·5H2O多少g?
解:设需称取CuSO4·5H2O为mg,则
m/249.7×1000=0.1×100
m=2.497(g)
即需称取2.497gCuSO4·5H2O。
例6 某患者需用0.56mol·L-1葡萄糖溶液,现有2.78mol·L-1和0.28mol·L-1葡萄溶液两种,问要用这两种溶液各多少毫升或配制0.56mol·L-1溶液500mL?
解:设应取2.78mol·L-1葡萄糖溶液为χmL,则
2.78χ+0.28×(500-χ)=0.56×500
χ=56(mL)
应取0.28mol·L-1葡萄糖溶液为
500-56=444(mL)
第三节 溶液的渗透压
渗透作用是自然界的一种普遍现象,它对于人体保持正常的生理功能有着十分重要的意义。下面讨论渗透作用的基本原理、渗透压及其在医学上的意义。
一、渗透现象和渗透压
在蔗糖浓溶液上小心加入一层清水,水分子即从上层渗入下层,蔗糖分子也由下层涌入上层,直到蔗糖溶液的浓度均匀为止。一种物质的粒子自发地分布于另一种物质中的现象称为扩散。
如果将蔗糖水溶液与水用半透膜隔开(图1-2甲),使膜内和膜外液面相平,静置一段时间后,可以看到膜内溶液的液面不断上升(图1-2乙),说明水分子不断地透过半透膜进入溶液中。溶剂透过半透膜进入溶液的自发过程称为渗透现象。不同浓度的两种溶液被半透膜隔开时都有渗透现象发生。
半透膜是一种只允许某些物质透过,而不允许另一些物质透过的薄膜。上面实验中的半透膜只允许水分子透过,而蔗糖分子却不能透过。细胞膜、膀胱膜、毛细血管壁等生物膜都具有半透膜的性质。人工制造的火棉胶膜、玻璃纸等也具有半透膜的性质。
上述渗透现象产生的原因是蔗糖分子不能透过半透膜,而水分子却可以自由通过半透膜。由于膜两侧单位体积内水分子数目不等,水分子在单位时间内从纯水(或稀溶液)进入蔗糖溶液的数目,要比蔗糖溶液中水分子在同一时间内进入纯水(或稀溶液)的数目多,因而产生了渗透现象。渗透现象的产生必须具备两个条件:一是有半透膜存在,二是半透膜两侧必须是两种不同浓度的溶液。
图1-2是渗透过程的示意图,图中v入表示水分子进入半透膜内的速度,v出表示膜内水分子透出到膜外的速度。甲表示渗透刚开始,乙表示渗透不断进行,管内液面不断上升。但是液面的上升不是无止境的,而是达到某一高度时便不再上升(图1-2丙),此时,v入=v出,渗透达到平衡状态即渗透平衡。阻止纯溶剂向溶液中渗透,在溶液液面上所施加的压力为该溶液的渗透压。
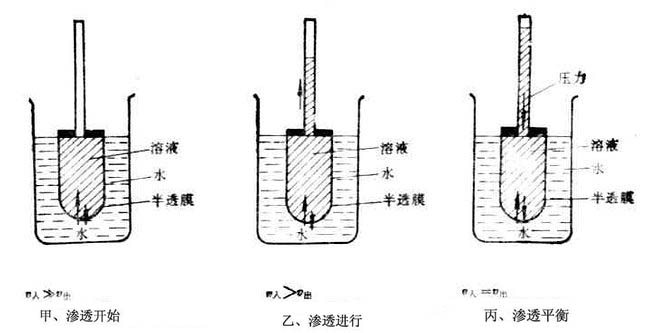
如果被半透膜隔开的是两种不同浓度的溶液,这时液柱产生的静液压,既不是浓溶液的渗透压,也不是稀溶液的渗透压,而是这两种溶液渗透压之差。
渗透压的单位用Pa或kPa表示。
渗透压是溶液的一个重要性质,凡是溶液都有渗透压。渗透压的大小与溶液的浓度和温度有关。
二、渗透压与浓度、温度的关系
1886年范特荷甫(van’t Hoff)根据实验数据得出一条规律:对稀溶液来说,渗透压与溶液的浓度和温度成正比,它的比例常数就是气体状态方程式中的常数R。这条规律称为范特荷甫定律。用方程式表示如下:
πV=nRT
或π=cRT(1-5)
式中π为稀溶液的渗透压,V为溶液的体积,c为溶液的浓度,R为气体常数,n为溶质的物质的量,T为绝对温度。
式(1-5)称为范特荷甫公式,也叫渗透压公式。常数R的数值与π和V的单位有关,当π的单位为kPa,V的单位为升(L)时,R值为8.31kPa•L•K-1•mol-1。
范特荷甫公式表示,在一定温度下,溶液的渗透压与单位体积溶液中所含溶质的粒子数(分子数或离子数)成正比,而与溶质的本性无关。
对于稀溶液,c近似于质量摩尔浓度,因此上式又可写成
π=mBRT
对于相同cB的非电解质溶液,在一定温度下,因为单位体积溶液中所含溶质的粒子(分子)数目相等,所以渗透压是相同的。如0.3mol•L-1葡萄糖溶液与0.3mol•L-1蔗糖溶液的渗透压相同。但是,相同cB的电解质溶液和非电解质溶液的渗透压则不相同。例如,0.3mol.L-1NaCl溶液的渗透压约为0.3mol.L-1葡萄糖溶液渗透压的2倍。这是由于在NaCl溶液中,每个NaCl粒子可以离解成1个Na+和1个Cl-。而葡萄糖溶液是非电解质溶液,所以0.3mol•L-1NaCl溶液的渗透压约为0.3 mol•L-1葡萄糖溶液的2倍。
由此可见,渗透压公式中,对电解质溶液来说,浓度cB(或mB)是1升溶液中能产生渗透效应的溶质分子与离子总物质的量,称为渗透物质的量浓度。
通过测定溶液的渗透压,可以计算溶质的相对分子质量。如果溶质的质量为m,摩尔质量为M。实验测得溶液的渗透压为π,则该溶质的相对分子质量(数值等于摩尔质量)可通过下式求得:
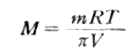 (1-6)
(1-6)
式(1-6)主要用于测定高分子(蛋白质等)的相对分子质量。
渗透压公式在医疗工作中有其现实意义。人体血液的渗透压在正常体温(37℃)时约为769.9kPa。要配制与血液渗透压相等的溶液,即可由渗透压公式计算出溶液的浓度。
三、渗透压在医学上的意义
(一)等渗、低渗、高渗溶液
渗透压相等的两种溶液称为等渗溶液。渗透压不同的两种溶液,把渗透压相对高的溶液叫做高渗溶液,把渗透压相对低的溶液叫做低渗溶液。对同一类型的溶质来说,浓溶液的渗透压比较大,稀溶液的渗透压比较小。因此,在发生渗透作用时,水会从低渗溶液(即稀溶液)进入高渗溶液(即浓溶液),直至两溶液的渗透压达到衡为止。
在医疗实践中,溶液的等渗、低渗或高渗是以血浆总渗透压为标准。即溶液的渗透压与血浆总渗透压相等的溶液为等渗溶液。溶液的渗透压低于血浆总渗透压的溶液为低渗溶液。溶液的渗透压高于血浆总渗透压的溶液为高渗溶液。
给伤病员进行大量补液时,常用与血浆等渗的0.154mol•L-1NaCl溶液(生理盐水),而不能用0.256 mol•L-1NaCl的高渗溶液或0.068 mol•L-1NaCl的低渗溶液。这是与血浆渗透压有关的问题。下面讨论红细胞分别在这三种NaCl溶液中所产生的现象。
将红细胞放到0.068 mol•L-1NaCl溶液中,在显微镜下可以看到红细胞逐渐膨胀,最后破裂。医学上称这种现象为溶血。这是因为红细胞内液的渗透压大于0.068mol·L-1NaCL溶液渗透压,因此,水分子就要向红细胞内渗透,使红细胞膨胀,以致破裂.如将红细胞放到0.256mol·L-1NaCL溶液中,在显微镜下可以看到红细胞逐渐皱缩,这种现象称为胞浆分离.因为这时红细胞内液的渗透压小于0.256mol·L-1NaCL溶液的渗透压,因此,水分子由红细胞内向外渗透,使红细胞皱缩.如将红细胞放到生理盐水中,在显微镜下看到红细胞维持原状.这是因为红细胞与生理盐水渗透压相等,细胞内外达到渗透平衡的缘故.图1-3为细细胞在不同浓度NaCL溶液中的形态图。
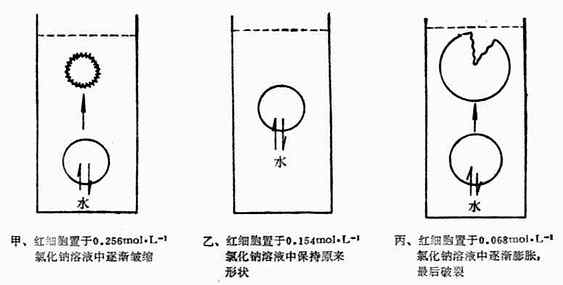
图1-3 红细胞在不同浓度NaCl溶液中的形态未意图
在医疗工作中,不仅大量补液时要注意溶液的渗透压,就是小剂量注射时,也要考虑注射液的渗透压。但临床上也有用高渗溶液的,如渗透压比血浆高10倍的2.78mol·L-1葡萄糖溶液。因对急需增加血液中葡萄糖的患者,如用等渗溶液,注射液体积太大,所需注射时间太长,反而不易收效。需要注意,用高渗溶液作静脉注射时,用量不能太大,注射速度不可太快,否则易造成局部高渗引起红细胞皱缩。当高渗溶液缓缓注入体内时,可被大量体液稀释成等渗溶液。对于剂量较小浓度较稀的溶液,大多是将剂量较小的药物溶于水中,并添加氯化钠、葡萄糖等调制成等溶液,亦可直接将药物溶于生理盐水或0.278mol·L-1葡萄糖溶液中使用,以免引起红细胞破裂。
(二)毫渗透量浓度
人的体液中既有非电解质(如葡萄糖等),也有电解质(如NaCL,CaCL2,NaHCO3等盐类)。为了表示体液总的渗透压大小,医学上常用毫渗透量浓度来比较,简称毫渗量·升-1,用mOsm·L-1表示。这种浓度是溶液中能产生渗透作用的溶质的粒子(分子或离子)的总物质的量浓度。
例7分别计算0.278mol·L-1葡萄糖溶液和生理盐水(0.154mol·L-1NaCL)的毫渗透量浓度。
解:0.278mol·L-1葡萄糖溶液的毫渗透量浓度为:0.278×1000=278≈280(mOsm·L-1)生理盐水的毫渗透量浓度为:0.154×2×1000=308(mOsm·L-1)
由于在一定温度下,溶液的渗透压与溶液的毫渗量·升-1成正比,因此,常用它来衡量或比较溶液渗透压的大小.表1-4为正常人血浆中各种离子的毫渗量浓度.
从表4-1可看出,正常人血浆中各种离子的总浓度为151.0+139.5=290.5mOsm·L-1(血浆中非电解质如葡萄糖、尿素等含量较少,仅相当于5mOsm·L-1左右)。临床上规定血浆总渗量浓度正常范围是280~320mOsm·L-1。如果溶液的毫渗透量浓度处于这个范围以内,则为血浆的等渗溶液;小于此范围的溶液为低渗溶液;大于此范围的溶液则为高渗溶液。
表1-4 正常人血浆中各种离子的mOsm·L-1
| 正离子 | mOsm·L-1 | 负离子 | mOsm·L-1 |
| Na+ | 142 | CL- | 103 |
| K+ | 5 | HCO3- | 27 |
| Ca+ | 2.5 | HPO42- | 1 |
| Mg2+ | 1.5 | SO42- | 0.5 |
| 有机酸 | 6 | ||
| 蛋白质 | 2 | ||
| 总量 | 151.0 | 总量 | 139.5 |
由例7计算结果说明生理盐水为血浆的等渗溶液,0.278mol.L-1葡萄糖溶液为278mOsm·L-1近似于280mOsm·L-1,所以它也是血浆的等渗溶液.
临床上常用的等渗溶液有:
1. 生理盐水(0.154mol·L-1NaCL溶液),毫渗透量深度为308mOsm·L-1。
2.0.278mol·L-1葡萄糖溶液,亳渗量溶液浓度为278mOsm·L-1(近似于280mOsm·L-1)。
3.0.149mol·L-1碳酸氢钠溶液,毫渗透量浓度为298mOsm·L-1。
临床上常用的高渗溶液有:
1.0.513mol·L-1.NaCL溶液,毫渗透量浓度为1026mOsm·L-1.
2.0.278mol·L-1葡萄糖氯化钠溶液(是生理盐水中含0.278mol·L-1葡萄糖),毫渗透量浓度应为308+278=586mOsm·L-1,其中生理盐水维持渗透压,葡萄糖则供给热量和水.
3.2.78mol·L-1葡萄糖溶液,毫渗透量浓度为2780mOsm·L-1。
(三) 晶体渗透压和胶体渗透压
血浆中含有低分子的晶体物质(如氯化钠、葡萄糖和碳酸氢钠等)和高分子的胶体物质(如蛋白质)。血浆中的渗透压是这两类物质所产生渗透压的总和。其中由低分子晶体物质产生的渗透压叫做晶体渗透压;由高分子胶体物质产生的渗透压叫做胶体渗透压。
血浆中低分子晶体物质的含量约为0.7%,高分子胶体物质的含量约为7%.虽然高分子胶体物质的百分含量高,它们的相对分子质量却很大,因此,它们的粒子数很少.低分子晶体物质在血浆中含量虽然很低,但由于相对分子质量很小,多数又可离解成离子,因此粒子数较多.所以,血浆总渗透压绝大部分是由低分子的晶体物质产生的.在37℃时,血浆总渗透压约为769.9kPa,其中胶体渗透压仅为2.9~4.0kPa.
人体内半透膜的通透性不同,晶体渗透压和胶体渗透压在维持体内水盐平衡功能上也不相同。胶体渗透压虽然很小,但在体内起着重要的调节作用。
细胞膜是体内的一种半透膜,它将细胞内和细胞外液隔开,并只让水分子自由透过膜内外,而K+、Na+则不易自由通过。因此,水在细胞内外的流通,就要受到盐所产生的晶体渗透压的影响。晶体渗透压对维持细胞内外水分的相对平衡起着重要作用。临床上常用晶体物质的溶液来纠正某些疾病所引起的水盐失调。例如,人体由于某种原因而缺水时,细胞外液中盐的浓度将相对升高,晶体渗透压增大,于是使细胞内液的水分通过细胞膜向细胞外液渗透,造成细胞内液失水。如果大量饮水或者输入过多的葡萄糖溶液,则使细胞外液盐浓度降低,晶体渗透压减小,细胞外液中的水分向细胞内液中渗透,严重时可产生水中毒。高温作业之所以饮用盐汽水,就是为了保持细胞外液晶体渗透压的恒定。
毛细血管壁也是体内的一种半透膜,它与细胞膜不同,它间隔着血浆和组织间液,可以让低分子如水、葡萄糖、尿素、氢基酸及各种离子自由透过,而不允许高分子蛋白质通过。所以,晶体渗透压对维持血液与组织间液之间的水盐平衡不起作用。如果由于某种原因造成血浆中蛋白质减少时,血浆的胶体渗透压就会降低,血浆中的水就通过毛细血管壁进入组织间液,致使血容量降低而组织液增多,这是形成水肿的原因之一。临床上对大面积烧伤,或者由于失血而造成血容量降低的患者进行补液时,除补以生理盐水外,同时还需要输入血浆或右旋糖酐等代血浆,以恢复血浆的胶体渗透压和增加血容量。
第二章 电解质溶液
电解质分为强电解质和弱电解质.强电解质在水溶液中全部离解或近乎全部离解.而弱电解质在水溶液中只有一小部分离解。这两类电解质溶液的性质有较大差别。
电解质在水溶液中离解出来的离子全部都是水化的,但由于参加水化的水分子数目并不固定,所以在书写时仍以简单离子的符号表示,如H+、Na+、OH-离子等。
电解质在化学和生产上经常遇到,与人体亦关系密切,它常以一定浓度的离子形式广泛存在于人的体液和组织液中,其含量关系到人体的生理工能。因此,研究电解质溶液的有关性质,对医科学生来说很有必要。
第一节 电解质在溶液中的离解
一、一元弱酸弱碱的离解平衡
(一)离解度和离解常数
一元弱酸弱碱(如HOAc,NH3等)是弱电解质,在溶液中只能部分离解。离解程度用离解度表示。
离解度是指溶液中已经离解的电解质的分子数占电解质总分子数(已离解的和未离解的)的百分数。通常用α表示。

一元弱酸HA存在以下的离解平衡:
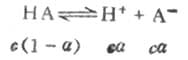
平衡浓度为
c(1-α) cα cα其中c为HA的总浓度,α为离解度。
离解常数KI可表示为
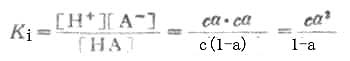 (2-1)
(2-1)
KI在一定温度下为一常数,不能随浓度变化而变化。弱酸的离解常数习惯上用Ka表示,弱碱的离解常数用Kb表示。
如果弱电解质离解度α很少,则
1-α≈1
这时式(2-1)为
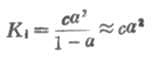
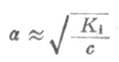 (2-2)
(2-2)
从式(2-2)可以看出,在一定温度下,同一弱电解质的离解度大约与溶液浓度的平方根成反比,即离解度随溶液的稀释而升高。这条说明溶液浓度与离解度关系的定律,叫做稀释定律。式(2-2)叫做稀释定律公式。利用此公式可以进行有关离解试或离解常数的计算。
例1在25℃时,已知(1)0.1mol·L-1HOAc的离解度为1.32%;(2)0.2mol·L-1HOAc的离解度为0.93%,求HOAc的离解常数。
解:(1)
(2)
从例1可以看出,对不同浓度HOAc溶液,在一定温度下,所计算出来的离解常数基本是一致的。表2-1是HOAc溶液在25℃时,不同浓度的离解度以及由离解度计算出来的离解常数值。
表2-1 25℃,不同浓度醋酸的离解度和离解常数
| 浓度/mol·L-1 | 离解度/% | 离解常数 |
| 0.001 | 12.4 | 1.76×10-5 |
| 0.01 | 4.1 | 1.76×10-5 |
| 0.02 | 2.96 | 1.80×10-5 |
| 0.1 | 1.32 | 1.76×10-5 |
| 0.2 | 0.93 | 1.76×10-5 |
利用离解常数可以计算一定浓度某弱酸溶液中的H+浓度,或计算弱碱溶液中的OH-=浓度。
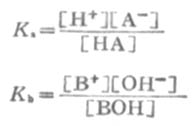
式中HA为弱酸,BOH为弱碱。
在浓度为c的弱酸中,[H+]=cα,即α=[H+]/c,又根据稀释定律,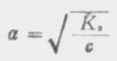 , 则
, 则
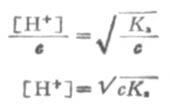 (2-3)
(2-3)
同理,在浓度为c的弱碱溶液中,
![]() (2-4)
(2-4)
根据式(2-3)和式(2-4),可以计算一定浓度的弱酸或弱碱的[H+]或[OH-]。
离解常数的大小用以衡量酸或碱的强弱程度。酸或碱越弱,它们的离解常数值就越小。一般认为KI在10-5至10-9范围内的电解质是弱电解质;KI值小于10-10时是极弱电解质。
(二)影响离解平衡的因素
弱酸和弱碱的离解平衡都是暂时的、相对的动态平衡。当外界条件改变时,离解平衡像其它平衡一样,会发生移动,结果弱酸和弱碱的离解程度都有所增减。因此,可以应用平衡移动原理,通过改变外界条件,控制弱酸和弱碱的离解程度。外界条件主要指温度,同离子效应和盐效应的影响。
1.温度的影响
温度变化能使离解平衡发生移动,这种移动是通过离解常数的改变实现的,但在常温范围内变化不大。
2.同离子效应
离子浓度的改变,对弱酸和弱碱离解程度的影响极为显著。
例如,在醋酸溶液中加入一些醋酸钠,由于醋酸钠是强电解质,在水溶液中完全离解Na+OAc-,这样溶液中[OAc-]增大,使![]()
离解平衡向左移动,从而降低了醋酸的离解度和溶液中的H+浓度。
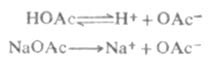
又如,在氨水中加入一些氯化铵,由于氯化铵是强电解质,在水溶液中完全离解成NH4+和CL-,这样溶液中[NH4+]增大,使离解平衡向左移动,从而降低了氨水的离解度和溶液中的OH-浓度。
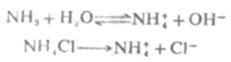
由此可以得出结论,在弱电解质溶液中,加入与弱电解质具有相同离子的强电解质,使弱电解质的离解度降低的效应,称为同离子效应。
3.盐效应
在弱电解质溶液中,加入与弱电解质没有相同离子的强电解质,而使弱电解质的离解度略微增大的效应,称为盐效应。
盐效应的产生,是由于强电解质的加入,使溶液中离子间的相互牵制作用增强,离子结合成分子的机会减少,降低了分子化的程度,因而达到平衡时,弱电解质的离解度比未加入强电解质时略微大些。
例如,在0.1mol·L-1HOAc溶液中加入NaCL晶体,使NaCL的浓度为0.1mol·L-1时,[H+]不是1.32×10-3mol·L-1,而是1.70×10-3mol·L-1,离解度不是1.32%而是1.70%.
应该指出,在发生同离子效应的同时,必然伴随着盐效应的发生.这两个效应对弱电解质离解度影响不同.盐效应可以使弱电解质的离解度增大一些,而同离子效应可以使弱电解质的离解度大大降低.这说明同离子效应和盐效应对溶液酸碱性的影响是不能相提并论的.因此,对稀溶液来说,如不考虑盐效应,是不会引起很大误差的.
二、多元酸碱在溶液中的离解
多元酸碱在溶液中的离解是分步进行的,叫做分步离解。表2-2列出了一些常见的多元酸的分步离解常数。表中pKa为Ka的负对数值。
表2-2 一些常见的多元酸的分步离解常数
| 名称 | 分子式 | Ka1 | PKa1 | Ka2 | PKa2 | Ka3 | PKa3 | |
| 酸性强度增加 | 草酸 | H2C2O4 | 5.4×10-2 | 1.27 | 5.4×10-5 | 4.27 | 2.2×10-13 | 12.67 |
| 亚硫酸 | H2SO3 | 1.54×10-2 | 1.81 | 1.02×10-7 | 6.91 | |||
| 磷酸 | H3PO4 | 7.52×10-3 | 2.12 | 6.23×10-8 | 7.21 | |||
| 丙二酸 | CH2(COOH)2 | 1.38×10-3 | 2.86 | 2×10-6 | 5.70 | |||
| 邻苯二甲酸 | C6H4(COOH)2 | 1.12×10-3 | 2.95 | 3.9×10-5 | 5.41 | |||
| 酒石酸 | (CHOHCOOH)2 | 9.1×10-4 | 3.04 | 4.3×10-5 | 4.37 | |||
| 碳酸 | H2CO3 | 4.30×10-7 | 6.37 | 5.61×10-11 | 10.25 | |||
| 氢硫酸 | H2S | 9.1×10-8 | 7.04 | 1.1×10-12 | 11.96 |
例如草酸(H2C2O4)的离解分两步进行。
一级离解
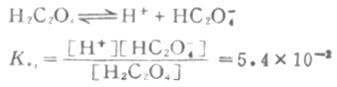
二级离解
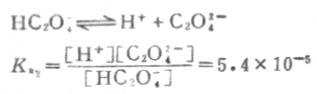
二级离解总比一级离解困难,因为H+要克服带有两个电荷的C2O2-4对它的吸引。从Ka1和Ka2可以反映这一点。草酸溶液中的HC2O-4浓度要比C2O2-4浓度大得多。
磷酸的离解要分三步,有Ka1、Ka2、和Ka3三个离解常数,且Ka1》Ka2》Ka3。这说明多元酸分级离解是依次变难。
根据多元酸的浓度和各级离解常数,可以算出溶液中各种离子的浓度。
例2 计算0.1mol·L-1H2S溶液中的H+和S2-的浓度。
解:由于H2S的 Ka1》Ka2,所以H2S溶液中的H+主要来自第一步离解,而第一步离解所产生的H+,又抑制第二步离解。这样计算H2S溶液中H+的总浓度时,可以忽略第二步离解的H+,近似地等于第一步离解平衡时H+浓度。
设第一步离解平衡时[H+]=x,则[H+]≈[HS-],平衡时则有下列关系:
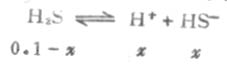
由表2-2知H2S的Ka为9.1×10-8,则
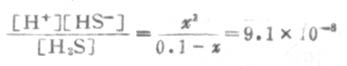
因Ka1很小,x必然很小,所以0.1-x≈0.1,则
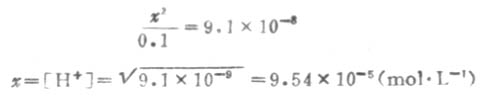
溶液中的S2-是第二步离解的产生,因此,计算溶液中的S2-浓度时,应根据第二步离解平衡进行计算.
设第二步离解时,[S2-]=y,平衡时有下列关系:
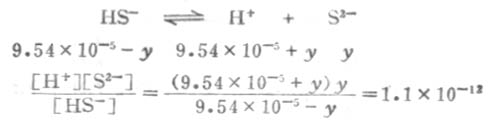
因为Ka1极小,y必然极小,所以9.54×10-5±y≈9.54×10-5,则
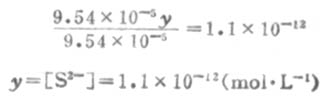
所以,[S2-]≈Ka2。
三、强电解质在溶液中的离解
(一)离子互吸学说
稀释定律适用于弱电解质溶液,而不适用于强电解质溶液。为了阐明强电解质在溶液中的实际情况,德拜(Debye)和休克尔(Huckel)提出了离子互吸学说,又叫完全电离学说。这种学说认为,强电解质在水溶液中完全离解成离子,离子在水溶液中并不完全自由。带异号电荷的离子相互吸引,距离近的吸引力大;带同号电荷的离子相互排斥,距离近的排斥力大。因此,离阳离子越近的地方,阳离子越少,阴离子越多;离阴离子越近的地方,阴离子越少,阳离子越多。总的结果是,任何一个离子都好像被一层球形对称的异号电荷离子所包围着。这层在中心阳离子周围所构成的球体,叫做离子氛。如图2-1所示,位于球体中心的离子称为中心离子,在中心阳离子周围有阴离子氛,在中心阴离子周围有阳离子氛。
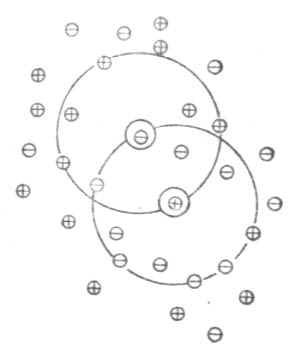
图2-1 离子氛示意图
在离子氛的影响下,溶液中的离子受到带有相反电离子荷氛的影响,而不能完全自由活动。使强电解质溶液中的离子不能百分之百地发挥应有的效能。因此,实测的离解度总是小于100%,这不是强电解质的真实离解度,它反映了溶液中离子间相互影响的程度,我们把这种离解度称为“表现离解度”。而强电解质的真实离解度是100%。
后来发现在强电解质溶液中,不但有离子氛存在,而且相反电荷的离子还可以缔合成离子对作为一个独立单位而运动。有的离子对没有导电能力。离子对在遇到强力碰撞时,可以分开,随后又可以重新形成新的离子时对。离子对的存在也使自由离子的浓度下降,导致溶液的导电能力下降。
离子氛和离子对的形成显然与溶液的浓度和离子电荷有关。溶液愈浓,离子所带的电荷愈多,上述效应愈显著。
如取不同浓度的KCL溶液,测定它的离解度(α)值,根据稀释定律求得相就的“离解常数”值如表2-3。
表2-3 18℃,不同浓度KCL溶液的“离解度”和“离解常数”
| 浓度/mol·L-1 | 离解度/% | 离解常数 |
| 0.01 | 94.2 | 0.152 |
| 0.1 | 86.2 | 0.536 |
| 1.0 | 75.6 | 2.34 |
| 2.0 | 71.2 | 3.52 |
由表2-3可以看出,强电解质”离解常数”K随溶液浓度的不同变化很大,这说明强电解质不存在离解常数.也就是说强电解质在溶液中是完全离解的,不存在离解平衡,因而就不存在离解度和离解常数.稀释定律是以弱电解质的可逆性过程为基础推导得出的,所以它不适用于强电解质溶液,不能客观地阐明强电解质在溶液中的实际情况.
(二)离子活动和活度系数
由于强电解质溶液中存在离子氛和离子对,每个离子不能完全自由地发挥它在导电等方面的作用,路易斯(Lewis)就提出了活度的概念.离子活度是溶液中离子的有效浓度.它等离子和活度系数的乘积.设离子的浓度为c,活度系数为f,则离子的活度(α)为:α=fc (2-5) 或f=α/c
活度系数f反映了离子间存在着相互影响这一因素.由于离子的活度一般都比浓度小,所以f一般都小于1.活度系数大,表示离子牵制作用弱,离子活动的自由程度大.溶液愈稀,活度系数愈接近于1.当溶液无限稀释时,活度系数等于1,这时离子的运动完全自由,离子活动就等于离子浓度.
因为电解质溶液中必定同时存在阳离子和阴离子,实验无法独测出阳离子的活度系数或阴离子的活度系数.但实验可以测出一个电解质的阳/阴离子的平均活度系数(f±).强电解质溶液的活度一般指溶液的平均活度(α±)
α±= f±×c
表2-4列举了25℃时,一些强电解质的离子平均活度系数.
表2-4 一些强电解质的离子平均活度系数(25℃)
| 电解质 | C/mol·L-1 | ||||||
| 0.001 | 0.005 | 0.01 | 0.05 | 0.1 | 0.5 | 1.0 | |
| HCL | 0.966 | 0.928 | 0.904 | 0.803 | 0.796 | 0.758 | 0.809 |
| KOH | 0.96 | 0.92 | 0.90 | 0.82 | 0.80 | 0.73 | 0.76 |
| KCL | 0.965 | 0.927 | 0.901 | 0.815 | 0.769 | 0.651 | 0.606 |
| H2SO4 | 0.630 | 0.639 | 0.544 | 0.340 | 0.265 | 0.154 | 0.130 |
| Ca(NO3)2 | 0.88 | 0.77 | 0.71 | 0.54 | 0.48 | 0.38 | 0.35 |
| CuSO4 | 0.74 | 0.53 | 0.41 | 0.21 | 0.16 | 0.068 | 0.047 |
例3 已知25℃时,0.1mol·L-1KCL溶液中,离子的平均活度系数为0.769,求离子的平均活度.
解:已知f±=0.769 c=0.1 mol·L-1
α±=0.769×0.1=0.0769×mol·L-1
(三)离子强度
溶液中离子的活度系数不仅与它的浓度有关,并且还与溶液中其它各种离子的总浓度和离子的电荷数有关,但与离子的种类无关.因此,溶液中离子的浓度和离子的电荷数就成为影响离子活度系数的主要因素.为了阐明离子浓度和离子电荷数对离子活度的影响,引入了离子度的概念.离子强度表示溶液中离子所产生的电场强度.它是溶液中各种离子的量浓度乘以离子电荷数的平方总和的二分之一
![]() (2-6)
(2-6)
式中,I代表溶液的离子浓度;c是离子的量浓度;z是离子的电荷数.
例4 求0.01mol·L-1NaCL溶液的离子强度.
解:I=1/2×(0.01×12+0.01×12)=0.01
例5 溶液中含有0.05mol·L-1NaCL和0.01 mol·L-1KCL,求该溶液的离子强度.
解:I=1/2×(0.05×12+0.05×12+0.01×12+0.01×12)=0.06
离子活度系数随溶液中离子强度的改变而显著改变,表2-5列出了离子强度和平均活度系数的关系.溶液中离子强度越大,离子间的相互影响越强,离子活动受到的限制就越大。只有当溶液接近于无限稀释时,离子强度趋近于零,离子才能完全自由活动,这时离子的活度生活费数就接近于1,即离子活度就接近于离子的真实浓度。
表2-5 不同离子强度时离子的活度系数(25℃)
| 活度系数 离子强度 |
电 荷 数 | |||
| 1 | 2 | 3 | 4 | |
| 1×10-4 | 0.99 | 0.95 | 0.90 | 0.83 |
| 2×10-4 | 0.98 | 0.94 | 0.87 | 0.770.77 |
| 5×10-4 | 0.97 | 0.90 | 0.80 | 0.67 |
| 1×10-3 | 0.96 | 0.86 | 0.73 | 0.56 |
| 2×10-3 | 0.95 | 0.81 | 0.64 | 0.45 |
| 5×10-3 | 0.92 | 0.72 | 0.51 | 0.30 |
| 1×10-2 | 0.89 | 0.63 | 0.39 | 0.19 |
| 2×10-2 | 0.87 | 0.57 | 0.28 | 0.12 |
| 5×10-2 | 0.81 | 0.44 | 0.15 | 0.04 |
| 0.1 | 0.78 | 0.33 | 0.08 | 0.01 |
| 0.2 | 0.70 | 0.24 | 0.04 | 0.003 |
| 0.3 | 0.66 | 0.62 | - | - |
| 0.5 | 0.62 | - | - | - |
采用离子强度的目的,是因为离子的活度系数的测定方法一般比较复杂,不容易测定。但是,离子活度系数与离子强度间却存在着一定的联系,并且离子强度很容易由离子的浓度与其所带电荷而求得。在测定离解迷路数时等精密工作中,要求对离子的有效浓度作精确计算,这就需要由离子将浓度换算成活度。但在一般有关稀溶液的计算中,可直接换算成活度。
第二节 酸碱质子理论
一、权碱概念
酸碱离子理论是阿累尼乌其斯(Arrhenius)根据他的电离学说提出来的。他认为在水中能电离出氢离子并且不产生其它阳离子的物质叫酸。在水中能电离出氢氧根离子并且不产生其它阴离子的物质叫碱。酸碱中和反应的实质是氢离子和氢氧根离子结合成水。这个理论取得了很大成功,但它的局限性也早就暴露出来。倒台,气态氨与氯脂氢反应迅速生成氯化铵,这个酸碱中和反应并墙角水的生成;又如氨的水溶液显碱性,曾错误地认为NH3和H2O形成弱电解质NH4OH分子,然后离解出OH-+等。
由于阿累尼乌斯的酸碱离子理论不能解一些非水溶液中进行地酸碱反应等问题,1923年布朗特(Bronsted)提出了酸碱质子理论,把酸碱概念加以推广。酸碱质子理论认为凡是能给出质子的物质都是酸,凡是能与质子结合的物质都是碱。即酸是质子的给予体,碱是质子的接受体。这样,一个酸给出质子后余下的部分自然就是碱,因为它本身就是与质子结合的。它们的关系如下:
![]()
这种关系叫做酸碱的共轭关系,式中略去了HB和B可能出现的电荷。右边的碱是左边酸的共轭碱,左边的酸是右边碱的共轭酸,两者组成一个共轭酸碱对,它们只直差一个质子。
例如,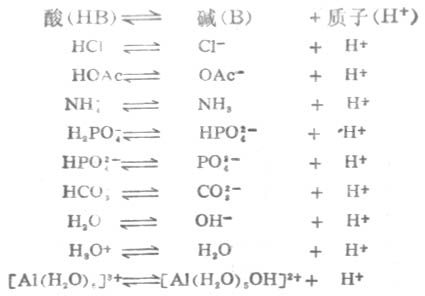
从以上例子可以看出,酸和碱可以是分子,也可以是阳离子和阴离子。还可以看出,像HPO2-4这样的
物质,既表现酸,也表现为碱,所以它是两性物质。同理,H2O,HCO-3等也是两性物质。
二、共轭酸碱的强弱
共轭酸碱对的离解常数Ka和Kb之间有确定的关系。以HOAc为例推导如下:
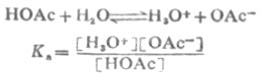
由于溶剂水的浓度不常数,所以它不出现在平衡常数式中。
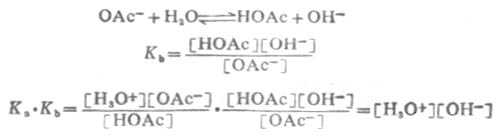
用KW表示[H3O+][OH-],KW称为水的离子积。这说明在一定温度下,水中的[H3O+]与[OH-]的乘积为一常数。所以 Ka·Kb=KW (2-7)
24℃时KW值为1.0×10-14.这个关系说明,只知道了酸的离解常数Ka,就可以计算出它的共轭碱的Kb,反之亦然。Ka和Kb是成反比的,而Ka和Kb正是反映酸和碱的强度,所以,在共轭酸碱对中,酸的强度愈大,其共轭碱的强度愈小;碱的强度愈大,其共轭酸的强度愈小。表2-6列出了一些共轭厔碱对的强度次序。
表2-6 共轭酸碱的强度次序
| 酸性增强 | 共轭酸(HB) | Ka(在水中) | pKa(在水中) | 共轭碱(B) | 碱性增强 |
| H3O+ | H2O | ||||
| H2C2O4 | 5.4×10-2 | 1.27 | HC2O-4 | ||
| H2SO3 | 1.54×10 | 1.81 | HSO-3 | ||
| HSO-4 | 1.20×10-2 | 1.92 | SO2-4 | ||
| H3PO4 | 7.51×10-3 | 2.12 | H2PO-4 | ||
| HNO2 | 4.6×10-4 | 3.37 | NO-2 | ||
| HF | 3.53×10-4 | 3.45 | F- | ||
| HCOOH | 1.77×10-4 | 3.75 | HCOO- | ||
| HC2O-4 | 5.4×10-5 | 4.27 | C2O2-4 | ||
| CH3COOH | 1.76×10-5 | 4.75 | CH3COO- | ||
| H2CO3 | 4.30×10-7 | 6.37 | HCO-3 | ||
| HSO-3 | 1.02×10-7 | 6.91 | SO2-3 | ||
| H2S | 9.1×10-8 | 7.04 | HS- | ||
| H2PO-4 | 6.23×10-8 | 7.21 | HPO2-4 | ||
| NH+4 | 5.68×10-10 | 9.25 | NH3 | ||
| HCN | 4.93×10-10 | 9.31 | CH- | ||
| HCO-3 | 5.61×1011 | 10.25 | CO2-3 | ||
| H2O2 | 2.4×10-12 | 11.62 | HO-2 | ||
| HS- | 1.1×10-12 | 11.96 | S2- | ||
| HPO2-4 | 2.2×10-13 | 12.67 | PO3-4 | ||
| H2O | OH- |
根据酸碱质子理论,酸碱在溶液中所表现出来的强度,不仅与酸碱的本性有关,也与溶剂的本性有关。我们所能测定的是酸碱在一定溶剂中表现出来的相对强度。同一种酸或碱,如果溶于不同的溶剂,它们所表现的相对强度就不同。例如HOAc在水中表现为弱酸,但在液氨中表现为强酸,这是因为液氨夺取质子的能力(即碱性)比水要强得多。这种现象进一步说明了酸碱强度的相对性。
三、酸碱反应
酸碱质子理论中的酸碱反应是酸碱之间的质子传递。例如:
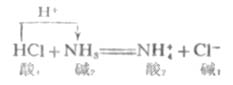
这个反应无论在水溶液中、苯或气相中,它的实质都是一样的。HCL是酸,放出质子给NH3,然后转变成共轭碱CL-,NH3是碱,接受质子后转变成共轭酸NH4+。强碱夺取了强酸放出的质子,转化为较弱的共轭酸和共轭碱。
酸碱质子理论不仅扩大了酸碱的范围,还可以把酸碱离解作用、中和反应、水解反应等,都看作是质子传递的酸碱反应。
由此可见,酸碱质子理论更好地解释了酸碱反应,摆脱了酸碱必须在水中才能发生反应的局限性,解决了一些非水溶剂或气体间的酸碱反应,并把水溶液中进行的某些离子反应系统地归纳为质子传递的酸碱反应,加深了人们对酸碱和酸碱反应的认识。但是酸碱质子理论不能解释那些不交换质子而又具有酸碱性的物质,因此它还存在着一定的局限性。
路易斯提出的酸碱电子理论是目前概括最广的酸碱理论。该理论认为,凡是能给出电子对的物质叫做碱;凡是能接受电子对的物质叫做酸。即酸是电子对的接受体,碱是电子对的给予体。因此,碱中给出电子的原子至少有一对孤对电子(未成键的电子对),而酸中接受电子的原子至少有一个空轨道(外层未填充电子的轨道),以便接受碱给予的电子对,这种由路易斯定义的酸和碱叫做路易斯酸和路易斯碱。例如,三氟化硼(BF3)是路易斯酸,因为BF3中的B原子有一个空轨道是电子的接受体。NH3中N原子有一对孤对电子,是电子对的给予体,为路易斯碱。但是,由于酸碱电子理论概括的酸碱范围太宽,使其实用价值受到一定的限制。
第一节 沉淀-溶解平衡
一、溶度积
电解质的溶解度在每100g水中为0.1g以下的,称为微溶电解质。在一定温度下,当水中的微溶电解质MA溶解并达到饱和状态后,固体和溶解于溶液中的离子之间就达到两相之间的溶解平衡:
![]()
s表示固体,根据化学平衡原理:
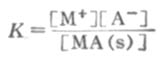
[MA(s)]是常数,可以并入常数项中,得到
[M+][A-]=K[MA(s)]=Ksp (2-8)
式(2-8)表明:在微溶电解质的饱和溶液中,温度一定时,各离子浓度幂之乘积为一常数,称为溶度积常数,简称溶度积。用符号Ksp表示。
对于MmAn型电解质来说,溶度积的公式是
[M]m[A]n= Ksp (2-9)
须注意,式(2-9)中省略了离子的电荷。
表2-7列出了一部分微溶电解质的溶度积。溶度积的大小取决于微溶电解质的本性,它随温度的升高而升稍微增大。
表2-7 一些微溶电解质的溶度积(18~25℃)
| 微溶电解质 | Ksp | 微溶电解质 | Ksp |
| AgBr | 5.0×10-13 | Ca3(PO4)2 | 2.0×10-29 |
| AgCL | 1.8×10-10 | Mg(OH)2 | 1.8×10-11 |
| Ag2CrO4 | 1.1×10-12 | Cu(OH)2 | 2.2×10-20 |
| AgI | 8.3×10-17 | CuS | 6.3×10-36 |
| Ag2S | 6.3×10-50 | Fe(OH)2 | 8.0×10-16 |
| Al(OH)3 | 1.3×10-33 | Fe(OH)3 | 4×10-38 |
| BaCO3 BaSO4 |
5.1×10-9 1.1×10-10 |
HgS(红色) | 4×10-53 |
| CaCO3 | 2.8×10-9 | PbS | 8.0×10-28 |
| CaF2 | 2.7×10-11 | CaC2O4 | 4×10-9 |
溶度积和溶解度都可以表示物质的溶解能力,所以它们之间可以互相换算。知道溶解度可以求出溶度积,也可以由溶度积求溶解度。不过由于影响微溶电解质溶解度的因素很多,如同离子效应、盐效应等,所以换算往往是比较复杂的。我们只介绍不考虑这些因素时的简单换算方法。但是要注意不能把它推广应用到任意微溶电解质。
应该指出:溶度积的大小与溶解度有关,它反映了物质的溶解能力。对同类型的微溶电解质,如AgCL,AgBr,AgI,BaSO4,PbSO4,CaCO3,CaC2O4等,在相同温度下,Ksp越大,溶解度就越大;Ksp越小,溶解度就越小。对于不同类型的微溶电解质,不能认为溶度积小的,溶解度都一定小。如Ag2CrO4的溶度积(Ksp=1.1×10-12)比CaCO3的溶度积(Ksp=2.8×10-9)小,但Ag2CrO4的溶解度(6.5×10-5mol·L-1)却比CaCO3的溶解度(5.29×10-5mol·L-1)大.因此,从Ksp大小比较溶解度大小时,只有在同类型的电解质之间才能直接比较,否则要通过计算,下面举例说明溶解度和溶度积之间的换算。
例6 25℃时,AgCL的溶解度是0.00192g·L-1,求它的溶度积.
解: AgCL的相对分子质量为143.3,AgCL饱和溶液的量浓度为:
0.00192/143.3=1.34×10-5(mol·L-1)
根据AgCL在溶液中的离解:
![]()
溶液中应有 [A+]=[CL-]=1.34×10-5 mol·L-1
所以AgCL的Ksp=[A+][CL-]=(1.34×10-5)2=1.80×10-10
例7 25℃时, Ag2CrO4的溶解度是6.50×10-5mol·L-1,求它的溶度积。
解: 根据Ag2CrO4在溶液中的离解:
![]()
溶液中应有
CrO42-]=6.50*10-5=mol.L-1
[Ag+]=2*6.50*10-5=13.0*10-5mol.L-1
所以Ag2CrO4的Ksp=[Ag+]2[CrO42-]=(13.0*10-5)2*6.50*10-5=1.1*1012
例8 18℃时,Mg(OH)2的Ksp=1.8×10-11,求它的溶解度。
解: 设Mg(OH)2的溶解度为x mol·L-1,根据Mg(OH)2在溶液中的离解:
![]()
溶液中应有
[Mg2+]=χmol.L-1[OH-]=2χmol.L-1
Ksp=[Mg2+][OH-]2=χ.(zχ)2=1.8*10-11
χ=1.65*10-4(mol.L-1)
二、影响微溶电解质溶解度的因素
影响微溶电解质溶解度的因素较多,这里只讨论有其它电解质存在时对溶解度的影响。
(一) 同离子效应
在微溶电解质溶液中,加入含有同离子的强电解质时,微溶电解质多相平衡将发生移动。例如,在AgCL的饱和溶液中加入AgNO3,由于Ag+浓度增大,平衡将向生成AgCL沉淀的方向移动,即降低了AgCL的溶解度。这种结果也是同离子效应。反应如下:

(二)盐效应
如果在微溶电解质溶液中,加入不含同离子的强电解质,则微溶电解质的溶解度会增加。例如,AgCL在KNO3溶液中要比在纯水中的溶解度大。这种结果称为盐效应。
严格地讲,溶度积应是电解质离子活度的乘积。以AgCL为例:
Ksp=αAg+.αc1=[Ag+].fAg+.[Cl-].fcl-
由于在单纯的AgCL的溶液中,离子强度极低,fAg+和fCl-均接近于1,所以
Ksp=[Ag+][Cl-]
但是,当溶液中同时存在一定量KNO3时,溶液的离子强度大为增加,fAg+和fCL-都不接近于1,而是比1小。为了保持Ksp不变,[A+]及[CL-]都要相应增大,即AgCL的溶解度有所增大 ,这就是盐效应的结果。
三、沉淀的生成和溶解
在某微溶电解质溶液中,各有关离子浓度幂之乘积称为离子积。对于MmAa微溶电解质来说,溶液中[M]m[A]n称为它的离子积它可以是任意数值,不是常数,因为并未注明是饱和溶液。离子积和溶度积两者的概念是有区别的。①当溶液中[M]m[A]n<Ksp时,是未饱和溶液,如果体系中有固体存在,将继续溶解,直至饱和为止;②当[M]m[A]n = Ksp时,是饱和溶液,达到动态平衡;③当[M]m[A] n>Ksp时,将会有MmAn沉淀析出,直至成为饱和溶液。以上三点称为溶度积规则,它是微溶电解质多相离子平衡移动规律的总结。根据溶度积规则可以控制离子浓度,使沉淀生成或溶解。
(一)沉淀的生成
根据溶度积的规则,在微溶电解质溶液中,如果离子积大于溶度积常数Ksp,就会有沉淀生成。因此,要使溶液析出沉淀或要使沉淀得更完全,就必须创造条件,使其离子积大于溶度积。
例9 AgCL的Ksp=1.80×10-10,将0.001 mol·L-1NaCL和0.001 mol·L-1AgNO3溶液等体积混合,是否有AgCl 沉淀生成.
解: 两溶液等体积混合后, Ag+ 和CL-浓度都减小到原浓度的1/2.
[Ag+]=[CL-]=1/2×0.001=0.005(mol·L-1)
在混合溶液中,则[Ag+][CL-]=(0.005)2=2.5×10-7
因为[Ag+][CL-]>Ksp,所以有AgCl 沉淀生成.
例10 在0.1mol·L-1KCL和0.1 mol·L-1K2CrO4混合溶液中,逐滴加入AgNO3溶液,问AgCL和AgCrO4两种微溶电解质,哪个最先产生沉淀?
解:设混合液中产生AgCL沉淀时,所需[Ag+]为x mol·L-1,而产生Ag2CrO4沉淀时,所需[Ag+]为y mol·L-1;已知AgCL的Ksp=1.80×10-10,Ag2CrO4的Ksp=1.1×10-12.
根据溶度积常数表达式,则
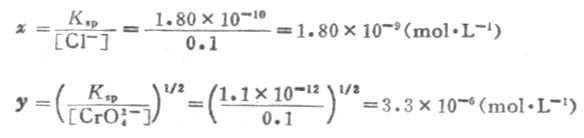
因为x《y ,就是说产生AgCL沉淀时所需Ag+的浓度远小于产生AgCrO4沉淀时所需Ag+的浓度。所以,在混合溶液中,逐滴加入AgNO3溶液时,最先析出AgCL白色沉淀;只有溶液中[Ag+]达到3.3×10-6mol·L-1以上时,才能析出Ag2CrO4砖红色沉淀。
由此可见,溶液中有两种以上都能与同种离子反应产生沉淀的离子时,最先析出的是溶解度较小的化合物,这就是分步沉淀。
例11 BaSO4在水中的溶解度是1.05×10-5 mol·L-1,问在0.01 mol·L-1Na2SO4溶液中BaSO4的溶解度是多少?
解: BaSO4的Ksp=1.1×10-10,BaSO4在溶液中的离解平衡:
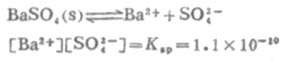
设在0.01 mol·L-1Na2SO4溶液中BaSO4的溶解度为x mol·L-1,则[Ba2+]=x mol·L-1,[SO2-4]=(0.01+x) mol·L-1因为x值远小于0.01,可以忽略不计,则(0.01+x)≈0.01,所以
x×0.01=1.1×10-10
x=1.1×10-8
由此可见,在微溶电解质饱和溶液中,加入含有相同离子的强电解质时,将使微溶电解质的溶解度降低,这就是前面所讲到的同离子效应.所以,加入适当过量的沉淀剂,可以使沉淀更趋完全,达到我们所要求的目的.
(二)沉淀的溶解
根据溶度积原理,沉淀溶解的必要条件是溶液中离子积小于溶度积Ksp因此,创造一定条件,降低溶液中的离子浓度,使离子积小于其溶度积,就可使沉淀溶解.
使沉淀溶解的常用方法主要有三种:
1.加入适当试剂,使其与溶液中某种离子结合生成弱电解质.
大多数微溶氢氧化物都能溶于强酸.例如Fe(OH)3能溶于盐酸.反应如下:
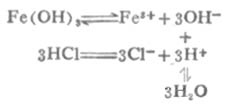
由于溶液中生成了弱电解质H2O,使[OH]-减小,溶液中[Fe3+][OH-]3<Fe(OH)3的Ksp,使平衡向Fe(OH)3溶解的方向移动,即向右移动.若有足量盐酸,沉淀可以完全溶解.
少数微溶氢氧化物能溶于铵盐.例如Mg(OH)2溶于铵盐的反应如下:
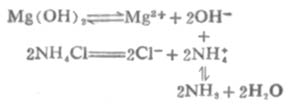
由于溶液中生成了弱电解质NH3和H2O,使[OH-]减小,溶液中[Mg2+][OH-]2<Mg(OH)2的Ksp,使平衡向Mg(OH)2溶解的方向移动。若有足量铵盐,沉淀可以完全溶解。
大多数微溶弱酸盐都能溶于强酸,例如CaCO3能溶于盐酸。反应如下:
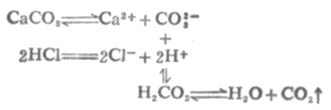
由于溶液中生成了弱电解质H2CO3,H2CO3不稳定,分解成H2O和CO2,CO2从溶液中逸出,使[CO2-3]减小。所以溶液中[Ca2+][CO2-3]<CaCO3的Ksp,平衡向CaCO3溶解的方向移动。若有足量盐酸,沉淀可以完全溶解。
2.加入适当氧化剂或还原剂,与溶液中某种离子发生氧化-还原反应。 例如,在CuS沉淀中加入稀HNO3,因为S2-被氧化成单质硫,从而使溶液中[S2-]减小,所以溶液中[Cu2+][S2-]<CuS的Ksp,使CuS沉淀逐步溶解。反应如下:
3CuS+8HNO3=3Cu(NOa)2+2NO↑+4H2O+3S↓
3.加入适当试剂,与溶液中某种离子结合生成配合物。
例如,AgCL沉淀能溶于氨水。反应如下:
由于生成了稳定的[Ag(NH3)2]+,大大降低了Ag+的浓度,所以AgCL沉淀溶解。
应当指出,在含有沉淀的溶液中,加入适当试剂与溶液中某种离子结合生成更难溶解于水的物质,这叫做沉淀转化。例如,在PbCL2沉淀中,加入Na2CO3溶液后,又生成了一种新的沉淀PbCO3。反应如下:
![]()
由于反应生成了更难溶解的PbCO3沉淀,降低了溶液中[Pb2+],使平衡向生成PbCO3沉淀的方向移动,所以PbCL2沉淀溶解。
由此可见,在有微溶电解质固体存在的溶液中,只要有关离子积小于Ksp,这种微溶电解质就能溶解。因此,在实际工作中,常在有微溶电解质固体存在的溶液中加入某种物质,如能与微溶电解质的离子反应,生成弱电解质、配合物、更难溶解垢物质或可以发生氧化还原反应,从而破坏了沉淀与离子间的平衡,可以促进微溶电解质的溶解或转化。
第三章 PH值与缓冲溶液
溶液中进行的化学反应,特别是生物体内的化学反应,往往需要在一定的PH值条件下才能正常进行。人的各种体液都有一定的PH值,而且不容易改变,因此能保证人体正常的生理活动。人的体液之所以具有一定的PH值,是由于它本身就是缓冲溶液,具有抵抗外来少量强酸或强碱的能力,从而能够稳定溶液的PH值。学习本章的目的有三个:一是掌握PH值及其与溶液酸碱性的关系、酸碱指示剂理论;二是掌握配制缓冲溶液所需要的知识和方法;三是为后续课程学习有关体内酸碱平衡理论提供必要的基础知识。
第一节 水的离子积和溶液的PH值
一、水的离子积
水是一种既能释放质子也能接受质子的两性物质。水在一定程度上也微弱地离解,质子从一个水分子转移给另一个水分子,形成H3O+和OH-。
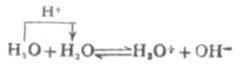
达到平衡时,可得水的离解常数Ki
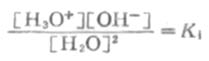
或[H2O+][OH-]=K1[H2O]2
由于水的离解度极小,[HO]数值可以看作是一个常数,令K1[H2O]2等于另一新常数Kw,则
[H3O+][OH-]=Kw
Kw称为水的离子积常数,简称水的离子积。上式表示在一定温度时,水中氢离子浓度与氢氧离子浓度的乘积为一常数(表3-1)。25℃时,由实验测出在纯水中[H3O+]和[OH-]各为1.0×10--7mol·L-1。通常将水合离子H3O+简写为H+,这样,在常温时:
表3-1 不同湿度时水的离子积
| 温度/℃ | KW | I温度/℃ | KW |
| 1.2×10-15 | 50 | 5.5×10-14 | |
| 10 | 3.0×10-15 | 60 | 9.6×10-14 |
| 20 | 6.8×10-15 | 70 | 1.6×10-18 |
| 25 | 1.0×10-14 | 80 | 2.5×10-13 |
| 30 | 1.5×10-14 | 90 | 3.8×10-13 |
| 40 | 2.9×10-14 | 100 | 5.5×10-13 |
K=1.0*10-7*1.0*10-7=1.0*1014
[H+][OH-]=1.0*10-14(3-2)
由于水离解时要吸收大量的热,所以温度升高,水的离解度和KW也相应地增大。
水的离子积原理不仅适用于纯水,也适用于一切稀的水溶液。在任何稀的水溶液中,不论[H+]和[OH-]怎样改变,它们的乘积总是等于KW。
二、溶液的PH值
在纯水或中性溶液中,25℃时
![]()
当向水中加入酸时,溶液中[H+]就会增大,设达到新的平衡时该溶液的[H+]为1.0×10-2mol·L-1,因[H+][OH-]=1.0×10-14,则
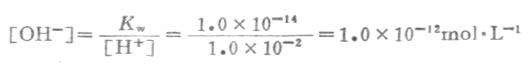
可见,在酸性溶液中,[H+]>1.0×10-7 mol·L-1,而[OH-]<1.0×10-7 mol·L-1.
如果向纯水中加入碱时,溶液中[OH-]就会增大,设达到新的平衡时该溶液的[OH-]为1.0×10-2mol·L-1,同理计算出[H+]=1.0×10-12 mol·L-1。可见,在碱性溶液中[OH-]>1.0×10-7mol·L-1,而[H+]<1.0×10-7 mol·L-1。由上述三种情况可知:
在纯水或中性溶液中 [H+]=1.0×10-7 mol·L-1=[OH-]
在酸性溶液中[H+]>1.0×10-7mol·L-1>[OH-]
在碱性溶液中[H+]<1.0×10-7mol·L-1<[OH-]
当然,[H+]或[OH-]都可用来表示溶液中的中性、酸性或碱性,但实际应用中多采用[H+]来表示。但是,在生物学与医学上许多重要溶液的[H+]往往是一个很小的数值,而且带有负指数,用[H+]表示溶液的酸碱性不方便。例如,人的血液[H+]为0.0000000398mol·L-1,即3.98×10-8 mol·L-1,血液究竟是酸性还是碱性,不容易看清楚。索仑生(Sorensen)首先提出用PH值表示水溶液的酸碱性。
溶液的PH值是氢离子浓度的负对数值。
它的数学表示式为:pH=-lg[H+]
即 [H+]=10-pH(3-3)严格地说,考虑活度时:
Pα+=lgαH+ (3-4)
必须注意,PH值每相差一个单位时,其[H+]相差10倍;PH值相差二个单位时,[H+]相差100倍;依此类推。
用PH值表示稀的水溶液的酸碱性,则有“
在纯水或中性溶液中, [H+]=1.0×10-7 mol·L-1 PH=7
在酸性溶液中, [H+]>1.0×10-7mol·L-1 PH<7 ,PH越小,则酸性越强。
在碱性溶液中, [H+]<1.0×10-7 mol·L-1 PH>7,PH越大,则碱性越强。
和PH相仿,[OH-]和KW也可用它们的负对数来表示,即
pOH=-lg[OH-] (3-5)
pKw=-lgKw(3-6)
由于在25℃时,[H+][OH-]=KW=1.0×10-14
将方程两边取负对数,则得
-lg[H+]-lg[OH-]=-lgKw=-lg1.0*10-14
所以
pH+pOH=pKw=14 (3-7)
水溶液中[H+],[OH-],PH,POH值与溶液酸碱性的关系如表3-2。
表3-2 [H+],[OH-],PH,POH值与溶液酸碱性的关系
| [H+] | 100 | 10-1 | 10-2 | 10-3 | 10-4 | 10-5 | 10-6 | 10-7 | 10-8 | 10-9 | 10-10 | 10-11 | 10-12 | 10-13 | 10-14 |
| PH | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | |
| 的酸碱性 | 中酸性逐渐增强性 碱性逐渐增强 | ||||||||||||||
| POH | 14 | 13 | 12 | 11 | 10 | 9 | 8 | 7 | 6 | 5 | 4 | 3 | 2 | 1 | |
| [OH-] | 10-14 | 10-13 | 10-12 | 10-11 | 10-10 | 10-9 | 10-8 | 10-7 | 10-6 | 10-5 | 10-4 | 10-3 | 10-2 | 10-1 | 100 |
在实际应用中,PH值一般只限于0-14范围内。当 [H+]或[OH-]大于(即100)时,就不再采用PH值,而仍用[H+]或[OH-]表示溶液的酸碱性。
必须注意,用PH值表示的是溶液的酸度或有效酸度而不是酸的浓度。酸度或有效酸度是指溶液中H+浓度,严格地说是指H+的活度,是指已离解部分酸的浓度。酸的浓度也称总酸度或分析浓度,它是指在1升溶液中所含酸的物质的量,包括已离解和未离解两部分酸的总浓度,其大小要用滴定分析来确定。酸度或有效酸度则用PH试纸或PH计来测定。潜在酸度是指未离解部分的浓度,即总酸度与有效酸度之差。例如,0.01mol·L-1HCL和0.01 mol·L-1HOAc的浓度相同,但有效酸度不同。0.01 mol·L-1HCL溶液总酸度为0.01mol·L-1,其有效酸度[H+]也是相同数值,25℃时,总酸度为0.01mol·L-1的HOAc溶液,其有效酸度[H+]则仅为4.2×10-4mol·L-1。
例1 分别求出0.1mol.L-1HCl溶液和0.01mol.L-1HOAc溶液的pH值,已知其[H+]分别为0.01mol.L-1和4.2*10-4mol.L-1。
解:HCl溶液的pH=-lg0.01=-lg10-2=2.0
HOAc溶液的pH=-lg(4.2*10-4)
=[0.62+(-4)]
=3.38
例2 已知某溶液的pH=4.60,计算该溶液的氢离子浓度。
解:-lg[H+]=pH=4.60
lg[H+]=4.60=-5+0.40=5.40
查0.4的反数为2.512,故
[H+]=2.512*10-5mol.L-1
三、PH值在医学上的应用
医学上常用PH来表示体液的酸碱性(见表3-3)。PH值在医学上具有很重要的意义,例如,正常人血浆的PH值相当恒定,保持在7.35-7.45之间,如果血液的PH值大于7.5,在临床上就表现出明显的碱中毒.反之,当血液的PH值小于7.3时,则表现出明显的酸中毒。
测定溶液中PH值的方法很多,临床上常用PH试纸测定病人尿液的PH值。更为精确的测定PH值,要使用PH计。
表3-3 人体各种体液的PH值
| 体液 | PH | 体液 | PH |
| 血清 | 7.35~7.45 | 大肠液 | 8.3~8.4 |
| 成人胃液 | 0.9~1.5 | 乳 | 6.6~6.9 |
| 婴儿胃液 | 5.0 | 泪 | 7.4 |
| 唾液 | 6.35~6.85 | 尿 | 4.8~7.5 |
| 胰液 | 7.5~8.0 | 脑脊液 | 7.35~7.45 |
| 小肠液 | 7.6左右 |
第二节 酸碱指示剂
酸碱指示剂是一类在其特定的PH值范围内,随溶液PH值改变而变色的化合物,通常是有机弱酸或有机弱碱。当溶液PH值发生变化时,指示剂可能失去质子由酸色成分变为碱色成分,也可能得到质子由碱色成分变为酸色成分;在转变过程中,由于指示剂本身结构的改变,从而引起溶液颜色的变化。指示剂的酸色成分或碱色成分是一对共轭酸碱。
一、指示剂的变色原理
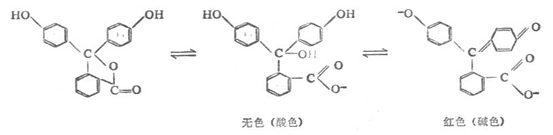
现以弱酸型指示剂(如酚酞)为例,说明酸碱指示剂的变色原理。
弱酸型酸碱指示剂在溶液中存在下列平衡:
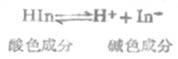
HIn表示弱酸的分子,为酸色成分;In-是弱酸分子离解出H+以后的复杂离子,为碱色成分。酚酞的酸色成分是无色的,碱色的成分则呈红色。根据平衡原理:
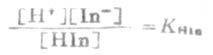
或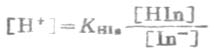
将等式两边各取负对数得:
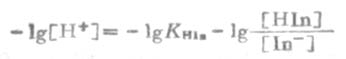
或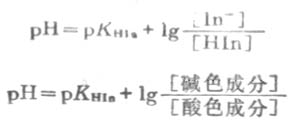 (3-8)
(3-8)
由式(3-8)可知,溶液的颜色决定于碱色成分的浓度比值,而此比值又与PH和PHHin值有关。一定温度下,对指定的某种指示剂,PHHin是一常数。所以碱色成分与酸色成的浓度比值随溶液PH值的改变而变化,溶液的颜色也随之改变。例如,在酚酞指示剂溶液中加入酸时,H+就大量增多,使酚酞的离解平衡向左移动,这时酸色成分增多,碱色成分减少,溶液的颜色以酸色为主,酚酞在酸液中是无色的。反之,如向溶液中加碱时,则平衡向右移动,碱色成分增加,酸色成分减少,溶液的颜色就以碱色为主,酚酞在碱液中是红色的。所以指示剂可用以指示溶液的酸碱性或测定溶液的PH值。
上述弱酸指示剂的变色原理,同样适用于弱碱指示剂。
二、指示剂的变色范围和变色点
由式(3-8)可以看出,当溶液的PH值大于PKHin时,[ In-]将大于[HIn],溶液的颜色将以碱色为主。反之,当溶液的PH值小于PKHin时,[In-]就小于[HIn],溶液的颜色将以酸色为主。通常当[ In-]/[HIn]=10时,即碱色成分的浓度是酸色成分浓度10倍时,溶液将完全呈现碱色成分的颜色,而酸色被遮盖了。这量溶液的PH值为:
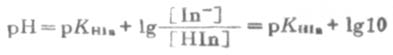
即 pH=pKHIn+1
同理,当[In-]/[HIn]=1/10时,即酸色成分浓度是碱色成分浓度10倍时,溶液的颜色将完全呈现指示剂的酸色。这时溶液的PH值为:
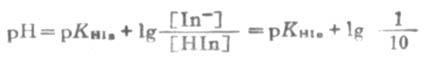
即 pH=pKHIn-1
可见溶液的颜色是在PH=PKHin-1到 PH= PKHin+1的范围内变化的,这个范围称为指示剂的变色范围即变色域。在变色范围内,当溶液的PH值改变时,碱色成分和酸色成分的比值随之改变,指示剂的颜色也发生改变。超出这个范围,如Ph≥PKHin+1时,看到的只是碱色;而在PH ≤PKHin-1时,则看到的只是酸色。因此指示剂的变色范围约2个PH单位。当[In-]/[HIn]=1即PH= PKHin时,称为指示剂的变色点。由于人的视觉对各种颜色的敏感程度不同,加上在变色域内指示剂呈现混合色,两种颜色互相影响观察,所以实际观察结果与理论值有差别,大多数指示剂的变色范围小于2个PH单位。表3-4列出了常用指示剂的变色范围。
表3-4 几种常用的酸碱指示剂
| 酸碱指示剂 | 变色范围 | PKHin | 颜色 | 浓度 | 用量 | |
| 酸色 | 碱色 | (滴/10mL试液) | ||||
| 百里酚蓝(麝香草酚蓝) | 1.2~2.8 | 1.65 | 红 | 黄 | 0.1%的20%酒精溶液 | 1~2 |
| 甲基黄 | 2.9~4.0 | 3.3 | 红 | 黄 | 0.1%的90%酒精溶液 | 1 |
| 甲基橙 | 3.1~4.4 | 3.40 | 红 | 黄 | 0.05%的水溶液 | 1 |
| 溴酚蓝 | 3.0~4.6 | 3.85 | 黄 | 蓝紫 | 0.1%的20%酒精溶液或其钠盐水溶液 | 1 |
| 甲基红 | 4.4~6.2 | 4.95 | 红 | 黄 | 0.1%的60%酒精溶液或其钠盐水溶液 | 1 |
| 溴百里酚蓝(溴麝香草酚蓝) | 6.2~7.6 | 7.1 | 黄 | 蓝 | 0.1%的20%酒精溶液或其钠盐水溶液 | 1 |
| 中性红 | 6.8~8.0 | 7.4 | 红 | 黄 | 0.1%的60%酒精溶液 | 1 |
| 酚红 | 6.7~8.4 | 7.9 | 黄 | 红 | 0.1%的60%酒精溶液或其钠盐水溶液 | 1 |
| 酚酞 | 8.0~10.0 | 9.1 | 无 | 红 | 0.5%的90%酒精溶液 | 1~3 |
| 百里酚酞(麝香草酚酞) | 9.4~10.6 | 10.0 | 无 | 蓝 | 0.1%的90%酒精溶液 | 1~2 |
在测定溶液的PH值时,也常用混合指示剂,它是把许多范围不同的指示剂混合起来,使其在不同的PH值范围内显示不同的颜色。一种可以测定PH4-10范围内溶液酸度的混合指示剂的配方是:百里酚蓝0.01g,溴百里酚蓝1.20g,甲基红0.32g,酚酞1.20g.配制时,可将上述指示剂按配方称取,然后研匀,用200mL95%酒精润湿并溶解,加蒸馏水150mL稀释,用0.1mol·L-1的NaOH溶液中和至溶液显绿色,再加水至400mL。其PH值为8.1。它在不同酸度的溶液中显出不同的颜色。例如:
PH: 4 5 6 7 8 9 10
颜色: 红 橙 黄 绿 青 蓝 紫
为了使用方便起见,也可用混合指示剂溶液将试纸润湿,凉干制成PH试纸供测试之用。
第三节 盐类溶液的PH值
除强酸强碱盐无水解反应外,根据酸碱质子理论,其它各种盐的水解反应,实质由是一种质子转移反应,即酸碱反应。在纯水中,[H+]和[OH-]相等,呈中性。但加入盐的离子和H+及OH-作用后使水中H+或OH-浓度发生改变,故多数盐的溶液显示出酸性或碱性。这种盐的离子与水中H+或OH-作用生成难离解物质,使水中的[H+]或[OH-]发生改变的反应称为盐的水解。由于生成盐和碱强弱不同,水解后酸碱性也有所不同。
一、强碱弱酸盐溶液的PH值
一元强碱弱酸盐溶液,例如 NaOAc 溶液中:
NaOAc→Na++OAc-
Na+不与水电离出的OH-结合,它与溶液的酸碱性无关。OAc-是HOAc的共轭碱,与水作用放出OH-使溶液显碱性。
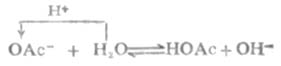
上式的平衡常数,也就是弱碱的离解常数:
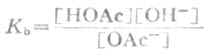
表3-5 一些一元弱碱的离解常数(18-25℃)
| 碱 | 分子式或离子 | Kb | PkB | |
| 碱的强度增 | 二甲胺 | (CH3)2NH | 1.18×10-3 | 2.93 |
| 乙胺 | C2H5NH2 | 4.7×10-4 | 3.33 | |
| 氨 | NH3 | 1.76×10-5 | 4.75 | |
| 硼酸根离子 | H2BO-3 | 1.37×10-5 | 4.86 | |
| 次氯酸根离子 | CLO- | 3.38×10-7 | 6.47 | |
| 吡啶 | C5H5N | 1.61×10-9 | 8.79 | |
| 醋酸根离子 | OAc- | 5.68×10-10 | 9.25 | |
| 苯胺 | C6H5NH2 | 4.0×10-10 | 9.40 | |
| 氟离子 | F- | 2.83×10-11 | 10.55 | |
表3-5 列出了一些一元弱碱的离解常数。通过Kb和碱的浓度c(OAc-的浓度近似地等于盐NaOAc的浓度),即可根据(式2-4)计算溶液中[OH-]及PH值,而不必像经典理论那样通过盐的水解来解释和计算。
![]()
使用这个公式的条件是c/Kb≥500。
例3计算0.100mol.L-1naOAc溶液的 pH值。
![]()
pOH=-lg[OH-]=-lg7.54*10-6=5.12
pH=14-pOH=14-5.12=8.88
多元弱酸的强碱盐溶液PH值的计算,与一元强碱弱酸盐相类似。因 Kb1》Kb2,溶液中[OH-]主要由第一级碱式离解所产生,而第二级碱式离解产生的OH-及弱酸很少,可以忽略。计算时以Kb1代入式(2-4)中之Kb,即可算出[OH-]。例如Na2CO3溶液中
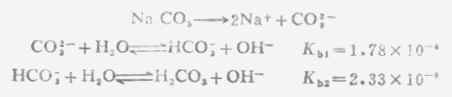
设Na2CO3的浓度为0.100mol·L-,c/Kb1=0.100/1.78×10-4>500,用式(2-4)计算
![]()
pOH=2.37
pH=14-2.37=11.63
二、强酸弱碱盐溶液的PH值
一元强酸弱碱盐,例如NH4CL溶液中:
![]()
NH4+离子是NH3的共轭酸,它在水中电离:
或简写为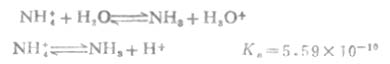
CL-离子不与水电离出的H+结合,它与溶液的酸碱性无关。可认为NH4+就是酸,与水作用放出H+而使溶液显酸性。当c/Ka≥500时,可用式(2-3)计算。
![]()
式中,c为浓盐酸的浓度。PH值可由[H+]计算。
多元强酸弱碱盐例如(NH4)2SO4溶液中PH值的计算,与一元强酸弱碱盐的PH值计算类似。
三、两性物质溶液的PH值
(一)多元酸酸式盐溶液的PH值
多元酸酸式盐中的酸式酸根离子,例如HCO-3在水溶液中的质子转移平衡如下:
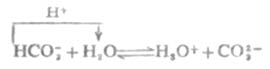
HCO-3作为酸,根据数学推导,当Ka2C>20KW,且c>20Ka1时,水的离解可以忽略,且两性物质浓度不是很稀时,HCO-3溶液中[H+]的近似计算式为
![]() (3-9)
(3-9)
式中Ka1和Ka2分别是碳酸的一级和二级离解常数。
对于其他酸式根离子水溶液和PH值,也可以类推得到近似公式。例如对于H2PO4溶液:
![]()
对于HPO2-4溶液
![]()
从这些近似公式可以看到,这些盐溶液的PH值与浓度无关。
例4 计算0.10mol.L-1NaHCO3溶液的pH值。已知H2CO3的Ka1=4.30*10-7,Ka1=5.61*10-11。
解:由符合近似条件,故可用近似公式计算。
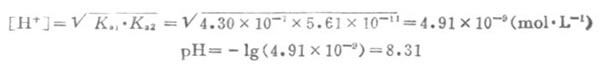
(二)、弱酸弱碱盐溶液的PH值
NH4OAc是两性物质。在溶液中,
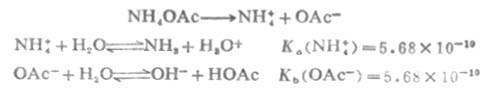
根据数学推导,当cKa(NH4+)>20Kw,且c〈20Ka(HOAc)时,计算溶液[H+]的近似公式为:
![]()
(3-10)
设NH4OAc浓度为0.100mol.L-1,则
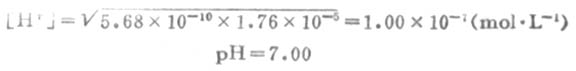
第二节 缓冲溶液
一、缓冲溶液与缓冲作用原理
(一)缓冲作用与缓冲溶液
纯水在25℃时PH值为7.0,但只要与空气接触一段时间,因为吸收二氧化碳而使PH值降到5.5左右。1滴浓盐酸(约12.4mol·L-1)加入1升纯水中,可使[H+]增加5000倍左右(由1.0×10-7增至5×10-4mol·L-1),若将1滴氢氧化钠溶液(12.4mol·L-1)加到1升纯水中,PH变化也有3个单位。可见纯水的PH值因加入少量的强酸或强碱而发生很大变化。然而,1滴浓盐酸加入到1升HOAc-NaOAc混合溶液或NaH2PO4-Na2HPO4混合溶液中,[H+]的增加不到百分之一(从1.00×10-7增至1.01×10-7mol·L-1),PH值没有明显变化.这种能对抗外来少量强酸/强碱或稍加稀释不引起溶液PH值发生明显变化的作用叫做缓冲作用;具有缓冲作用的溶液,叫做缓冲溶液。
(二)缓冲溶液的组成
缓冲溶液由足够浓度的共轭酸碱对组成。其中,能对抗外来强碱的称为共轭酸,能对抗外来强酸的称为共轭碱,这一对共轭酸碱通常称为缓冲对、缓冲剂或缓冲系,常见的缓冲对主要有三种类型。
1.弱酸及其对应的盐 例如,HOAc-NaOAc(实际上是OAc-);H2CO3-NaHCO3;H2C8H4O4-KHC8H4O4(邻苯二甲酸-邻苯二甲酸氢钾);H3BO3-Na2B4O7(四硼酸钠水解后产生H2BO-3)。
2.多元弱酸的酸式盐及其对应的次级盐,例如,NaHCO3-Na2CO3;NaH2PO4-Na2HPO4;NaH2C5HO7(柠檬酸二氢钠)-Na2HC6H5O7;KHC8H4O4-K2C8H4O4。
3.弱碱及其对应的盐 例如NH3-NH+4CL-;RNH2-RNH+3A-(伯胺及其盐);Tris-TrisH+A-(三羟甲基烷及其盐)。
(三)缓冲溶液的作用原理
现以HOAc-NaOAc缓冲溶液为例,说明缓冲溶液之所以能抵抗少量强酸或强碱使PH稳定的原理。醋酸是弱酸,在溶液中的离解度很小,溶液中主要以HOAc分子形式存在,OAc-的浓度很低。醋酸钠是强电解质,在溶液中全部离解成Na+和OAc-,由于同离子效应,加入NaOAc后使HOAc离解平衡向左移动,使HOAc的离解度减小,[HOAc]增大。所以,在HOAc-NaOAc混合溶液中,存在着大量的HOAc和OAc-。其中HOAc主要来自共轭酸HOAc,OAc-主要来自NaOAc。这个溶液有一定的[H+],即有一定的PH值。
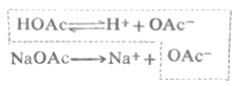
在HOAc-NaOAc缓冲溶液中,存在着如下的化学平衡:
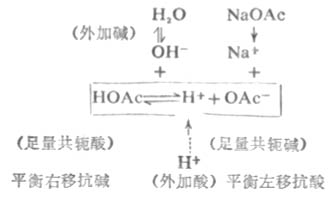
在缓冲溶液中加入少量强酸(如HCL),则增加了溶液的[H+]。假设不发生其他反应,溶液的PH值应该减小。但是由于[H+]增加,抗酸成分即共轭碱OAc-与增加的H+结合成HOAc,破坏了HOAc原有的离解平衡,使平衡左移即向生成共轭碱HOAc分子的方向移动,直至建立新的平衡。因为加入H+较少,溶液中OAc-浓度较大,所以加入的H+绝大部分转变成弱酸HOAc,因此溶液的PH值不发生明显的降低。
在缓冲溶液中加入少量强碱(如NaOH),则增加了溶液中OH-的浓度。假设不发生其他反应,溶液的PH值应该增大。但由于溶液中的H+立即加入的OH-结合成更难离解的H2O,这就破坏了HOAc原有的离解平衡,促使HOAc的离解平衡向右移动,即不断向生成H+和OAc-的方向移动 ,直至加入的OH-绝大部分转变成H2O,建立新的平衡为止。因为加入的OH-少,溶液中抗碱成分即共轭酸HOAc的浓度较大,因此溶液的PH值不发生明显升高。
在溶液稍加稀释时,其中[H+]虽然降低了,但[OAc-]同时降低了,同离子效应减弱,促使HOAc的离解度增加,所产生的H+可维持溶液的PH值不发生明显的变化。所以,溶液具有抗酸、抗碱和抗稀释作用。
多元酸的酸式盐及其对应的次级盐的作用原理与前面讨论的相似。例如,在NaH2PO4-Na2HPO4溶液中存在着离解平衡:
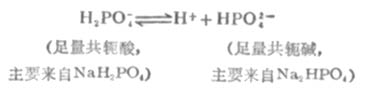
HPO2-4是抗酸成分,通过平衡移能对抗外加酸的影响。H2PO2-4是抗碱成分,通过平衡右移能对抗外加碱的影响。
弱碱及其对应盐的缓冲作用原理,例如,NH3-NH4CL(即NH3-NH+4)溶液中,NH3能对抗外加酸的影响是抗酸成分,NH+4能对抗外加碱的影响是抗碱成分。前者通过下述平衡向右移动而抗酸,后者通过平衡向左移动而抗碱,从而使溶液的PH值稳定。
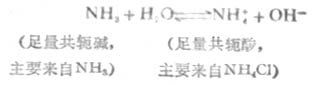
二、缓冲溶液PH的计算
(一)亨德森方程式
在缓冲溶液例如HOAc-NaOAc溶液中,有以下的离解平衡:
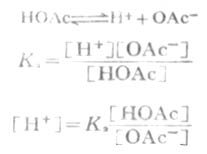
等式两边各取负对数,则
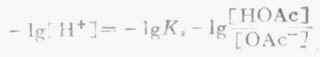
即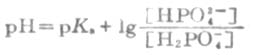
HOAc的离解度比较小,由于溶液中大量的OAc-对HOAc所产生的同离子效应,使HOAc的离解度变得更小。因此上式中的[HOAc]可以看作等于HOAc的总浓度[共轭酸](即缓冲溶液中共轭酸的浓度)。同时,在溶液中NaOAc全部离解,可以认为溶液中[OAc-]等于NaOAc的总浓度[共轭碱](即配制的缓冲溶液中共轭碱的浓度)。将[共轭酸]和[共轭碱]代入上式,则得
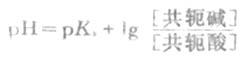 (3-11)
(3-11)
上式称为亨德森-哈塞尔巴赫方程式,简称为亨德森(Henderson)方程式。它表明缓冲溶液的
PH值决定于共轭酸的离解常数Ka和组成缓冲溶液的共轭碱与共轭酸浓度的比值。对于一定的共轭酸,PKa为定值,所以缓冲溶液的PH就决定于两者浓度的比值即缓冲比。当缓冲溶液加水稀释时,由于共轭碱和共轭酸的浓度受到同等程度的稀释,缓冲比是不变的;在一定的稀释度范围内,缓冲溶液的PH值实际上也几乎不变。
式(3-11)中的浓度项指的是混合溶液中共轭酸碱的浓度,而不是混合前的浓度.若混合前共轭酸的量浓度是c酸,体积是V酸,共轭碱的量浓度是c碱,体积是V碱,则式(3-11)可改写成:
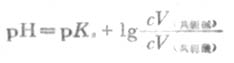 (3-12)
(3-12)
若两种溶液的量浓度相等,则
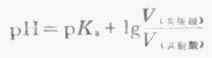 (3-13)
(3-13)
若是等体积的两溶液相混合,则
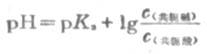 (3-14)
(3-14)
以上几种形式都称为亨德森方程式,可用以计算各种组成类型缓冲溶液的PH近似值。当用于弱酸及其对应的盐组成的缓冲溶液的PH值时,PKa即弱酸的离解常数负对数(见书后附表),[共轭碱]即[弱酸盐]。当用于多元弱酸的酸式盐及其对应的次级盐组成缓冲溶液的PH值时,共轭酸即酸式盐,pKa即该酸式盐负离子的离解常数的负对数,共轭碱即该酸式盐的次级盐。例如,NaHCO3-Na2CO3缓冲溶液的PH值:
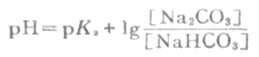 (3-15)
(3-15)
式中PKa即H2CO3的PKa2。
同样,NaH2PO4-Na2HPO4缓冲溶液的PH值:
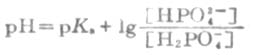 (3-16)
(3-16)
式中PKa为H3PO4的PKa2。
弱碱和它的共轭酸缓冲溶液的PH值也可根据式(3-11)计算。
(二)缓冲溶液PH值计算举例
例5 0.1mol.L-1的HOAc500mL与0.2mol.L-1的NaOAc250mL配成缓冲溶液,计算溶液的pH值。
解:把所给条件代入式(3-11),由书后附表查得HOAc的pKa=4.75,则得:
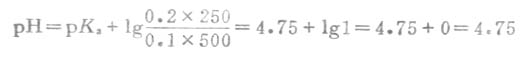
例6 将0.3mol.L-1HOAc溶液10mL与0.1mol.L-1NaOH溶液10mL混合后制成缓冲溶液,试计算这个溶液的pH值(2.5℃时,HOAc时pKa=4.75)。
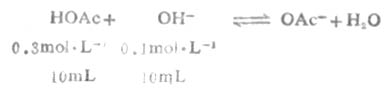
从反应看出HOAc有1/3被OH-中和,生成OAc-和H2O,溶液的总体积为20mL。
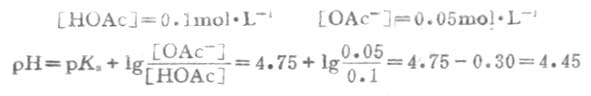
例7 H2PO2-4已知的pKa=7.21,求浓度为0.100mol.L-1、pH7.40的磷酸盐缓冲溶液的缓冲比以及共轭碱HPO2-4和共轭酸H2PO2-4的浓度。
解:设[H2PO2-4]为χmol.L-1,因缓冲溶液的总浓度(共轭酸浓度+共轭碱浓度)为已c=0.100mol.L-1,故[H2PO2-4]=(0.100-χ)mol.L-1
根据式(3-11)或式(3-14):
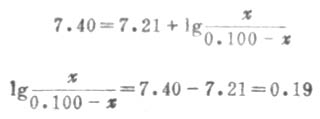
缓冲比为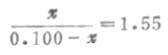
χ=0.061,[HPO2-4]=0.061mol.L-1
0.100-χ=0.100-0.061=0.039,[ H2PO2-4]=0.039mol.L-1
三、缓冲容量与缓冲范围
(一)缓冲容量
缓冲能力的强弱,可用缓冲容量β表示。缓冲容量也叫缓冲值或缓冲指数。
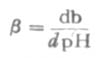
如图3-1所示,对任何一种缓冲溶液的每一个PH值,都有其相应的缓冲量。缓冲容量实际上是一个微分比,可定义为:使1升缓冲溶液的PH值增高很小一个数值dPH时,需加入的强碱物质的量为db,则db与dPH之比值叫缓冲容量,用数学式表示为β=db/dPH缓冲mol·L-1·PH-1。如总浓度(即共轭酸与共轭碱浓度之和)为0.100mol·L-1PH4.45的HOAc-NaOAc缓冲溶液(即醋酸缓冲溶液)的缓冲容量为0.051(mol·L-1·PH-1)。
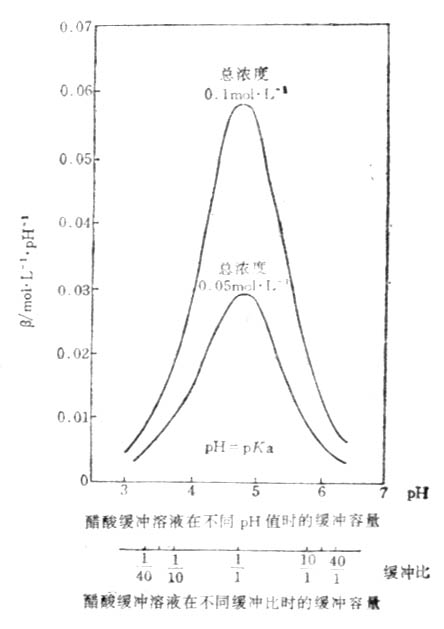
图3-1 醋酸缓冲溶液在不同缓冲比时的缓冲容量
在实际工作中,我们可以通过测量加入强碱的增量Δb(或加入强酸,相对于减少强碱量-Δb),同时测量相应的PH值的增量ΔPH(或加入强酸,PH减小,-ΔPH),从两者比值求得β。因此缓冲容量在数值上等于使1毫升缓冲溶液的PH值改变1个单位时所必须加入的强碱或强酸的物质的量(通常单位用毫摩)。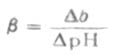 (3-17)
(3-17)
加入碱Δb以后,溶液PH值增大,加入酸以后(相当于减去Δb),溶液PH值减小,所以β总是正值。
(二)影响缓冲容量的因素
缓冲容量的大小与缓冲溶液的缓冲比和总浓度有关。设m和n分别为缓冲比中共轭酸和共轭碱的数值,即[共轭碱]:[共轭酸]=n:m,c总为总浓度,用下式可计算缓冲容量β:
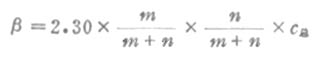
或β=2.30×[共轭酸]×[共轭碱]/ c总(3-18)
从式(3-18)及图3-1可以看出,缓冲溶液的缓冲容量取决于缓冲溶液的总浓度及缓冲比.可得出如下结论:
1.当缓冲溶液的缓冲比一定时,溶液的PH值也一定。缓冲溶液的缓冲容量取决于缓冲溶液的总浓度和缓冲比的比值。
2.当缓冲溶液的PH值一定时,即缓冲比垢比值一定时,缓冲溶液的总浓度越大,则加入少量强酸或强碱所引起缓冲比的比值变化越小,PH改变越小,缓冲容量就越大。图3-1表示两种总浓度都一定的醋酸缓冲溶液的β分别随缓冲比和PH改变的情况。总浓度为0.1mol·L-1和0.05 mol·L-1的醋酸缓冲溶液,当缓冲比为1:1时,PH为4.75,β分别为0.0575和0.0288(mol·L-1·PH-1),总浓度大的溶液缓冲容量较大。从式(3-18)也可见,当缓冲比一定即m和n的数值一定时,β与缓冲溶液的总浓度成正比。总浓度一般在0.05-0.20mol·L-1范围内。
3.当缓冲溶液的总浓度一定时,它的缓冲容量以缓冲比等于1(即[共轭碱]=[共轭酸])时为最大。这时溶液的PH=PKa。当溶液的缓冲比与1偏离愈远,则PH值与PKa的偏差也随着增大,溶液的缓冲容量也随着减小。当溶液的缓冲比大于10/1或小于1/10时,则溶液的缓冲容量极小,一般认为没有缓冲能力。从图3-1看出,对总浓度一定的缓冲溶液来说,当缓冲比愈接近于1:1,缓冲容量愈大;当缓冲比等于1:1,即缓冲溶液的PH值等于PKa时,缓冲容量达极大值(β极大)。当m=n=1,式(3-18)成为
β极大=2.30×1/2×1/2×β极大=0.575β极大 (3-19)
4.由足够浓度的共轭酸碱对组成的溶液,只能在一定的PH值范围内发挥有效的缓冲作用。这个能发挥有效缓冲作用的PH范围,叫缓冲范围。当缓冲比为1/10时,PH=PKa-1;当缓冲比为10/1时,PH=PKa+1。故缓冲范围PH值大致在PKa-1至PKa+1约两个PH单位范围内,即在
PH= PKa±1
的近似范围内,才能表现出缓冲作用。而且同一溶液在不同的PH值时,缓冲容量也不相同。从图3-1,缓冲超出此范围时,β值很小(<0.01),已无缓冲作用。
5.不同缓冲对所组成的缓冲溶液,由于共轭酸的PKa值不同,因此它们的缓冲范围也各不相同(表3-6)。
例8 将0.20mol.L-1NaOH溶液0.15mL加入10mLpH值为4.73的缓冲溶液中,缓站溶液的pH值变为4.78,试求此缓冲溶液的缓冲容量。
解:每毫升缓冲溶液中加入NaOH的毫摩尔数
△b=0.20*0.15/10
△pH=4.78-4.73
表3-6 几种常用缓冲溶液中共轭酸的PKa及缓冲范围
| 缓冲溶液的组成 | 共轭酸的PKa | 缓冲范围 |
| H2C8H4O4(邻苯二甲酸)-NaOH(即H2C8H4O-4-HC8H4O-4) | 2.89(PKa1) | 2.2~4.0 |
| KHC8H4O4( )- NaOH(邻苯二甲酸氢钾)(即HC8C4O-4-C8H4O2-4) | 5.41(PKa2) | 4.0~5.8 |
| HOAc- NaOH(即HOAc-OAc-) | 4.75 | 3.7~5.6 |
| KH2PO4-Na2HPO4 | 7.21(PKa2) | 5.8~8.0 |
| Htris+-Tris[三(羟甲基)氨基甲烷-HCL] | 8.21 | 7.1~8.9 |
| H3BO3- NaOH(即H3BO3-H2BO-3) | 9.14(PKa1) | 8.0~10.0 |
| NaHCO3-Na2CO3(即HCO-3-CO2-3) | 10.25(PKa2) | 9.2~11.0 |
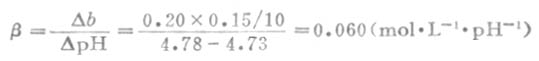
例9 (1)求0.100mol.L-1醋酸缓冲溶液的缓冲容量极大值;(2)已知醋酸的pK=4.75,求0.100mol.L-1pH4.45的醋酸缓冲溶液的缓冲容量。
解:(1)当缓冲溶液的缓冲比为1:1,即m=1和n=1时,缓冲容量达极大值。已知ca=0.100mol.L-1。则由式(3-19)
β极大=0.575c总=0.575*0.100=0.0575(mol.L-1.pH-1)
(2)根据式(3-11),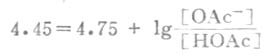

所以 缓冲比[OAc-]/[HOAc]=0.50/1
即 m-1 n=0.5
代入式(3-18)得
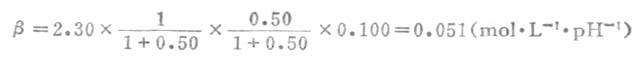
四、缓冲溶液的配制
在配制具有一定PH值的缓冲溶液时,为了使所得溶液具有较好的缓冲能力,应注意以下原则:
1.选择适当的缓冲对,使配制溶液的PH值在所选择的缓冲对的缓冲范围内。这个范围大约在PKa±1之内。例如HOAc-OAc-缓冲对的范围是3.7-5.6,要配制PH从3.7-5.6之间的缓冲溶液可选用这一缓冲对。
2.缓冲对中作为共轭酸的PKa,应尽量接近于配制溶液的PH值。例如,要配制PH为5.3的缓冲溶液时,可以选用HOAc-OAc=或HC8H4O4-C8H4O2-4缓冲对,因为pH5.3恰恰在这两种缓冲对的缓冲范围内。但是,前者的共轭酸的PKa 为4.75;后者共轭酸的PKa 为5.4,所以选用HC8H4O-4-C8H4O2-4配制的缓冲溶液较选用前者有更大的缓冲容量。
3.要有一定的总浓度(通常在0.05-0.20mol·L-1之间)使所配成溶液具有足够的缓冲容量,并采用适当的缓冲比使溶液的pH恰好等于所需要的PH值。
在具体配制时,为了简便起见,常用相同浓度的共轭酸碱溶液。此种情况可用式(3-13)计算所需两种溶液的体积。然后根据体积比,把共轭酸碱两种溶液混合,即得所需的缓冲溶液。设溶液的总体积是V总,则式(3-13)改写成
或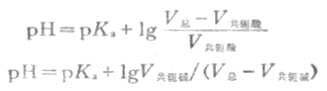
例10 如何配制100mLpH值为5.10的缓冲溶液?
解:根据配制缓冲溶液的原则,可选择HOAc-OAc-缓冲系来配制。因pH=5.10,pKa=4.75,V总=100L,故
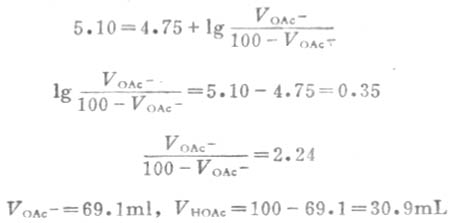
配制缓冲溶液还可采用共轭酸中加氢氧化钠或共轭碱中加盐酸的办法。两种方法都可组成有足够浓度的共轭酸碱对的缓冲溶液。
例11 欲配制pH值为5.10的缓冲溶液,计算在50mL的0.1ml.L-1HOAc溶液中应加0.1mol.L-1NaOH溶液多少mL?
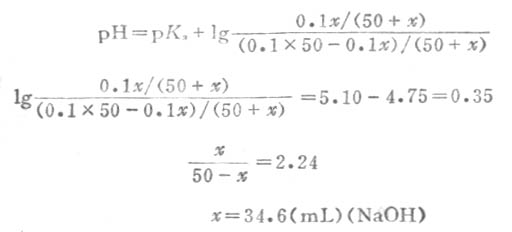
故χ=34.6(mL)(NaOH)
在50mL0.1mol.L-1HOAc溶液中加入34.6mL0.1mol.L-1NaOH溶液即得所需缓冲溶液。
应用亨德森方程式来配制缓冲溶液,没有考虑溶液的离子强度的影响。
一些缓冲溶液的配制法可查阅参考书或附录克拉克缓冲系列及碱性缓冲系列表,其准确度较高,表中的浓度及体积都要求准确。表中稀释值ΔPH1/2表示缓冲溶液用等体积水稀释后Ph 的变化。Tris缓冲系适合生理学和生物化学要求,比较常用。
五、缓冲溶液在医学上的意义
人体内各种体液的PH值具有十分重要的意义。它们均控制在一狭小范围内。因为只有在这范围内,机体的各种功能活动才能正常进行。离开正常范围的少许变化尚能允许,但如变化太大,都可能引起体内许多功能失调。
在体内差不多每项代谢的结果都有酸产生,如有机食物被完全氧化而产生碳酸,嘌呤被氧化而产生尿酸,碳水化合物的厌氧分解而产生乳酸以及因氧化作用不完全而导致乙酰乙酸和в-羟基丁酸的生成等。体内代谢也生成磷酸和硫酸。代谢过程也可以产生NaHCO3。这些代谢产生的酸或碱进入血液并没有引起PH值发生明显的变化,这说明血液具有足够的缓冲作用。也说明体内有着有效的生理作用支配着体内能及时地得到缓冲物的不断补充。
正常人血浆的PH值相当恒定。血液所以具有缓冲作用,是因为血液是一种很好的缓冲溶液。血液中存在下列缓冲系(HA表示有机酸):
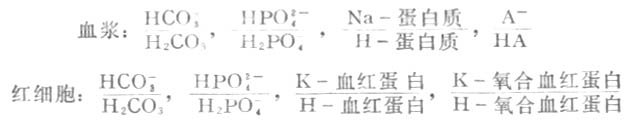
在这些缓冲系中,碳酸氢盐缓冲系(HCO-3/H2CO3)在血液中浓度很高,对维持血液正常PH值的作用很重要。其次红细胞中的血红蛋白和氧合血红蛋白缓冲系也很重要。这些缓冲系中的共轭酸(如H2CO3)起抗碱作用,共轭碱(如HCO-3)起抗酸作用,使PH值保持正常。
由于H2CO3-NaHCO3(或CO2-HCO-3)缓冲系在血浆中存在如下平衡:
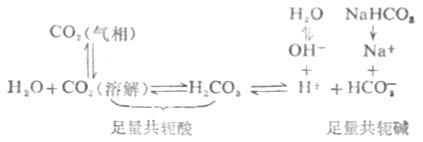
当人体内各组织和细胞在代谢中产生的酸进入血液时,血液中CO2-HCO-3缓冲系的共轭碱HCO-3就和H+反应,并转变为其共轭酸H2CO3及CO2,即上述H2CO3离解平衡向左移动。因碳酸仅轻度离解,所以,等于把加入的H+从溶液中有效地除去,维持PH基本不变。而溶解的CO2转变为气相CO2从肺部呼出。如果代谢产生的碱进入血液,则上述血液中的离解平衡向右移动,从而抑制PH值的升高。而血液中升高的[HCO-3]可通过肾脏功能的调节使其浓度降低。
血液中其他缓冲系的抗酸抗碱作用和CO2-HCO-3缓冲作用的原理相似。而且,当产生CO2过多时,主要是通过血红蛋白和氧合血红蛋白运送到肺部排出,或通过磷酸缓冲系使[CO2]降低。至于降低的[HCO-3]也可以通过肾脏功能的调节使其在血液中的浓度升高,从而使[CO2]、[HCO-3]和[HCO-3]/[CO2](溶解)都恢复正常。肺呼吸快些或慢些可调节CO2的量或酸量(呼吸慢则CO2积蓄);而肾的功能之一是调节血液中HCO-3的浓度及磷酸盐缓冲系的含量。肺和肾脏的协同调节操持[HCO-3]/[CO2](溶解)=20/1,虽然这时缓冲比超出(10/1)-(1/10)范围,可是缓冲容量仍然很大。总之,血液PH值能保持正常范围,是多种缓冲对的缓冲作用以及有效的生理调节作用的结果。
微生物的培养,组织切片和细菌染色,以及研究酶的催化,都需用一定PH值的缓冲溶液。在临床检验中,常把血液中HCO-3的浓度看作“碱储备”,作为一种常规来检查,也需要缓冲作用的知识。理解缓冲作用的基本原理和掌握这方面的基本实验知识,在医学上有重要的意义。
第四章 原子结构和分子结构
第一节 原子结构
自然界的物质种类繁多,性质各异。不同物质在性质上的差异是由于物质内部结构不同而引起的。在化学反应中,原子核不变,起变化的只是核外电子。要了解物质的性质及其变化规律,有必要先了解原子结构,特别是核外电子的运动状态。
一、核外电子运动的特征
我们知道,地球沿着固定轨道围绕太阳运动,地球的卫星(月球或人造卫星)也以固定的轨道绕地球运转。这些宏观物体运动的共同规律是有固定的轨道,人们可以在任何时间内同时准确地测出它们的运动速度和所在位置。电子是一种极微小的粒子,质量为9.1×10-31kg,在核外的运动速度快(接近光速)。因此电子的运动和宏观物体的运动不同。和光一样,电子的运动具有微粒性和波动性的双重性质。对于质量为m,运动速度为v的电子,其动量为:P=mv
其相应的波长为:
λ=h/P=h/mv (4-1)
式(4-1)中,左边是电子的波长λ,它表明电子波动性的特征,右边是电子的动量P(或mv),它表明电子的微粒性特征,两者通过普朗克常数h联系起来。
实验证明,对于具有波动性的微粒来说,不能同时准确地确定它在空间的位置和动量(运动速度)。也就是说电子的位置测得愈准时,它的动量(运动速度)就愈测不准,反之亦然。但是用统计的方法,可以知道电子在原子中某一区域内出现的几率。
图4-1 氢原子五次瞬间照像
图 4-2 若干张氢原子瞬间照片叠印
电子在原子核外空间各区域出现的几率是不同的。在一定时间内,在某些地方电子出现的几率较大。而在另一些地方出现的几率较小。对于氢原子来说,核外只有一个电子。为了在一瞬间找到电子在氢原子核外的确切位置,假定我们用高速照相机先给某个氢原子拍五张照片,得到图4-1所示的五种图象,⊕ 代表原子核,小黑点表示电子。如果给这个氢原子照几万张照片,叠加这些照片(图4-2)进行分析,发现原子核外的一个电子在核外空间各处都有出现的可能,但在各处出现的几率不同。如果用小黑点的疏密来表示电子在核外各处的几率密度(单位体积中出现的几率)大小,黑点密的地方,是电子出现几率密度大的地方;疏的地方,是电子出现几率密度小的地方,如图4-3所示。像这样用小黑点的疏密形象地描述电子在原子核外空间的几率密度分布图象叫做电子云。所以电子云是电子在核外运动具有统计性的一种形象表示法。

图4-3 氢原子的电子云图 4-4氢原子电子云界面图
从图4-3中可见,氢原子的电子云是球形的,离核越近的地方其电子云密度越大。但是由于离原子核越近,球壳的总体积越小,因此在这一区域内黑点的总数并不多。而是在半径为53pm 附近的球壳中电子出现的几率最大,这是氢原子最稳定状态。为了方便,通常用电子云的界面表示原子中电子云的分布情况。所谓界面,是指电子在这个界面内出现的几率很大(95%以上),而在界面外出现的几率很小(5%以下)。
二、核外电子的运动状态
电子在原子中的运动状态,可n,l,m,ms四个量子数来描述。
(一)主量子数n
主量子数n是用来描述原子中电子出现几率最大区域离核的远近,或者说它是决定电子层数的。主量子数的n的取值为1,2,3…等正整数。例如,n=1代表电子离核的平均距离最近的一层,即第一电子层;n=2代表电子离核的平均距离比第一层稍远的一层,即第二电子层。余此类推。可见n愈大电子离核的平均距离愈远。
在光谱学上常用大写拉丁字母K,L,M,N,O,P,Q代表电子层数。
| 主量子数(n) | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| 电子层符号 | K | L | M | N | O | P | Q |
主量子数n是决定电子能量高低的主要因素。对单电子原子来说,n值愈大,电子的能量愈高。但是对多电子原子来说,核外电子的能量除了同主量子数n有关以外还同原子轨道(或电子云)的形状有关。因此,n值愈大,电子的能量愈高这名话,只有在原子轨道(或电子云)的形状相同的条件下,才是正确的。
(二)副量子数l
副量子数又称角量子数。当n给定时,l可取值为0,1,2,3…(n-1)。在每一个主量子数n中,有n个副量子数,其最大值为n-1。例如n=1时,只有一个副量子数,l=0,n=2时,有两个副量子数,l=0,l=1。余此类推。按光谱学上的习惯l还可以用s,p,d,f等符号表示。
| l | 1 | 2 | 3 | |
| 光谱符号 | s | p | d | F |
副量子数l的一个重要物理意义是表示原子轨道(或电子云)的形状。L=0时(称s轨道),其原子轨道(或电子云)呈球形分布(图4-5);l=1时(称p轨道),其原子轨道(或电子云)呈哑铃形分布(图4-6);…
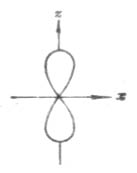
图4-5 s电子云图4-6 p电子
副量子数l的另一个物理意义是表示同一电子层中具有不同状态的亚层。例如,n=3时,l可取值为0,1,2。即在第三层电子层上有三个亚层,分别为s,p,d亚层。为了区别不同电子层上的亚层,在亚层符号前面冠以电子层数。例如,2s是第二电子层上的亚层,3p是第三电子层上的p亚层。表4-1列出了主量子数n,副量子数l及相应电子层、亚层之间的关系。
表4-1 主量子数n,副量子数l及其相应电子层亚层之间的关系
| n | 电子层 | l | 亚层 |
| 1 | 1 | 1s | |
| 2 | 2 | 2s | |
| 1 | 2p | ||
| 3 | 3 | 3s | |
| 1 | 3p | ||
| 2 | 3d | ||
| 4 | 4 | 4s | |
| 1 | 4p | ||
| 2 | 4d | ||
| 3 | 4f |
前已述及,对于单电子体系的氢原子来说,各种状态的电子能量只与n有关。但是对于多电子原子来说,由于原子中各电子之间的相互作用,因而当n相同,l不同时,各种状态的电子能量也不同,l愈大,能量愈高。即同一电子层上的不同亚层其能量不同,这些亚层又称为能级。因此副量子数l的第三个物理意义是:它同多电子原子中电子的能量有关,是决定多电子原子中电子能量的次要因素。
(三)磁量子数m
磁量子数m决定原子轨道(或电子云)在空间的伸展方向。当l给定时,m的取值为从-l到+l之间的一切整数(包括0在内),即0,±1,±2,±3,…±l,共有2l+1个取值。即原子轨道(或电子云)在空间有2l+1个伸展方向。原子轨道(或电子云)在空间的每一个伸展方向称做一个轨道。例如,l=0时,s电子云呈球形对称分布,没有方向性。m只能有一个值,即m=0,说明s亚层只有一个轨道为s轨道。当l=1时,m可有-1,0,+1三个取值,说明p电子云在空间有三种取向,即p亚层中有三个以x,y,z轴为对称轴的px,py,pz轨道。当l=2时,m可有五个取值,即d电子云在空间有五种取向,d亚层中有五个不同伸展方向的d轨道(图4-7)。
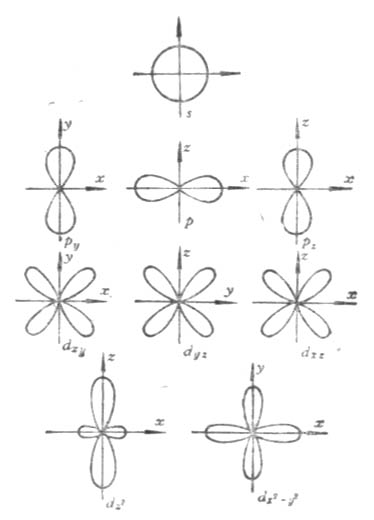
图4-7 s,p,d电子云在空间的分布
n,l相同,m 不同的各轨道具有相同的能量,把能量相同的轨道称为等价轨道。
(四)自旋量子数ms
原子中的电子除绕核作高速运动外,还绕自己的轴作自旋运动。电子的自旋运动用自旋量子数ms表示。ms 的取值有两个,+1/2和-1/2。说明电子的自旋只有两个方向,即顺时针方向和逆时针方向。通常用“↑”和“↓”表示。
综上所述,原子中每个电子的运动状态可以用n,l,m,ms四个量子数来描述。主量子数n决定电子出现几率最大的区域离核的远近(或电子层),并且是决定电子能量的主要因素;副量子数l决定原子轨道(或电子云)的形状,同时也影响电子的能量;磁量子数m决定原子轨道(或电子云)在空间的伸展方向;自旋量子数ms决定电子自旋的方向。因此四个量子数确定之后,电子在核外空间的运动状态也就确定了。
三、核外电子的排布规律
(一)最低能量原理
所谓最低能量原理是,原子核外的电子,总是尽先占有能量最低的原子轨道,只有当能量较低的原子轨道被占满后,电子才依次进入能量较高的轨道,以使原子处于能量最低的稳定状态。
原子轨道能量的高低为:
1.当n相同,l不同时,轨道的能量次序不s<p<d<f。例如,E3S<E3P<E3d。
2.当n不同,l相同时,n愈大,各相应的轨道能量愈高。例如,E2S<E3S<E4S。
3.当n和l都不相同时,轨道能量有交错现象。即(n-1)d轨道能量大于ns轨道的能量,(n-1)f轨道的能量大于np轨道的能量。在同一周期中,各元素随着原子序数递增核外电子的填充次序为ns,(n-2)f,(n-1)d,np。
核外电子填充次序如图4-8所示。
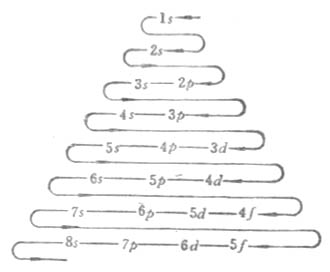
图4-8 电子填充的次序
(二)鲍里(Pauli)不相容原理
鲍里不相容原理的内容是:在同一原子中没有四个量子数完全相同的电子,或者说在同一原子中没有运动状态完全相同的电子。例如,氦原子的1s轨道中有两个电子,描述其中一个原子中没有运动状态的一组量子数(n,l,m,ms)为1,0,0,+1/2,另一个电子的一组量子数必然是1,0,0,-1/2,即两个电子的其他状态相同但自旋方向相反。根据鲍里不相容原理可以得出这样的结论,在每一个原子轨道中,最多只能容纳自旋方向相反的两个电子。于是,不难推算出各电子层最多容纳的电子数为2n2个。例如,n=2时,电子可以处于四个量子数不同组合的8种状态,即n=2时,最多可容纳8个电子,见下表。
| N | 2 | 2 | 2 | 2 | 2 | 2 | 2 | 2 |
| L | 1 | 1 | 1 | 1 | 1 | 1 | ||
| M | +1 | +1 | -1 | -1 | ||||
| ms | +1/2 | -1/2 | +1/2 | -1/2 | +1/2 | -1/2 | +1/2 | -1/2 |
在等价轨道中,电子尽可能分占不同的轨道,且自旋方向相同,这就叫洪特规则。
洪特规则实际上是最低能量原理的补充。因为两个电子同占一个轨道时,电子间的排斥作用会使体系能量升高,只有分占等价轨道,才有利于降低体系的能量。例如,碳原子核外有6个电子,除了有2个电子分布在1s轨道,2个电子分布在2s轨道外,另外2个电子不是占1个2p轨道,而是以自旋相同的方向分占能量相同,但伸展方向不同的两个2p轨道。碳原子核外6个电子的排布情况如下:

作为洪特规则的特例,等价轨道全充满,半充满或全空的状态是比较稳定的。全充满、半充满和全空的结构分别表示如下:
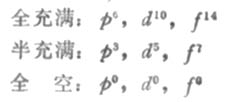
用洪特规则可以解释为什么Cr原子的外层电子排布为3d54s1而不是3d44s2,Cu原子的外层电子排布为3d104s1而不是3d94s2。
应该指出,核外电子排布的原理是从大量事实中概括出来的一般规律,绝大多数原子核外电子的实际排布与这些原理是一致的。但是随着原子序数的增大,核外电子排布变得复杂,用核外电子排布的原理不能满意地解释某些实验的事实。在学习中,我们首先应该尊重事实,不要拿原理去适应事实。也不能因为原理不完善而全盘否定原理。科学的任务是承认矛盾,不断地发展这些原理,使之更加趋于完善。
四、元素的电负性
元素的原子在分子中吸引电子的能力叫元素的电负性。元素的电负性愈大,表示该元素原子吸引电子的能力愈大,生成阴离子的倾向愈大。反之,吸引电子的能力愈小,生成阳离子的倾向愈大。表4-2列出了元素的电负性数值。元素的电负性是相对值,没有单位。通常规定氟的电负性为4.0(或锂为1.0),计算出其他元素的电负性数值。从表4-2可以看出,元素的电负性具有明显的周期性。电负性的周期性变化和元素的金属性、非金属性的周期性变化是一致的。同一周期内从左到右,元素的电负性逐渐增大,同一主族内从上至下电负性减小。在副族中,电负性变化不规则。在所有元素中,氟的电负性(4.0)最大,非金属性最强,钫的电负性(0.7)最小,金属性最强。一般金属元素的电负性小于2.0,非金属元素的电负性大于2.0,但两者之间没有严格的界限,不能把电负性2.0作为划分金属和非金属的绝对标准。
表4-2 元素的电负性
| Li | Be | H | B | C | N | O | F | |||||||||
| 1.0 | 1.5 | 2.1 | 2.0 | 2.5 | 3.0 | 3.5 | 4.0 | |||||||||
| Na | Mg | Al | Si | P | S | Cl | ||||||||||
| 0.9 | 1.2 | 1.5 | 1.8 | 2.1 | 2.5 | 3.0 | ||||||||||
| K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br |
| 0.8 | 1.0 | 1.3 | 1.5 | 1.6 | 1.6 | 1.5 | 1.8 | 1.8 | 1.9 | 1.9 | 1.6 | 1.6 | 1.8 | 2.0 | 2.4 | 2.8 |
| Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I |
| 0.8 | 1.0 | 1.2 | 1.4 | 1.6 | 1.8 | 1.9 | 2.2 | 2.2 | 2.2 | 1.9 | 1.7 | 1.7 | 1.8 | 1.9 | 2.1 | 2.5 |
| Cs | Ba | La~Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At |
| 0.7 | 0.9 | 1.1~1.2 | 1.3 | 1.5 | 1.7 | 1.9 | 2.2 | 2.2 | 2.2 | 2.4 | 1.9 | 1.8 | 1.8 | 1.9 | 2.0 | 2.2 |
| Fr | Ra | Ac | Th | Ha | U | Np~No | ||||||||||
| 0.7 | 0.9 | 1.1 | 1.3 | 1.4 | 1.4 | 1.4~1.3 |
素电负性的大小,不仅能说明元素的金属性和非金属性,而且对讨论化学键的类型,元素的氧化数和分子的极性等都有密切关系。
第二节 分子结构
所谓分子结构通常包括下面一些内容:分子中直接相邻的原子间的强相互作用力,即化学键问题,分子的空间构型问题;分子之间还有一种弱的相互作用力,即分子间力问题;此外分子间或分子内的一些原子间还可能形成氢键。
本节主要简介杂化轨道理论,有关氢键的问题留在下一节讨论。
一、化学键的概念
分子或晶体中相邻原子间强烈的相互作用力称为化学键。化学键的基本类型有:离子键(电价键)、共价键、配价键和金属键等。
以阳离子和阴离子之间静电引力形成的化学键 叫离子 键。
分子中原子间通过共享电子对所形成的化学键为共价键。
配价键是一种特殊的共价键,其共享电子对是一个原子单独提供的。这种由一个原子单独提供一对电子与另一个原子共享所形成的共价键,叫配位共价键,简称配价键。
自1916年刘易斯提出经典的共价键理论以来,共价键理论有了很大的发展。现代共价键理论有两种,一是价键理论,二是分子轨道理论。本书不介绍轨道理论。
(一)价键理论的基本要点
价键理论,又称电子配对法,其基本要点如下:
1.具有自旋相反的未成对电子的两个原子相互接近,可以形成稳定的共价键。
如果A、B两个原子各有一个自旋相反的未成对的电子,那么这两个未成对电子可以相互配对形成稳定的共价键,这对电子为A、B两原子所共有。如果A、B各有两个或三个未成对的电子,则自旋相反的单电子可两两配对形成共价键或叁键。
如果A原子有两个未成对电子,B原子有一个未成对电子,那么一个A原子能与两个B原子结合形成AB2型分子。
2.原子中未成对的电子数等于原子所能形成的共价键数目。
共价键是由成键原子中自旋相反的未成对电子配对形成的。一个原子的一个电子和另一个原子的一个电子配对以后,不能再和第二个电子配对。因为这时其中必有两个电子的自旋方向相同而相斥。也就是说一个原子所能形成共价键的数目是一定的。原子中未成对的电子数等于原子所能形成的共价键数目,这就是共键价的饱和性。例如,H原子只有一个未成对电子,它和另一个H原子的未成对电子配对后,就不能再与第二个H原子的电子配对了。
3.成键电子的电子云重叠越多,核间电子子云密度越大,形成的共价键越牢固。
共价键的生成是由于自旋相反的单电子相互配对,电子云重叠的结果。因此,当两个原子形成分子时,电子云重叠的程度越大,则两原子间的电子云密度越大,生成的共价键越牢固,所以,在形成共价键时,电子云总是尽可能达到晨大程度的重叠,这叫电子云最大重叠原理。
根据电子云最大重叠原理,在形成共价键时,原子间总是尽可能沿着电子云最大重叠方向成键。s电子云呈球形对称分布,p、d、f电子云在空间都有一定的伸展方向。在形成共价键时,除了s电子云和s电子云可以在任何方向上都能达到最大程度的重叠外,p、d电子云的重叠,只有在一定方向上才能使电子云有最大程度的重叠。即共价键是有方向性的。例如,当氢原子1s电子云和氯原子的3p电子云重叠形成HCL分子时,氢原子的1s电子云总是沿着氯原子未成对电子的3p电子云对称轴方向作最大程度的重叠(图4-9(a))。其他方向都不能形成稳定的分子(图4-9(b)(c))。
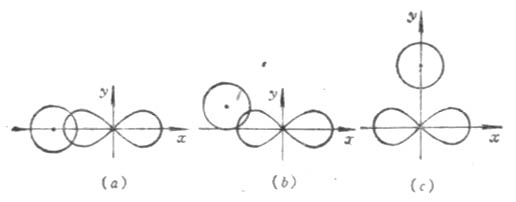
图4-9 氢原子的1s电子云与氧原子的3Pχ电子云的三种重叠情况
(二)共价键的类型
共价键有两种成键方式。一种是电子云以:“头碰头”方式相重叠,电子云及重叠部分沿键轴(两核间连线)呈圆柱形对称分布,重叠部分绕轴旋转任何角度形状不会改变,这种键叫σ键。另一种是成键的两个电子云的对称轴相平行,以“肩并肩”方式相重叠,电子云重叠部分对通过键轴的一个平面具有对称性,这种键称为π键。
例如在N2分子中,氮原子的电子层结构为1s22s22p1x2p1y2p1z三个未成对的p电子分占三个互相垂直的p轨道。当两个氮原子结合成N2分子时,px电子云沿x轴方向以“头碰头”方式重叠形成一个σ键,每个原子剩下的两个p电子云不能再沿x轴方向“头碰头”重叠,只能让p电子云的对称轴平行,以“肩并肩”方式重叠形成两个π键。如图4-10。
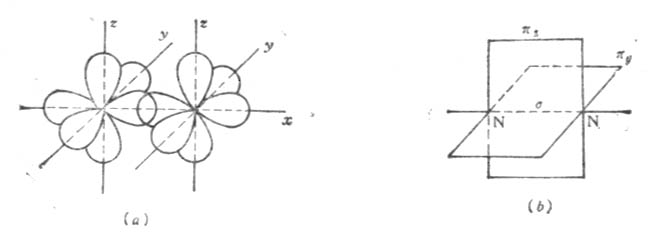
图4-10 N2分子形成示意图
由于σ键电子云重叠程度较π键大,因而σ键比π键牢固。一般来说,π键容易断开,化学活泼性较强。π键不能单独存在,只能与σ键共存于具有双键或叁键的分子中。σ键不易断开,是构成分子的骨架,可单独存在于两原子间。通常在以共价键结合的两原子间只能有一个σ键。
二、杂化轨道理论
价键理论比较简明地阐明了共价键的本质,共价键的饱和性和方向性。但在解释分子的空间结构方面却遇到了困难。例如,经实验测知,甲烷分子具有正四面体的空间构型,如图4-11所示。图中实线代表C-H键,虚线表示CH4分子具有正四面体的空间构型。碳原子位于四面体的中心,与四个氢原子形成四个等同的C-H键,指向四面体的顶点,两个C-H键间夹角(<HCH)为109°28’。
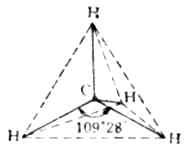
图4-11 CH4分子构型
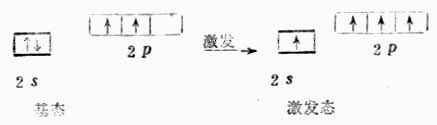
碳原子的外层电子构型是2s22p1x2p1y有两个未成对的p电子,按照价键理论,碳只能与两个氢原子形成两个共价键。如果考虑将碳原子的一个2s电子激发到2p空轨道上去,则碳原子有四个未成对电子(一个s电子和三个p电子),可与四个氢原子的1s电子配对形成四个C-H键。从能量观点上看,2s电子激发到2p轨道所需要的能量(402kJ·mol-1)可能被多形成两个C-H键所放出的能量(410KJ.mol-1)所补偿而余。由于碳原子的2s电子和2p电子的能量不同,形成的四个C-H键也应当不同,这与实验事实不符。为了解决这个矛盾,1931年鲍林(Pauling)和斯莱脱(Slater)提出了杂化轨道理论,进一步发展和丰富了现代价键理论。
(一)杂化轨道理论的基本要要点
1.在成键过程中,由于原子间的相互影响,同一原子中参加成键的几个能量相近的原子轨道可以进行混合,重新分配能量和空间方向,组成数目相等的新原子轨道。这种轨道重新组合的过程称为轨道杂化,简称杂化。所组成的新原子轨道叫做杂化轨道。
2.杂化轨道之间互相排斥,力图在空间取得最大的键角,使体系能量降低。原子轨道杂化以后所形成的杂化轨道更有利于成键。因为杂化后原子轨道的开头发生了变化,如s轨道和p轨道杂化形成的杂化轨道,使本来平分在对称两个方向上的p轨道比较集中在一个方向上,变成一头大一头小,成键时在较大一头重叠,有利于最大重叠。因此杂化轨道的成键能力比单纯轨道的成键能力强。
(二)杂化轨道类型
根据原子轨道的种类和数目不同,可以组成不同类型的杂化轨道。这里我们只介绍s轨道和p轨道之间的杂化。
1.Sp杂化
一个s轨道和一个p轨道杂化可组成两个sp杂化轨道。每个sp杂化轨道各含有1/2s和1/2p成分。两个杂化轨道夹角为180°。
两个sp杂化轨道的对称轴在同一条直线上,只是方向相反(图4-12)。因此sp杂化轨道又叫直线形杂化轨道。
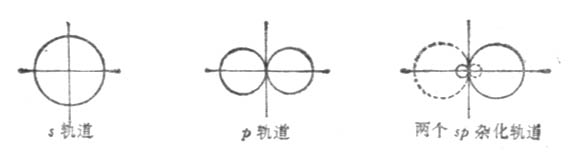
图 4-12 sp杂化轨道的形成
气态BeCL2是直线形分子,铍原子的电子层结构为1s22s2,似乎不会形成共价键。但实际上铍可与氯气反应生成BeCL2共价分子。根据杂化轨道理论,铍原子成键时,2s轨道上的一个电子先被激发到一个空的2p轨道上去,然后由含有一个未成对电子的2s轨道和2p轨道进行sp杂化形成能量相等夹角为180°的两个sp杂化轨道。两个杂化轨道再分别与两个氯原子的3p轨道重叠,形成两个互为180°的Be-Cl键,它们是(sp-p)σ键。因此BeCL2是直线形分子(图4-13)。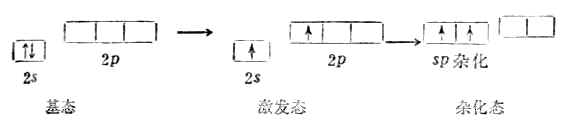
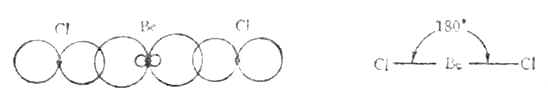
图4-13 BeCL2分子型
2.sp2杂化
一个s轨道和两个p轨道杂化可组成三个sp2杂化轨道。每个sp2杂化轨道有1/3s成分,2/3p成分。两个sp2杂化轨道间的夹角120°。
三个sp2杂化轨道的取向是指向平面三角形的三个顶角,因此sp2杂化轨道又叫平面三角形杂化轨道(图4-14)。

图4-14 三个sp2杂化轨道
BF3是平面三角形分子。硼原子的价电子结构为2s22p1。当硼与氟反应时,硼原子2s轨道上的一个电子先激发到空的2p轨道上去,然后一个2s轨道和两个2p轨道进行sp2杂化形成三个夹角为120°的sp2杂化轨道。每个sp2杂化轨道与F原子的一个2p轨道重叠组成一个(sp2-p)σ键。BG3是平面三角形结构。分子中四个原子处在同一平面上,B原子位于中心(图4-15)。
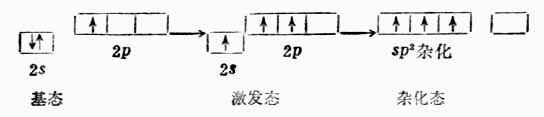
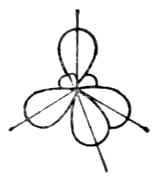
图4-15 BF分子构成 图4-16四个sp杂化轨道
3.sp3杂化
一个s轨道和三个p轨道杂化形成四个sp3杂化轨道,每个sp3杂化轨道含有1/4s和3/4p成分。每两个杂化轨道间的夹角为109°28’。
四个sp3杂化轨道的取向是指向正四面体的四个顶角。所以sp3杂化轨道也称正四面体杂化轨道(图4-16)。
在形成CH4分子时,碳原子的一个2s电子先激发到空的2p轨道上去然后一个2s轨道和三个2p轨道杂化组成四个等同的sp3杂化轨道。四个氢原子的1s轨道分别同碳原子的四个sp3杂化轨道重叠,组成四个(sp3-p)σ键,形成CH4分子。
第三节 氢键
一、氢键的本质
氢原子与电负性很大、半径很小的原子X(F,O,N)以共价键形成强极性键H-X,这个氢原子还可以吸引另一个键上具有孤对电子、电负性大、半径小的原子Y,形成具有X-H…Y形式的物质。这时氢原子与y 原子之间的定向吸引力叫做氢键(以H…Y表示)。
氢键的本质一般认为主要是静电作用。在X-H…Y中,X-H是强极性共价键,由于X的电负性很大,吸引电子能力强,使氢原子变成一个几乎没有电子云的“裸露”的质子而带部分正电荷。它的半径特别小,电场强度很大,又无内层电子,可以允许另一个带有部分负电荷的Y原子(即电负性大,半径小且有孤对电子的原子)充分接近它,从而产生强烈的静电相互作用而形成氢键。
一般分子形成氢键必须具备两个基本条件:
1.分子中必须有一个与电负性很强的元素形成强极性键的氢原子。
2.分子中必须有带孤对电子,电负性大,原子半径小的元素。
氢键常在同类分子或不同类分子之间形成,叫做分子间氢键,如氟化氢、氨水:
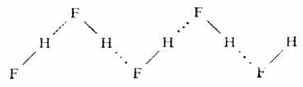
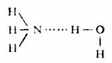
二、氢键的键长和键能
氢键的键长是指X-H…Y中X与Y原子的核间距离。在HF缔合而成的(HF)n缔合分子中,氢键的键长为255pm,而共价键(F-H间)键长为92pm。由此可得出,H…F间的距离为163pm(255-92)。可见氢原子与另一个HF分子中的F原子相距是较远的。
氢键的键能是指被破坏H…Y键所需要的能量。氢键的键能约为15-30kJ·mol-1,比一般化学键的键能小得多,和范德华力的数量级相同。氢键的强弱与X和Y的电负性大小有关。电负性越大,氢键的强弱还和Y的半径大小有关,y 的半径越小,越能接近H-X键,形成的氢键也越强。例如F的电负性最大,半径又小,所以F-H…F是最强的氢键,O-H…O次之,O-H…N又次之,N-H…N更次之。
三、氢键的饱和性和方向性
氢键具有饱和性和方向性。氢键的饱和性表现在X-H只能和一个Y原子相对合。因为H原子体积小,X、Y都比氢大,所以当有另一个Y原子接近他们时,这个Y原子受到X-H…Y上X和Y的排斥力大于受到H原子的吸引力,使得X-H…Y上的氢原子不能再和第二个Y原子结合,这就是氢键的饱和性。
氢键的方向性是指Y原子与X-H形成氢键时,在尽可能的范围内要使氢键的方向与X-H键轴在同一个方向,即以H原子为中心三个原子尽可能在一条直线上。氢原子尽量与Y原子的孤对电子方向一致,这样引力较大;三个原子尽可能在一条直线上,可使X与Y的距离最远,斥力最小,形成的氢键强。
四、氢键对物质性质的影响。
(一)对沸点和熔点的影响
在同类化合物中,能形成分子间氢键的物质,其熔点、沸点要比不能形成分子间氢键的物质的熔点、沸点高些。因为要使固体熔化或液体汽化,不仅要破坏分子间的范德华力,还必须提供额外的能量破坏氢键。H2O,HF,NH3的熔点和沸点比同族同类化合物为高(见表4-3),因为它们都可形成分子间氢键。
表4-3 H2O,HF,NH3及其同族同类化合物的熔、沸点
| 化合物 | mp/℃ | bp/℃ | 化合物 | mp/℃ | bp/℃ | 化合物 | mp/℃ | bp/℃ |
| H2O | 100 | HF | -80.3 | 19.5 | NH3 | -77.7 | -33.4 | |
| H2S | -85.6 | -60.7 | HCL | -112 | -84 | PH3 | -133.5 | -87.4 |
| H2Se | -64 | -42 | HBr | -88 | -67.0 | AsH3 | -116 | -62 |
| H2Te | -48 | -1。8 | HI | -50。9 | -35.4 | SbH3 | -88 | -17 |
(二)对溶解度的影响
在极性溶剂中,如果溶质分子和溶剂分子之间可以形成氢键,则溶质的溶解度增大。例如,苯胺和苯酚在水中的溶解度比在硝基苯中的溶解度要大。
第四节 硫酸和硫醚
硫在周期表内与氧同属第六主族,最外层未成对的p电子也是两个,因此硫也能形成与氧相类似的化合物。
R-OH 醇R-O-R ‘醚
R-SH硫醇R-S-R‘ 硫醚
一、硫醇的构造和性质
硫醇可看作是硫化氢(H2S)分子中一个氢被烃基取代的化合物,通式为R-SH。-SH称为巯基或氢硫基,它是硫醇的官能团。简单的硫醇有甲硫醇CH3SH、乙硫醇CH3CH2SH等。巯基也存在于某些结构复杂的化合物中,例如与人体代谢有关的辅酶A分子中就含有巯基。
低级的硫醇具有极难闻的臭味,沸点比对应的醇为低,微溶于水。高级的硫醇的臭味随相对分子质量的增大而逐渐减少,沸点则与相应的醇相近,难溶于水面易溶于有机溶剂中。
硫醇的化学性质与醇有相似的方面,也有不同的地方,如硫醇也可与酸成酯,但硫醇的酸性却比相应的醇强(例如乙硫醇的pKa为9.5,就比乙醇的pKa=17小得多)。因此硫醇可与氢氧化钠作用,也能与某些金属特别是重金属的氧化物作用,生成相应的硫醇盐。由重金属形成硫醇盐后大减低了重金属的毒性,因此临床上常用某些含有巯基的化合物作重金属中毒时的解毒剂。例如:
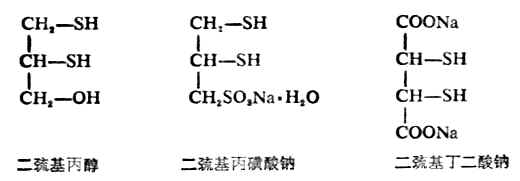
它们均含有两个相邻的巯基,能与砷、汞、锑等金属作用生成稳定无毒的环状化合物。例如:
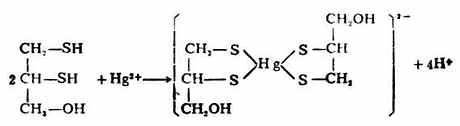
反应产物可由尿排出,从而使金属不再损害体内酶系统的活性,起到解毒作用。
二巯式丙醇,最早是路易斯气(一种含砷的毒气CLCH=CHAsCL2)中毒的解毒剂,因毒性较大,已逐渐被其他解毒剂所代替,如二巯基丁二酸钠就是由我国创制的一个毒性较低、效力更强的新解毒剂。
硫醇另一个与醇不同的性质是,它容易被氧化生成二硫化物。
![]()
二硫化物
二硫化合物中的“-S-S-”键称二硫键,许多蛋白质的结构中存在这种键。当二硫化物还原时,二硫键断裂重新恢复原来的巯基。
二、硫醚的构造和性质
硫醚可看作是硫化氢分子中的两个氢原子都被烃基取代的化合物,通式为R-S-R。例如二甲硫醚CH3-S-CH3、甲乙硫醚CH3-S-C2H5等。
硫醚的物理性质与硫醇相似,但臭味不如硫醇那样强烈。硫醚易被氧化,而使硫的化合价从二价变为四价或六价,即硫醚第一步可氧化成亚砜,亚砜又可进一步氧化成砜。
芥子气(β,β‘-二氯二乙硫醚)是硫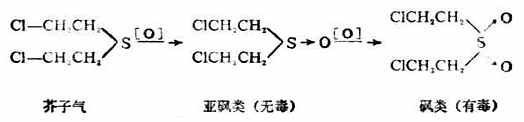 醚的衍生物,是持久性的糜烂性毒剂,对皮肤有腐蚀作用,沾在皮肤上引起难以痊愈的溃疡。它的蒸气能透过衣服,对人类的粘膜组织及呼吸器官都有损害作用。
醚的衍生物,是持久性的糜烂性毒剂,对皮肤有腐蚀作用,沾在皮肤上引起难以痊愈的溃疡。它的蒸气能透过衣服,对人类的粘膜组织及呼吸器官都有损害作用。
芥子气是无色油状液体,沸点217℃,熔点14℃。具有芥末的气味,不溶于水,易溶于乙醇、苯等有机溶剂。
漂白粉能与芥子气起氧化、氯代反应,将芥子气变为毒性较小的亚砜等产物。
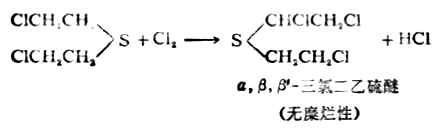
第五章 配位化合物
配位化合物简称配合物,又称络合物,是一类非常广泛和重要的化合物。随着科学技术的发展,它在科学研究和生产实践中显示出越来越重要的意义,配合物不仅在化学领域里得到广泛的应用,并且对生命现象也具有重要的意义。例如,在植物生长中起光合作用的叶绿素,是一种含镁的配合物;人和动物血液中起着输送氧作用的血红素,是一种含有亚铁的配合物;维生素B12是一种含钴的配合物;人体内各种酶(生物催化剂)的分子几乎都含有以配合状态存在的金属元素。因此学习有关配合物的基本知识,对学习医学来说也是十分必要的。
第一节 配合物的基本概念
一、配合物的定义
如果在硫酸铜溶液中加入氨水,首先可得到浅蓝色碱式硫酸铜[Cu(OH)2]SO4沉淀,继续加入氨水,则沉淀溶解而得到深蓝色溶液。显然由于加入过量的氨水,NH3分子与Cu2+离子间已发生了某种反应。
经研究确定,在上述溶液中生成了深蓝色的复杂离子[Cu(NH3)4]2+。从溶液中还可结晶出深蓝色[[Cu(NH3)4]SO4晶体。这说明CuSO4溶液与过量氨水发生了下列反应:
![]()
或离子方程式
![]()
已知NaCN,KCN有剧毒,但是亚铁氰化钾(K4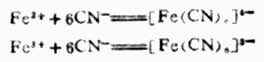
[Fe(CN)6])和铁氰化钾(K3[Fe(CN)6])虽然都含有氰根,却没有毒性,这是因为亚铁离子或铁离子与氰根离子结合成牢固的复杂离子,失去了原有的性质。
由一个阳离子(如Cu2+或Fe3+)和几个中性分子(如NH3)或阴离子(如CN-)以配价键结合而成的,具有一定特性的复杂粒子,其带有电荷的叫配离子或络离子,其不带电荷的叫配合分子或络合分子。配合分子或含有配离子的化合物叫配合物。例如:[Cu(NH3)4]SO4,K4[Fe(CN)6],K3[Fe(CN)6],K2[HgI4],[Ag(NH3)2]NO3,[Pt(NH3)2CL4],[Co(NH3)5(H2O)]CL3等都是配合物。
二、配合物的组成
(一)中心离子
中心离子也称配合物的形成体,它是配合物的核心部分,位于配离子(或分子)的中心,一般都是带正电荷的,具有空的价电子轨道的阳离子。例如,上例中的Cu2+,Fe3+,Pt4+等。中心离子绝大数都是金属离子。其中的过渡金属离子是较强的配合物形成体。
(二)配位体
在配离子中同中心离子配合的离子(或分子)叫配位体。配位体是含有孤对电子的分子或阴离子,直接同中心离子结合的原子称为配位原子。配位原子主要属于周期表中Ⅴ、Ⅵ、Ⅶ三个主族元素。一个配位体可能含有一个以上的配位原子。
配合物一般可分为内界和外界两个组成部分。中心离子和配位体组成配合物的内界,在配合物的化学式中一般用方括号表示内界,方括号以外的部分为外界。例如,在[Cu(NH3)4]SO4中,四个NH3和一个Cu2+组成内界,一个SO2-4为外界。在K3[Fe(CN)6]中,六个CN-和一个F3+组成内界,三个K+为外界。
在[Pt(NH3)CL4]中,二个NH3,四个CL-和Pt4+为内界,它没有外界。
配位体按所含配位原子的数目,可分为单齿配体和多齿配体。只有一个配位原子同中心离子配合的配位体,称为单齿(或一价)配体,如F-,CL-,Br-,I-,CN-,NO-2,NO-3,NH3,H2O等。有两个以上的配位原子同时跟一个中心离子配合的配位体,统称为多齿配体,如乙二胺H2N-CH2-CH2-NH2,有两个氨基氮是配位原子。又如,乙二胺四乙酸根(-OOC-CH2)2N-CH2-CH2-N(CH2-COO-)2中,除有两个氨基氮是配位原子外,还有四个羟基氧也是配位原子。
现将常见的配位体列入表5-1。
表5-1 常见的配位体
| 配位原子 | 配位体举例 |
| 卤素 | F-,CL-,Br-,I- |
| O | H2O,RCOO-,C2O2-4(草酸根离子) |
| N | NH3,NO(亚硝基),NH2-CH2-CH2-NH2(乙二胺) |
| C | CN-(氰离子) |
| S | SCN-(硫氰根离子) |
(三)配位数
在内界里,与中心离子的结合的配位原子的数目,叫做该中心离子的配位数。一般中心离子的配位数为2,4,6,8。最常见的是4和6(表5-2)
表5-2 常见离子的配位数
| 配位数 | 离子 |
| 2 | Ag+,Cu2+,Au+ |
| 4 | Zn2+,Cu2+,Hg2+,Ni2+,Co2+,Pt2+,Pd2+,Si4+,Ba2+ |
| 6 | Fe2+,Fe3+,Co2+,Co3+,Cr3+,Pt4+,Pd4+,Al3+,Si4+,Ca2+,Ir3+ |
| 8 | Mo4+,W4+,Ca2+,Ba2+,Pb2+ |
| 配位数 | 离子 |
在计算中心离子的配位数时,一般是先在配合物中确定中心离子和配位体,接着找出配位原子的数目。如果配位体是单齿的,配位体的数目就是该中心离子的配位数。例如,[Pt(NH3)4]Cl2和[Pt(NH3)2Cl2]中的中心离子都是Pt2+,而配位体前者是NH3,后者是NH3和Cl--,这些配位体都是单齿的,因此它们的配位数都是4。
如果配位体是多齿的,那么配位体的数目显然不等于中心离子的配位数(见螯合物一节)。
(四)配离子(或络离子)的电荷
配离子的电荷等于中心离子电荷与配位体电荷的代数和。
[Cu(NH3)4]2++2+4×0=+2
[Fe(CN)6]3- +3+6×(-1)=-3
[Fe(CN)6]4- +2+6×(-1)=-4
[HgI4]2- +2+4×(-1)=-2
三、配合物的命名
配合物的命名方法从一般无机物的命名原则:阴离子名称在前,阳离子名称在后;当配离子是阳离子时,外界阴离子为酸根;当配离子是阴离子时,则该配离子为酸根。命名时,酸根为简单离子时称“某化某”,酸根为复杂离子时称“某酸某”。在命名配离子时,要在形成体与配位体的名称间加个“合”字,并按下列顺序列出其组成部分的名称。配位体数-配位体名称-“合”字-形成体名称-形成体价态(用罗马数字表示)。当配位体个数为一时,有时可将“一”字省去。若形成体仅有一种价态时也可不加注罗马数字。如果内界中含有不止一种配位体,则命名时,阴离子配位体在先,中性分子配位体在后。对于几种不同阴离子组成的配位体,命名顺序为:简单阴离子-复杂阴离子-有机酸根离子。对于几种中性分子组成的配位体,命名顺序为:简单阴离子-复杂阴离子-有机酸根离子。对于几种中性分子组成的配位体,命名顺序为:水-氨-有机分子。
配位体的个数用一、二、三等表示。
中心离子的价态用Ⅰ、Ⅱ、Ⅲ等表示。
例如:
[Cu(NH3)4]2+四氨合铜(Ⅱ)离子
[Fe(CN)6]3- 六氰合铁(Ⅲ)离子
配离子是阳离子的配合物:
[Co(NH3)4CL2]CL氯化二氯四氨合钴(Ⅲ)
[Cu(NH3)4]SO4硫酸四氨合铜(Ⅱ)
配离子是阴离子的配合物:
K2[PtCL6]六氯合铂(Ⅳ)酸钾
Na4[Fe(CN)6] 六氰合铁(Ⅱ)酸钠
在不致引起误解的情况下,“合”字和价数有时可以省略。如二氯二氨合铁(Ⅱ)可称为二氯二氨铂,称为氯化二氨银。
有些常见的配合物和配离子可用简称。
K4[Fe(CN)6] 亚铁氰化钾
K3[Fe(CN)6] 铁氰化钾
K2[PtCL6] 氯铂酸钾
K2[HgI4]碘化汞钾
[Ag(银NH3)2]+ 氨配离子
[PtCL6]2- 氯铂酸根
第二节 配合物的配位键理论
一、配合物配位键理论的基本要点
配位键理论又叫配价键理论,其基本要点可归纳为三点:
1.中心离子和配位原子间是以配价键结合的,具有孤对电子的配位原子提供电子对,填入中心离子的外层空轨道形成配位键。
2.中心离子所提供的空轨道在与配位原子成键时必须经杂化,形成数目相等的杂化轨道。这些杂化轨道的能量相同,而且有一定的方向性。它们分别和配位原子的孤对电子轨道在一定方向上彼此接近,发生最大的重叠而形成配位键,这样就形成了各种不同的配位数和不同构型的配合物。
3.中心离子的空轨道杂分时,若有次外层d轨道参加,则形成的配合物属内轨型;若均为最外层轨道参加杂化,则形成的配合物属外轨型。内轨型配合物的配位键更具有共价键性质所以叫共价配键,外轨型配合物的配位键更具有离子键性质所以叫电价配键,但本质上两者均属共价键范畴。
例1 [Ni{CH}4]2- Ni 原子和Ni2+的价电子层结构分别是3d84s2和3d3。
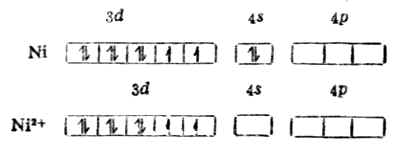
在Ni2+的外层电子中,有两上自旋方向上相同的未成对电子,故具顺磁性。但当它与四个CN-形成[Ni{CN}4]2-配合后却具反磁性,说明配离子中已无未成对电子。配位键理论认为:原在3d轨道中的两个未成对电子合并在一个3d轨道上,空出一个3d轨道和外层的一个4s轨道及二个4p轨道杂化形成四个等价的dsp2杂化轨道所构成的配离子属内轨型配合物,它的磁性比简单离子(Ni2+)的磁性小,它的外层电子结构为:
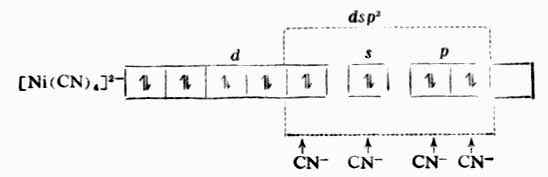
例2 [Fe(CN)6]3- Fe原子和Fe 3+的价电子层结构分别是3d6,4s2,3d5。
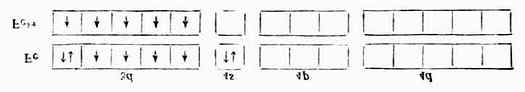
[Fe(CN)6]3-配离子中的Fe 3+在配位体CN-的影响下,把原来分布在5个3d轨道上的5个未成对电子挤到3个3d轨道上,空出2个3d轨道与外层的1个4s轨道和3个4p轨道杂化成6个等价的d2sp3杂化轨道与6个配位体CN-成键,形成的[Fe(CN)6]3-配离子属内轨型。在与离子中只有1个未成对电子,故它的磁性比Fe 3+的磁性小,它的外层电子结构为:
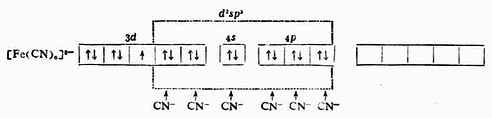
例3 [FeF6]3-
当Fe 3+和6个F-形成[FeF6]3-配离子时,磁矩未变,说明配离子中仍保留有5个未成对电子。配位键理论认为:Fe 3+利用外层的一个4 s 轨道、3个4p轨道和2个4d轨道与6个配位体F-成键,故所形成的[FeF6]3-配离子属外轨型,它的外层电子结构为:
①原子或离子的磁矩μ与原子中未成对电子数n有如下近似关系:
![]()
式中μ以玻尔磁子(BM)为单位
(1BM=eh/2m)
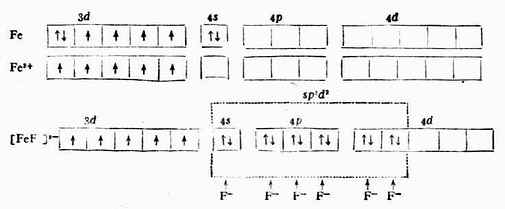
二、内轨型配合物与外轨型配合物
前面已提到,在形成配合物中,配位体的孤对电子所占空轨轨道是有(n-1)d轨道参与的杂化轨道[(n-1)d+ns+np],所以叫轨型配合物。如[Ni(CN)4]2-,[Fe(CN)6]3-,[Mn(CN)6]4-,[Co(NH3)6]3+,[Pt(NH3)2CL2]等都属于此类。一般来说,内轨型配合物中,共享电子对深入中心离子内层杂化轨道,成键时中心离子的电了层结构有所改变,形成的配键主要是共价键性质,因此这种配合物比较稳定。
在形成配合物中,配位体的孤对电子所占据的ns+np+nd所组成的杂化轨道,没有(n-1)d轨道参加,所以叫外轨型配合物。如[FeF6]3-,[Fe(H2O6]3+,[Co(NH3)6]2+,[Ni(NH3)4]2+等都属于此类。一般来说,内轨型配合物中,共用电子对处于中心离子的外层杂化轨道,成键时,中心离子的电子层结构保持不变,形成的配键具有离子键的特性。由于nd轨道的能量比(n-1)d为高,所以外轨型配合物一般不如内轨型配合物稳定。
表5-3 内轨型配 合物与外轨型配合物
| 类别 | 键型 | 配位体 | 电子结构 | 中心离子 | 杂化轨道 | 配位数 | 稳定性 |
| 外轨型配合物 | 电价配键 | F-离子和H2O分子等配位体 | 成键时中心离子的电子层结构保持 | Ag+,Hg2+ | sp | 2 | 较小 |
| Al3+Zn2+,Co2+,Fe2+,Cu2+,Cd2+ | Sp3 | 4 | |||||
| Fe3+Cr3+Co2+Ni2+Pd4)MN3+ | sp3d2 | 6 | |||||
| 内轨型配合物 | 共价配键 | NH3CL-RNH2 | 成键时引起中心离子d层电子层电的重排。 | Pt2+,Pt4+,Ni2+Au3+,Pd2+ | Dsp2 | 4 | 较大 |
| CN-和NO-2等配位体 | Fe3+,Cr3+,Co3+,Ni3+,Pd4+,Mn3+ | D 2sp3 | 6 |
第三节 配合物的稳定性
一、配离子的离解平衡
将氨水加到硝酸银溶液中,则有[Ag(NH3)2]+配离子生成,反应式为:
Ag++2NH3→[Ag(NH3)2]+
此反应称为配合反应(也叫络合反应)。
由于配离子是由中心离子和配位体以配价键结合起来的,因此,在水溶液中比较稳定。但也并不是完全不能离解成简单离子,实质上和弱电解质类似,也有微弱的离解现象。
![]()
(一)配合物的稳定常数
配合物的稳定性,可以用生成配合物的平衡常数来表示,例如:
![]()
应用化学平衡原理,可得:
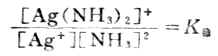
K稳值越大,表示形成配离子的倾向越大,此配合物越稳定。所以配离子的生成常数又称为稳定常数(附录八)。
(二)分布稳定常数
配合物在溶液中的生成与离解,与多元酸、碱相似,也是分级进行的,而且各级离解或生成常数也不一样。例如,Cu2+与NH3逐步配合过程中的分步稳定常数(30℃)分别为:
K1,K2,K3,K4称为逐级稳定常数。由上可见,配合物的逐级稳定常数随着配位数的增加而下降。一般认为,随着配位体数目增多,配位体之间的排斥作用加大,故其稳定性下降。
配合物的逐级稳定常数和稳定常数间有下述关系:
K= K1·K2·K3·K4…Kh
对[Cu(NH3)4]2+来说,其稳定性k 为:
K= K1·K2·K3·K4
K=(1.41×104)(3.17×103)(7.76×102)(1.39×102)=4.8×1012
(三)不稳定常数
在水溶液中,[Ag(NH.3)2]+是稳定的,不过像其他弱电解质一样也有少数[Ag(NH.3)2]+发生离解,可用下式表示:
![]()
则平衡常数表达式为:
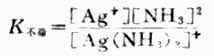
K不稳值愈大,表示配离子离解愈多,故称K不稳为配离子的不稳定常数。
K稳和K不稳互成倒数:
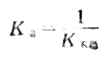
二、配合平衡的移动
金属离子Mn+和配位体A-生成配离子MA(n-x)+x,在水溶液中存在如下平衡:
![]()
根据平衡移动原理,改变Mn+或A-的浓度,会使上述平衡发生移动。若在上述溶液中加入某种试剂使Mn+生成难溶化合物,或者改变Mn+的氧化状态,都会使平衡向左移动。若改变溶液的酸度使A-生成难离解的弱酸,也可使平衡向左移动。
配合平衡同样是一种相对的平衡状态,它同溶液的PH值、沉淀反应、氧化还原反应等都有密切的关系。
(一)与酸度的关系
根据酸碱质子理论,所有的配位体都可以看作是一种碱。因此,在增加溶液中的H+浓度时,由于配位体同H+结合成弱酸面使配合平衡向右移动,配离子平衡遭到破坏,这种现象称为酸效应,例如:
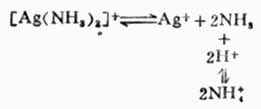
配位体的碱性愈强,溶液的PH值愈小,配离子愈易被破坏。
金属离子在水中,都会有不同程度的水解作用。溶液的PH值愈大,愈有利于水解的进行。例如:Fe3+在碱性介质中容易发生水解反应,溶液的碱性愈强,水解愈彻底(生成Fe(OH)3沉淀)。
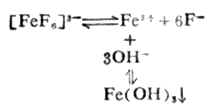
因此,在碱性介质中,由于Fe3+水解成难溶的Fe(OH)3沉淀而使平衡向右移动,因而[FeF6]3-遭到破坏,这种现象称为金属离子的水解效应。
(二)与沉淀反应的关系
当向含有氯化银沉淀的溶液中加入氨水时,沉淀即溶解。
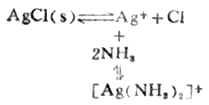
当在上述溶液中加入溴化钠溶液时,又有淡黄色的沉淀生成。
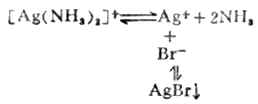
由于AgBr的溶解度比AgCL的溶解度小得多,因而Br-=争夺Ag+的能力比CL-的大,所以能产生AgBr沉淀而不能产生AgCL沉淀。沉淀剂与金属离子生成沉淀的溶解度愈小,愈能使配离子破坏而生成沉淀。
(三)与氧化还原反应的关系
配合反应的发生可以改变金属离子的氧化能力。例如:当PbO2(Pt+)与盐酸反应时,其产物不是PbCL4,而是PbCL2和CL2。但是当它形成[PbCL6]2-配离子后,Pb就能保持它的+4氧化态。
配合反应影响氧化还原反应的方向。例如,Fe3+可以把I-氧化成I2:
![]()
在加入F-后,由于生成[FeF6]3-,减少了Fe3+的浓度,使平衡向左移动。
当我们考查配合反应对氧化还原反应的影响时,不仅要注意配离子的形成,而且还要注意配离子的稳定性。
第四节 螯合物(内络合物)
一、螯合物的概念
螯合物又称内络合物,是螯合物形成体(中心离子)和某些合乎一定条件的螯合剂(配位体)配合而成具有环状结构的配合物。“螯合”即成环的意思,犹如螃蟹的两个螯把形成体(中心离子)钳住似的,故叫螯合物。
形成螯合物的第一个条件是螯合剂必须有两个或两个以上都能给出电子对的配位原子(主要是N,O,S等原子)。第二个条件是每两个能给出电子对的配位原子,必须隔着两个或三个其他原子,因为只有这样,才可以形成稳定的五原子环或六原子环。例如,在氨基乙酸根离子(H2N-CH2-COO-)中,给出电子的羟基氧和氨基氮之间,隔着两个碳原子,因此它可以形成稳定的具有五原子环的化合物。
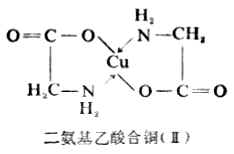
四原子环在螯合物中是不常见的,六原子以上的环也是比较少的。中心离子有一定的电荷数,同时也有一定的配位数。Cu(Ⅱ)带有二个正电荷,它的配位数为4。氨基乙酸根离子(H2N-CH2-COO-)既有氨基氮,都能给出电子对;氨基氮能满足中心离子的配位数,羟基氧则能使配位数和电荷数同时得到满足,因此Cu 2+和两个(H2N-CH2-COO-)螯合后,得到的是中性分子二氨基乙酸合铜(Ⅱ)(简称氨基乙酸酮)[Cu(H2N-CH2-COO)2]由于羟基氧带有负电荷,故它与Cu 2+形成的配键通常用“-”表示。
螯合物的特殊稳定性是环形结构带给它们的特征之一。环愈多使螯合物愈稳定。通常所说的“螯合反应”就是指由于螯合而使化合物具有特殊的稳定性。
由于螯合物的特殊稳定性,已很少能反映金属离子在未螯合前的性质。金属离子在形成螯合物后,在颜色、氧化还原稳定性、溶解度及晶形等性质发生了巨大的变化。很多金属螯合物具有特征性的颜色,而且这些螯合物可以溶解于有机溶剂中。利用这些特点,可以进行沉淀、溶剂萃取分离、比色定量等分析分离工作。
二、螯合剂
常用的螯合剂是氨螯合剂,是一类似以氨基二乙酸[HN(CH2COOH)2]为基体的螯合剂,它以N,O为螯合原子,与金属离子螯合时形成环状的螯合物
![]()
常用的氨羧螯合剂有:
氨羧螯合剂Ⅰ(ATA)指的是氨三乙酸,它的结构是:
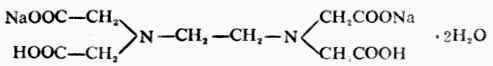
氨羧螯合剂Ⅱ(EDTA)指的是乙二胺四乙酸。它的结构是:
![]()
乙二胺四乙酸是四元酸,如果用Y表示它的酸根,则乙二胺四乙酸可以简写成H4Y。
由于乙二胺四乙酸在水中的溶解度比较小,而其二钠盐在水中的溶解度却比较大。因些在实际应用中人们常采用EDTA二钠盐。EDTA二钠盐含有2分子结晶水,它的结构是:
![]()
EDTA二钠盐有时也叫做EDTAⅢ。但习惯上仍把它叫做EDTA。用简式Na2H2Y·2H2O表示它。
EDTA是四元酸,它在水中是分步离解的:
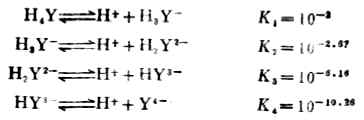
除碱金属离子外,EDTA几乎能与所有的金属离子形成稳定的金属螯合物。并且,在一般情况下,不论金属离子是几价,1个金属离子都能与1个EDTA酸根(Y4-)形成可溶性的稳定螯合物。例如:
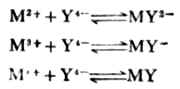
式中M表示金属离子,右上角的数字和符号表示离子的离子价。
虽然,除碱金属离子外,各金属离子大多数能与EDTA形成螯合物,但它们的稳定性差别很大。
EDTA是应用最广的一种氨羧螯合剂,用EDTA标准液可以滴定几十种金属离子,这个方法就称EDTA滴定法。目前所谓螯合滴定法主要是指EDTA滴定。
三、螯合物在医学上的应用
螯合物在自然界存在得比较广泛,并且对生命现象有着重要的作用。例如,血红素就是一种含铁的螯合物,它在人体内起着送氧的作用。
维生素B12是含钴的螯合物,对恶性贫血有防治作用。胰岛素是含锌的螯合物,对调节体内的物质代谢(尤其是糖类代谢)有重要作用。有些螯合剂可用作重金属(Pb2+,Pt2+,Cd2+,Hg2+)中毒的解毒剂。如二巯基丙醇或EDTA二钠盐等可治疗金属中毒。因为它们能和有毒金属离子形成稳定的螯合物,水溶性螯合物可以从肾脏排出。
有些药物本身就是螯合物。例如,有些用于治疗疾病的某些金属离子,因其毒性,刺激性、难吸收性等不适合临床应用,将它们变成螯合物后就可以降低其毒性和刺激性,帮助吸收。
另外在生化检验、药物分析、环境监测等方面也经常用到螯合物。
第六章 氧化还原与电极电位
氧化还原反应是一类重要的化学反应。它不仅在工农业生产和日常生活中具有重要意义,而且在人体内进行的一系列化学反应中,有许多是氧化还原反应。本章将在氧化还原反应的基础上,着重讨论如何将化学能转变为电能、电极电位和电池电动势的产生及其应用等有关知识。
第一节 氧化还原
一、氧化还原的概念
(一)元素的氧化数
元素的氧化素是指分子中各原子所表现出来的形式电荷数。确定元素氧化数的原则是:
1.在单质的氧化数为零。
2.在简单离子中,元素的氧化数等于该离子所带的电荷数。例如,Na+中Na的氧化数为+1,S2-中S的氧化数为-2。
3.氧在化合物中的氧化数为-2(过氧化物如H2O2中,氧的氧化数为-1,氢在化合物中的氧化数为+1,(金属氢化物如CaH2中,氢的氧化数为-1)。
4.分子中各元素氧化数的代数和等于零。
在离子化合物中元素的氧化数和它的化合价是一致的;在共价化合物中元素的氧化数与它的共价有所不同。氧化数有正、负之分,而共价则无正、负。元素的化合价只能是整数,而元素的氧化数可是整数彵可是分数。
例1:求Na2S4O6中S的氧化数。
解:设Na2S4O6中S的氧化数为x:
2×1+4x+6×(-2)=0
4x=10
x=+(5/2)
即Na2S4O6中S的氧化数为+(5/2)。
(二)氧化还原的概念
在化学发展的初期,氧化是指物质与氧化合的过程,还原是指物质失去氧的过程。例如,汞与氧化合生成的氧化汞时,汞被氧化生成氧化汞。
2Hg+O2→2HgO
相反地,当氧化汞加热分解成汞和氧时,氧化汞失去氧被还原成汞。
2HgO→2Hg+O2
以后氧化还原的概念扩大了,认为物质失去氢的过程也是氧化,与氢结合的过程则是还原。这种去氢氧化(即脱氢氧化),加氢还原的概念,在有机化学和生物化学中应用较为广泛。例如,乙醇脱氢被氧化成乙醛。
![]()
丙酮加氢被还原成异丙醇。
![]()
然而,这些概念不能应用到没有氢和氧参加的氧化还原反应上,也没有指出氧化还原反应的实质。
现在认为,氧化还原反应的特征是在反应前后某些元素的氧化数有了改变,其实质是物质之间有电子的得失。因此,有些反应虽然没有氧或氢参加,但由于有氧化数的改变,即有电子的得失,所以也是氧化还原反应。例如,锌与铜离子的反应。
Zn+Cu2+→Zn2+Cu
反应中,每个锌原子失去两个电子,变为锌离子,氧化数由零升高到+2,锌被氧化是还原剂;每个铜离子接受两个电子,变为铜,氧化数由+2降低到零,铜离子被还原是氧化剂。
Zn-2e-→Zn2+(氧化反应)
Cu2++2e-→Cu (氧化反应)
我们把物质失去电子(元素的氧化数升高)的过程称为氧化;物质得到电子(元素的氧化数降低)的过程称为还原。在任何化学反应中,若有得到电子的物质,必然有失去电子的物质,且得失电子总数相等,因而氧化与还原必定同时发生。
二、氧化剂与还原剂的共轭关系
在氧化还原反应中,还原剂被氧 化,生成与之共轭的氧化剂。
![]()
同理,在氧化还原反应中,氧化剂被还原,生成与之共轭的还原剂。
![]()
因此,氧化剂与还原剂的共轭关系可用下式表示:
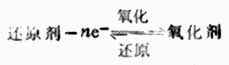
一种还原剂要失去电子表现出可被氧化的性质,只有在能得到电子可被还原的另一种氧化剂的存在下才能实现,即
![]()
例如,在 Zn +Cu2+=Cu+Zn2+反应中,还原剂1Z失去电子,氧化数升高,其产物为氧化化剂1Zn2+;氧化剂2Cu2+得到电子,氧化数降低,其产物为还原剂2Cu。这样Zn与Zn2+,Cu2+与 Cu构成了如下两个共轭的氧化还原电对:
Zn2+/Zn Cu2+/Cu
(氧化剂)(还原剂) (氧化剂)(还原剂)
在氧化还原电对中,氧化数高的物质为氧化型物质,氧化数低的物质为还原型物质。如果还原剂越强(失去电子的能力越大),则其共轭的氧化剂越弱(得到电子的能力越小);如果氧化剂越强,则其共轭的还原剂越弱。例如,在MnO-4/Mn2+电对中,MnO4是一个强氧化剂,Mn2+是一个弱还原剂。氧化还原反应是按较强的氧化剂和较强的还原剂相互作用方向进行的。
三、氧化还反应的计量关系
在氧化还原反应中,氧化剂与还原剂之间是按一定化学计量关系相互作用的。对于任何一个氧化还原反应:
aA+bB===dD+eE
当反应达到化学计量点时,amol(氧化剂)恰与bmol(还原剂)完全作用,也就是说对于一个能定量进行的氧化还原反应,化学反应方程式中氧化剂与还原剂物质的系数比,就是反应中氧化剂与还原剂相互作用的物质的量之比,即
nA:nB=a:b (6-1)
如果已知氧化剂或还原剂物质的量,通过上式可以计算出还原剂或氧化剂物质的量。例如,2KMnO4+5H2O2+3H2SO4====2MnSO4+K2SO4+8H2O+5O2
从反应式中知,2mol KMnO4与5mol H2O2完全作用,若已知KMnO4物质的量,可以求出H2O 2物质的量。
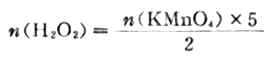
又如,Cr2O2-7+6Fe2++14H+=2Cr3++6Fe3++7H2O,从反应中知,Cr2O2-7与Fe2+反应的物质的量之比为1/6,即有
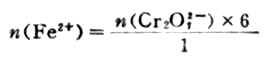
若已知Cr2O2-7物质的量,可求出Fe2+物质的量。
第二节 电极电位
一、原电池
将锌片插入CuSO4溶液中,锌片上的Zn原子失去电子成为Zn2+而溶解;溶液中的Cu2+得到电子成为金属Cu在锌片上析出,即发生如下的氧化还原反应:
反应中电子从锌原子转移给铜离子。由于锌片和硫酸铜溶液直接接触,溶液中铜离子无秩序地自由运动,使得
Zn和Cu2+之间电子的转移是直接的、无序的,不能定向地形成电流,化学能都以热的形式散失在环境之中。
如果我们采用一个装置(图6-1),使锌原子上的电子不直接转移给铜离子,而是使还原剂Zn失去的电子沿着一条金属导线转移到氧化剂Cu2+上。这样,在导线中就有电流通过。
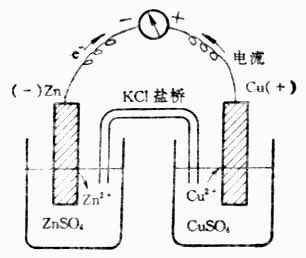
图6-1 铜锌原电池
这个装置是在盛有ZnSO4与CuSO4溶液的烧杯中分别插入锌片和铜片。两个溶液用盐桥相连。盐桥是一支U形管,通常充满用KCL(或KNO3)饱和了的琼脂胶冻。用导线联接两个金属片,并在导线中串联一个灵敏的电流计。通过实验可以看到:
电流计指针发生偏转,说明金属导线上有电流通过。根据指针偏转的方向,可以确定锌片为负极,铜片为正极。
锌片开始溶解,而铜片上有金属铜沉积上去。
取出盐桥,电流计指针回到零点,放入盐桥,电流计指针又偏转。
对上述实验现象可作如下分析:
锌片溶解说明锌片失去电子,成为Zn2+进入溶液。
Zn→Zn2++2e-
电子由锌片经金属导线流向铜片,溶液中Cu2+从铜片上得到电子成为铜原子在铜片上析出。
Cu2++2e-→Cu
盐桥的沟通电路,使反应顺利进行。因为随着反应的不断进行,在ZnSO4溶液中,Zn2+增多,溶液带正电荷;在CuSO4溶液中,由于Cu2+变为Cu,Cu2+减少,溶液带负电荷。这样将阻碍Zn的继续氧化和Cu2+的继续还原。由于盐桥的存在,其中CL-向ZnSO4溶液扩散,K+则向CuSO4溶液扩散,分别中和过剩的电荷,使两溶液维持电中性,保证了氧化还原反应持续进行。
上述装置中进行的总反应为,
Zn+Cu2+→Zn2++Cu
这一氧化不原反应分两处进行,一处进行氧化,另一处进行还原。即电子不是直接从还原剂转移到氧化剂,而是通过外电路进行传递,电子进行有规则的流动,从而产生电流,实现了由化学能到电能的转变。这种借助于氧化还原反应将化学能转变为电能的装置称为原电池。上述由铜、锌及其对应离子所组成的原电池叫做铜锌原电池。
原电池由两个半电池组成。在鲷铜锌原电池中,锌和锌盐溶液组成一个半电池,铜和铜盐溶液组成另一个半电池。半电池又叫电极。
在原电池中,给出电子的电极为负极,发生氧化反应;接受电子的电极为正极,发生还原反应。在铜锌原电池中,锌半电池为负极,铜半电池为正极。
在负极或正极上进行的氧化或还原半反应叫做电极反应。总反应称为电池反应。铜锌原电池的电极反应和电池反应可分别表示如下:
电极反应负极 Zn→Zn2++2e-
正极 Cu2++2e-→Cu
电池反应Zn+Cu2+→Zn2++Cu
单独表示电极组成时,作为导体的金属通常写在右边。铜锌原电池有两个电极组成式为Zn2+│Zn和Cu2+│Cu。
为了方便,原电池装置可用符号表示。书写电池的惯例如下:
1.一般将负极写在左边,正极写在右边。
2.写出电极的化学组成及物态,气态要注明压力(单位为kPa),溶液要注明浓度。
3.单线 “│ ” 表示极板与电极其余部分的界面。
4.同一相中不同物质之间以及电极中其它相界面均用逗呈“,”分开。
5.双线“‖”表示盐桥。
6.气体或液体不能直接作为电极,必须附以不活泼金属(如铂)作电极板起导体作用。纯气体、液体如H2(g)Br2(l)紧靠电极板。
铜锌原电池的电池表示式为:
(一)Zn│Zn2+(c1)‖Cu+(c1)│Cu(+)
FeCL3和SnCL2溶液间可发生下面反应:
2FeCl3+SnCl2→2FeCl2+SnCl4
该反应可以组成一个原电池。电极反应和电池反应及电池表示式为:
电极反应 负极Sn2+→Sn4++2e-
正极Fe3++e→Fe2+
电池反应 2Fe3++Sn2+→2Fe2++Sn4+
电池表示式(-)Pt│Sn2+(c1),Sn4+(c2)‖Fe3+(c3),Fe2+(c4)│Pt(+)
上述电池两个电极组成式为Sn4+,Sn2+│Pt和Fe3+,Fe2+│Pt。
二、电极电位的产生
用导线将原电池的两个电极联接起来,其间有电流通过。这表明两个电极之间存在电位差。下面简单介绍金属及其盐溶液之间相界面上电位差是怎样产生的。
金属晶体是由金属原子、金属离子和自由电子组成的。当把金属插入其盐溶液中时,金属表面的离子与溶液中极性水分子相互吸引而发生水化作用。这种水化作用可使金属表面上部分金属离子进入溶液而把电子留在金属表面上,这是金属溶解过程。金属越活泼,溶液越稀,金属溶解的倾向越大。另一方面,溶液中的金属离子有可能碰撞金属表面,从金属表面上得到电子,还原为金属原子沉积在金属表面上。这个过程为金属离子的沉积。金属越不活泼,溶液浓度越大,金属离子沉积的倾向越大。当金属的溶解速度和金属离子的沉积速度相等时,达到了动态平衡。
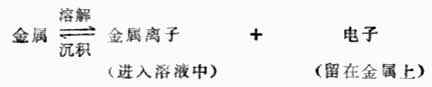
在一给定浓度的溶液中,若金属失去电子的溶解速度大于金属离子得到 电子的沉积速度,达到平衡时,金属带负电,溶液带正电。溶液中的金属离子并不是均匀分布的,由于静电吸引,较多地集中在金属表面附近的液层中。这样在金属和溶液的界面上形成了双电层(图6-2(a)),产生电位差。反之,如果金属离子的沉积速度大于金属的溶解速度,达到平衡时,金属带正电,溶液带负电。金属和溶液的界面上也形成双电层(图6-2(b)),产生电位差。金属与其盐溶液界面上的电位差称为金属的电极电位,常用符号![]()
表示。
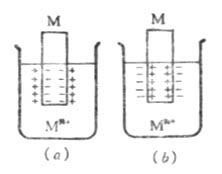
图6-2 双电层
金属与溶液间电位差的大小,取决于金属的性质,溶液中离子的尝试和温度。金属越活泼,电位越低;越不活泼,电位越高。在同一种金属电极中,金属离子浓度越大,电位越高,浓度越小,电位越低。温度越高,电位越高,温度越低,电位越低。
三、电极电位的测定
(一)标准氢电极
电极电位的绝对值是无法测定的,但可以选定一个电极作为标准,将各种待测电极与它相比较,就可得到各种电极的电极电位相对值。国际纯粹和应用化学协会(IUPAC)选定“标准氢电极”作为比较标准。
标准氢电极是氢离子浓度为1mol·L-1氢气的压力为101.325kPa的电极。国际上规定,298K 时,标准氢电极的电极电位为零。用符号![]()
H+/H2=0表示。其电极书写为:
H+(1mol.L-1),H2(101.325kPa)│Pt
标准氢电极的装置如图6-3所示。容器中装有H+浓度为1mol·L-1的硫酸溶液,插入一铂片。为了增大吸附氢气的能力,铂片表面上镀一层疏松的铂(铂黑0。在298k 时,不断从套管的支管中通入压力为101.325 kPa的纯氢气,H2被铂黑吸附直到饱和.这时整个铂黑片仿佛是由氢气组成,铂黑吸咐的H2和溶液中的H+构成了氢电极,其电极反应为;
![]()
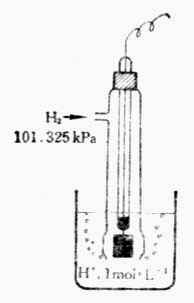
图6-3 标准氢气电极
(二)标准电极电位的测定
参与电极反应的各有关物质均为标准状态(离子浓度为1mol·L-1,气体物质的分压为101.325 kPa)时,其电极电位称为该 电极的标准电极电位,用符号![]() 表示。欲测定某标准电极的电位,可将该电极与标准氢电极组成原电池,书写时把标准氢电极列于左侧(假定为负极),将待测电极列于右侧(假定为正极)。用电位计测定该原电池的标准电动势 Eφ,则有
表示。欲测定某标准电极的电位,可将该电极与标准氢电极组成原电池,书写时把标准氢电极列于左侧(假定为负极),将待测电极列于右侧(假定为正极)。用电位计测定该原电池的标准电动势 Eφ,则有
Eφ=![]()
右-![]()
左=![]()
侍测-![]()
H+/H2
例2测定Zn2+│Zn电极的标准电位,![]()
Zn2+/Zn。
解:将标准Zn2+│Zn电极与标准氢电极组成原电池。
Pt│H2(101.325kPa),H+(1mol.L-1)‖Zn2+(1mol.L-1)│Zn
298K时,测得Eφ=-0.7628(V)。
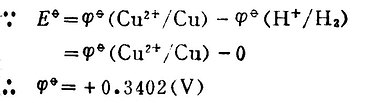
因为Zn2+│Zn电极的电位为负值,低于标准氢电极的电位。所以Zn2+│Zn是极为负极,标准氢电极为正极。其电极反应和电池反应为:
电极反应 负极Zn→Zn2++2e-
正极2H++2e-→H2
电池反应 Zn+2H+→Zn2++H2
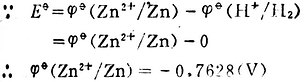
例3 测定Cu2+│Cu电极的标准电极电位,![]()
Cu2+/Cu。
解:将标准Cu2+│Cu电极与标准氢电极组成原电池。
Pt│H2(101.325kPa),H+(1mol.L-1)‖Cu2+(1mol.L-1)│Cu
298K时,测得Eφ=+0.3402(V)。
因为Cu2+│Cu电极的电位为正值,高于标准氢电极的电位。所以Cu2+│Cu电极,标准氢电极为负极。其电极反应和电池反应为,
电极反应 负极H2→2H++2e-
正极Cu2++2e-→Cu
电池反应 H2+Cu2+→2H++Cu
(三)标准电极电位表
用上述方法不仅可以测定金属的标准电极电位,也可测定非金属离子和气体的标准电极电位。对于某些与水剧烈反应而不能直接测定的电极,可以通过热力学数据用间接的方法计算出标准电极电位。表6-1列出了298k 时,一些物质在水溶液中的标准电极电位。
为了正确使用标准电极电位表,将有关问题概述如下:
1.在电极反应式氧化型![]()
还原型中,ne表示电极反应的电子数。氧
化型和还原型包括电极反应所需的H+,OH-,H2O等物质,如
![]()
氧化型与还原型是相互依存的。同一种物质在某一电对中是氧化型,在另一电对中也可以是还原型。例如,
![]()
中是氧化型,在
![]()
(![]() =0.77V)
=0.77V)
中是还原型。所以在讨论与Fe2+有关的氧化还原反应时,若Fe2+是作为还原剂而被氧化为Fe3+,则必须用与还原型的Fe2+相对应的电对的![]()
值(0.77V)。反之,若Fe2+是作为氧化剂而被还原为Fe,则必须用与氧化型的Fe2+相对应的电对的![]()
值(-0.88V)。
2.表6-1采用的电位是还原电位。不论电极进行氧化或还原反应,电极电位符号不改变。例如,不管电极反应是Zn→Zn2++2e-还是Zn2++2e-→Zn,Zn2+│Zn电极标准电极电位值均取-0.7628V。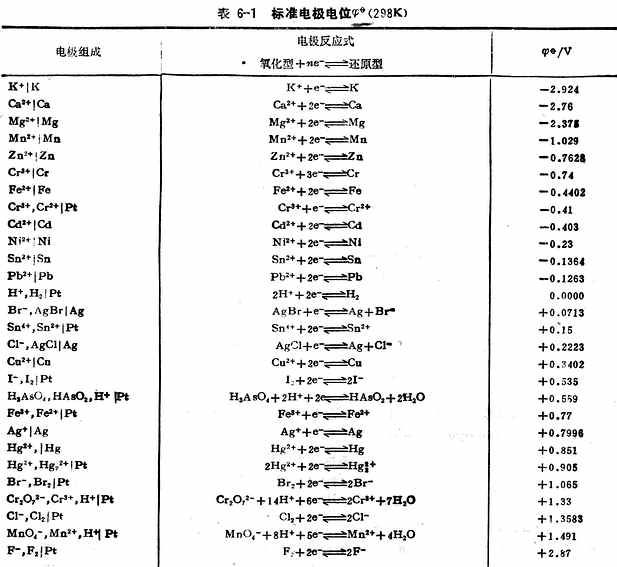
![]()
愈高,表示该电对的氧化型愈容易接受电子,氧化其它物质的能力愈强,它本身易被还原,是一个强氧化剂,而它的还原能力愈弱;![]()
愈低,表示该电对的还原型愈容易放出电子,还原其它物质的能力愈强,它本身易被氧化,是一个强还原剂,而它的氧化型的氧化能力愈弱。
电极反应式左方的氧化型可作氧化剂,右方的还原型可作还原剂。氧化型在表的愈下方就是愈强的氧化剂;还原型在表的愈上方就是愈强的还原剂。因此,在不同的氧化剂或在不同的还原剂之间进行强弱比较时,根据标准电极电位的数值可以明确地判断它们的强弱。例如,在表上所列的各物质中,F2是最强的氧化剂,k 是最强的还原剂。
4.标准电极电位![]()
值与电极反应中物质的计量系数无关。例如,Ag+│Ag电极的电极反应写成,若写成。?![]()
(Ag+/Ag)仍是+0.7996V,而不是2*0.7996V.
5.电极电位和标准电极电位,都是电极处于平衡状态时表现时出来的特征,它和达到平衡的快慢无关。
根据上面所述,在标准状态下,由任何两个电极(半电极)组成电池时,电极电位较高的一方,由于有较强的氧化剂,起还原作用为正极;电极电位较低的一方,由于有较强的还原剂,起氧化作用为负极。
四、影响电极电位的因素
(一)能斯特(Nernst)方程式
一个电极的电极电位的大小与温度、浓度间的关系可用能斯特方程式表示:
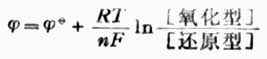 (6-2)
(6-2)
式中![]()
——电极电位,单位为V
![]()
——标准电极电位,单位为V
R——气体常数,8.314J-1.Kmol-1
F——法拉弟常数,96490C.mol-1
T——绝对温度,K
n——电极反应得失的电子数
当温度为298K时,将各常数值代入式(6-2),并将自然对数转换成常用对数,能斯特方程式可改写为:
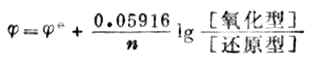 (6-3)
(6-3)
应用能斯特方程式时,应注意以下几点:
1.若电极反应式中有纯固体、纯液体或介质水时,它们的浓度不列入方程式中;气体物质用分压,即101.325kPa的倍数表示。
2.若电极反应式中氧化型、还原型物质前的系数不等于1时,则在方程式中它们的浓度项应以对应的系数为指数。
3. 氧化型、还原型物质包括与它们同存在的有关物质。例如, ,[氧化型]=[MnO4-][H+]8。
(二)有关能斯特方程式的计算
1.计算电极电位
利用能斯特方程式,可以计算不同条件下的电极电位值。
例4 计算298K,锌离子浓度为0.01mol.L-1时,Zn2+│Zn电极的电极电位。
解:电极反应
![]()
已知n=2,[Zn2+]=0.01mol.L-1,![]()
(Zn2+/Zn)=-0.7628V,则,
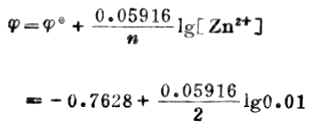
=-0.7628-0.05916
=-0.822(V)
在此例中,由于[Zn2+]<1mol.L-1,所以![]()
![]()
。若金属离子浓度愈小,则金属的电极电位愈低表明还原剂失电子的倾向增强了。
例5 计算298K时,Pt│Fe3+(mol.L-1),Fe2+(0.001mol.L-1)电极的电极电位。
解: 电极反应:
![]()
已知n=1,[Fe3+]=1mol.L-1,[Fe2+]=0.0001mol.L-1,![]()
(Fe3+/Fe2+)=0.77V,则
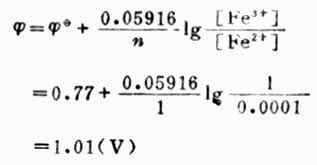
从本例中可以看出,氧化型离子浓度愈大,或还原型离子愈小,电极电位愈高,表明氧化型得电子的倾向愈大。也就是说电极电位随着氧化型物质浓度增大而升高,随着还原型物质浓度增大而降低。
例6 求电极反应
![]()
在pH=5溶液中的电极电位(其他条件同标准状态)。
解:已知n=5,[MnO4+-]=[Mn2+]=1mol.L-1,[H+]=10-5mol.L-1,![]()
(MnO4-/Mn2+)=+1.491V,则
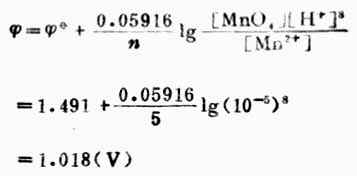
计算结果表明,[H+]降低,对应的氧化型物质(MnO4-)的氧化能力降低。
2.判断原电池的正、负极,计算电动势
通常组成原电池的各有关物质并不是处于标准状态。计算原电池的电动势,首先根据标准电极电位表,利用能斯特方程计算出标准状态下各电极的电极电位。然后根据电极电位的高低判断正、负极,把电极电位高的电极作正极,电极电位低的电极作负极。正极的电极电位减去负极的电极电位即得原电池的电动势。
例7 计算298K时,电池Cu│Cu2+(0.1mol.L-1)‖Fe2+(0.1mol.L-1);Pt的电动势,并说明它是否按惯例书写正负极,列出电池反应式。
解:从表6-1中查出电极反应式及标准电极电位:
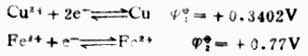
根据能斯特方程式,分别计算它们在非标准状态下的电极电位。

计算结果表明,电池右侧是正极,左侧是负极。该原电池是按惯例书写的。原电池的电动势为:
E=![]()
右-![]()
左=0.83-0.31=0.52(V)
电极反应 负极 Cu→Cu2++2e-(氧化反应)
正极 Fe3++e- →Fe2+(还原反应)
电池反应 Cu+2Fe3+→Cu2++2Fe2+
例8 计算298K时,电池Pt│I2,I-(0.1mol.L-1)‖MnO4-(0.1mol.L-1),Mn2+(0.1mol.L-1),H+(0.01mol.L-1)│Pt的电动势并写出电池反应式。
解:由表6-1中查出电极反应式及标准电极电位:
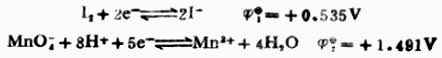
根据能斯特方程式,分别计算非标准状态下的电极电位。

计算表明,电池右侧电极的电极电位高为正极,左侧电极电位低为负极。所以,
E=![]()
右-![]()
左=1.195-0.594
=0.601(V)
电极反应 2I-→I2+2e-(氧化反应)
正极MnO-4+8H++5e-→Mn2++4H2o (还原反应)
电池反应 2MnO-4+10I-+16H+→2Mn2++5I2+8H2O
第三节 电极电位的应用
一、判断氧化还原反应自发进行的方向
电池反应都是自发进行的氧化还原反应。因此电池反应的方向即氧化还原反应自发进行的方向。判断氧化还原反应进行的方向时,可将反应拆为两个半反应,求出电极电位。然后根据电位高的为正极起还原反应,电位低的为负极起氧化反应的原则,就可以确定反应自发进行的方向。如果两个电对的![]() 值相差较大(即Eφ),浓度的变化对电位的影响不大,不致于使反应改变方向。因此,当Eφ<0.2V 时,即使不处于标准状态,也可直接用
值相差较大(即Eφ),浓度的变化对电位的影响不大,不致于使反应改变方向。因此,当Eφ<0.2V 时,即使不处于标准状态,也可直接用![]() 值的大小确定反应方向。否则,必须考虑浓度和酸度的影响,用能斯特方程式计算出电对的
值的大小确定反应方向。否则,必须考虑浓度和酸度的影响,用能斯特方程式计算出电对的![]() 值,用E>0作为判断确定反应进行的方向,若E>0,正向反应能自发进行;E<0,正向反应不能自发进行,其逆向反应能自发进行。
值,用E>0作为判断确定反应进行的方向,若E>0,正向反应能自发进行;E<0,正向反应不能自发进行,其逆向反应能自发进行。
例9 判断298K时下列反应进行的方向:
![]()
解:将上述反应写成两个半反应,并查出它们的标准电极是位:
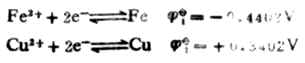
标准电动势为:Eφ=![]()
2-![]()
1=0.4402-(-0.4402)
=0.7804(V)。
因为Eφ<0.2V,可直接用![]()
值判断反应进行的方向。![]()
2>![]()
1,表明Cu2+是比Fe2+更强的氧化剂,Fe是比Cu更强的还原剂所以上述反应可自发地向右进行。
为了证明这个结论的正确性,我们可以按非标准态的电池反应计算电动势。
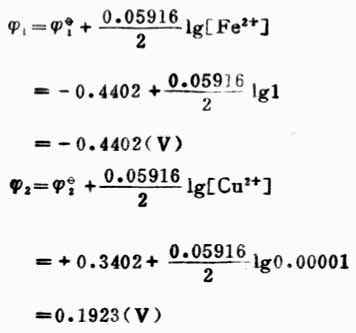
电池电动势为:E=![]()
2-![]()
1=0.1923-(-0.4402)
=0.6325(V)
因为E<0,上述反应可自发地向右进行。
例10 判断298K时反应
![]()
当[HAsO2]=[H3AsO4]=1mol.L-1,[I-]=1mol.L-1,在中性和酸性([H+]=1mol.L-1)溶液中反应进行的方向。
解:将上述反应写成两个半反应,并查出它们的标准电极电位:
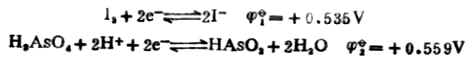
在中性溶液中,[H+]=1.0*10-71mol.L-1。
![]()
1=![]()
1=+0.535V
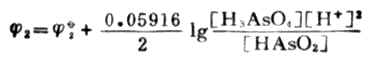
=0.559+0.059161g[H+]
=0.559+0.059161g10-7
=0.559+0.414
=0.145(V)
因为![]()
1![]()
2,所以I2是比H3AsO4更强的氧化剂,而HAsO2是比I-更强的还原
剂。因而上述反应能自发地向右进行。即
HAsO2+I2+2H2O→H3AsO4+2I-+2H+
当溶液中氢离子浓度为1mol.L-1时,
![]()
1=![]()
1=+0.535V
![]()
2=![]()
2=+0.559V
因为![]()
1<![]()
2,所以H3AsO4是比I2更强的氧化剂,而I-更强的还原剂。因而上
述反应能自发地向右进行。即
H3AsO4+2I-+2H+→HAsO2+I2+2H2O
二、判断氧化还原反应进行的程度
氧化还原反应属可逆反应,同其他可逆反应一样,在一定条件下也能达到平衡。随着反应不断进行,参与反应的各物质浓度不断改变,其相应的电极电位也在不断变化。电极电位高的电对的电极电位逐渐降低,电极电位低的电对的电极电位逐渐升高。最后必定达到两电极电位相等,则原电池的电动势为零,此时反应达到了平衡,即达到了反应进行的限度。利用能斯特方程式和标准电极电位表可以算出平衡常数,判断氧化还原反应进行的程度。若平衡常数值很小,表示正向反应趋势很小,正向反应进行得不完全;若平衡常数值很大,表示正向反应可以充分地进行,甚至可以进行到接近完全。因此平衡常数是判断反应进行程度的标志。
氧化还原K与反应中两个电对的标准电极电位的关系为:
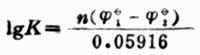 (6-4)
(6-4)
式中,n—反应中得失电子数;
![]()
1—正反应中作为氧化剂的电对的标准电极电位;
![]()
2—正反应中作为还原剂的电对的标准电极电位。
由式(6-4)可见,![]()
1与![]()
2之差值愈大,K值也愈大,反应进行得也愈完全。
例11 计算下列反应在298K时的平衡常数,并判断此的以应进行的程度。
![]()
解: 电极反应Ag++e-→1=+0.7996V
Fe2+→Fe3++e-2=+0.77V
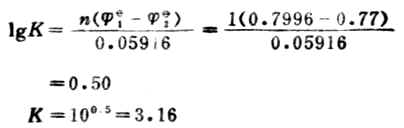
此反应平衡常数很小,表明此正反应进行得很不完全。
例12 计算下列反应的298K时的平衡常数,并判断此反应进行的程度。
![]()
解:
电极反应 Cr2O72-+14H++6e-+→2Cr3+7H2O
![]()
1=+1.33V
2I-→I2+2e-![]()
1=+0.535V
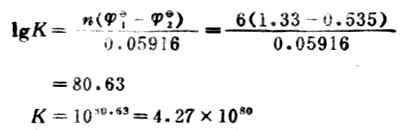
此反应的平衡常数很大,表明此正反应能进行完全,实际上可以认为能进行到底。
例13 向0.45mol.L-1铅盐溶液中加锡,发生下列反应,
![]()
计算298K时反应的平衡常数,达到反应限度时溶液中Pb2+浓度为多少。
解:
电极反应:Pb2++2e-→Pb![]()
1=-0.1263V
Sn→Sn2++2e-![]()
2=-0.1364V
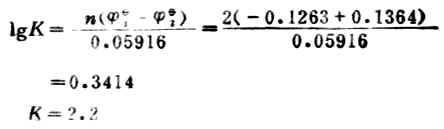
设平衡(达到反应限度)时溶液中Pb2+浓度为χmol.L-1。
![]()
χ 0.45-χ
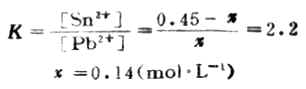
即达到反应限度时溶液中Pb2+浓度为0.14mol.L-1。
三、 电位法测定溶液的PH值
如果有H+或OH-参加电极反应,则H+浓度对电极电位会有影响。把这个电极作为指示电极和一个参比电极组成电池,测定电池电动势,就可以算出指示电极的电位,溶液中H+浓度即溶液的PH值。
所谓指示电极就是这一电极的电位与溶液中某种离子浓度的关系符合能斯特方程式。从它所显示的电位可以推算出溶液中这种离子的尝试通常把这种电极看作是待测离子的指示电极。测定溶液的PH值,就是测定溶液中H+浓度,因此要采用氢离子指示电极。所谓参比电极是指电极电位稳定且已知其准确数值的电极。
(一)参比电极
测定溶液的PH值常用饱和甘汞电极作为参比电极。
饱和甘汞电极的构造如图6-4所示。饱和甘汞电极由两个玻璃套管组成。内管上部为汞,连接电极引线。在汞的下方充填甘汞(HgCL2)和汞的糊状物。内管的下端用石棉或脱脂棉塞紧。外管上端有一个侧口,用以加入饱和氯化钾溶液,不用时侧口用橡皮塞塞紧。外管下端有一支管,支管口用多孔的素烧瓷塞紧,外边套以橡皮帽。使用时摘掉橡皮帽,使与外部溶液相通。
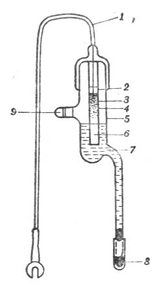
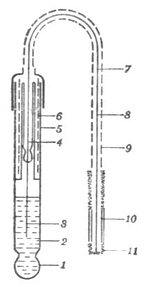
图6-5 玻璃电极
图6-4 饱和甘汞电极1.玻璃球膜,2.缓
1.电极引线 2.玻璃管,3.汞,4.甘示糊 冲溶液,3.银-氯化银电极,
(Hg2Cl2和Hg研成的糊),5.玻璃外套,6. 4.电极导线,5.玻璃管,6.
石棉或纸浆,7.饱和KCl溶液,8.素烧瓷 静电隔离层,7.电极导线,8
,9.小橡皮塞 .金属隔离罩,10.塑料绝缘
线,11.电极接头
饱和甘汞电极的组成式为:
KCl(饱和),Hg2Cl2(固),Hg(l)│Pt
其电极反应式为:
![]()
根据能斯特方程式,298K时电极电位为:
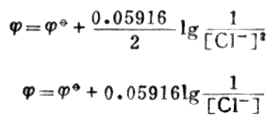
式中![]()
值是定值,在饱和溶液中[CL-]也为定值,故饱甘汞电极的电极电位为定值,298k 时为0.2412V。
饱和甘汞电极的电位稳定,再现性好,而且装置简单,容易保养,使用方便,因此广泛地用作参比电极。
(二)指示电极
常用的PH指示电极为玻璃电极。
玻璃电极的构造如图6-5所示。在玻璃管的下端连接一个厚度为50-100um的半球形玻璃膜。膜内盛有0.1mol ·L-1盐酸称参比溶液。在参比溶液中插入一根镀有氯化银的银丝,构成氯化银电极,为内参比电极。氯化银电极的电极反应为:
![]()
电极电位的能斯特方程式为:
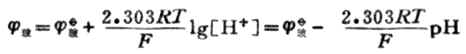
将氯化银电极的银丝与导线相连即构成玻璃电极。玻璃电极可表示为:
Ag,AgCl(s)│HCl(mol.L-1)│玻璃膜│待测溶液(H+)
因为玻璃电极内充液中CL-浓度为一常数,故内参比电极的电极电位值也为常数。
玻璃电极在使用前应先在蒸馏水中浸泡12-24h,使玻璃膜外侧硅酸盐层吸水膨润形成一层水化凝胶层。玻璃膜内侧浸泡在盐酸中,也形成一层水化凝胶层。
当将浸泡过的玻璃电极插入具有一定PH值的待测溶液中时,在玻璃膜外侧溶液中氢离子与膜外水化凝胶层中钠离子进行交换。玻璃膜内侧参比溶液中的氢离子与膜内水化凝胶层中钠离子进行交换。当膜两侧H+浓度不同,离子交换达到平衡时,由于离子交换速度和扩散速度不同而出现了电位差。这种电位差称为膜电位。由于膜内参比溶液的氢离子浓度为定值,所以膜电位仅由膜外溶液的氢离子浓度决定。膜电位值与H+浓度的关系符合能斯特方程。
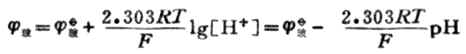
式中![]()
玻值与内参比电极的电极电位、膜内溶液的H+浓度以及膜表面状态有关。在一定条件下,每一个玻璃电极的![]()
玻为常数.
(三)电位法测定溶液的PH值
电位法测 定溶液的PH值常用饱和甘汞电极作参比电极,玻璃电极作指示电极,置于待测溶液中组成如下电池。
Ag│AgCl(s),Cl-(0.1mol.L-1),H+(0.1mol.L-1)│玻璃膜│待测pH溶液 ‖KCL(饱和),Hg2Cl2(s)│Hg(1
测出的电动势为饱和甘汞电极和玻璃电极的电位差值,即
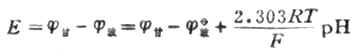
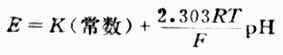
上式为溶液PH值与电池电动势的关系式。测出E值值后,若是不知道常数K的数值,还是不能算出PH值。因此要先用已知PH值为PHs的标准缓冲溶液进行测测定,测出电动势为Es,则可得关系式为:
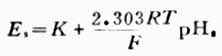 (6-6)
(6-6)
求出K值,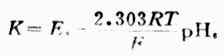
将电池装置中的标准缓冲溶液换成待测pHx的溶液,测出电动势为Ex,则
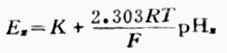 (6-7)
(6-7)
将式(6-7)代入式(6-8)得:
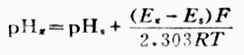 (6-9)
(6-9)
式中PHs 为已知数、Ex和 Es为先后两次测出的电动势,F,R,T为常数,故可根据式(6-9)计算出待测溶液的PH值。
第七章 滴定分析
分析化学是研究物质组成的测定方法与有关原理的一门科学。它分为定性分析和定量分析两在部分。定性分析的任务是确定物质的组成成分;定量分析的任务是在定性分析的基础上进一步确定各组成成分的相对含量。
定量分析通常可分为化学分析和仪器分析。化学分析是以物质化学性质为基础的分析方法,它包括重量分析和滴定分析。仪器分析是以物质的物理或物理化学性质为基础,应用特殊的检验仪器进行分析的方法。
滴定分析由于其简便、快速等特点且有足够的准确度,不仅在化学、化工领域有很大的实用性,医药卫生等工作中也有广泛的应用。
第一节 滴定分析概念
一、滴定分析的特点和方法
滴定分析是通过“滴定”来实现的一种分析方法。在滴定过程中,使用的已知准确的溶液称为标准溶液,被滴定的溶液叫做试样溶液。当标准溶液与被测组成的反应恰好完全时,即为反应的理论终点,称为化学计量点附近发生的、容易观察到的变化来确定。若反应本身无此种变化,就须借助指示剂。指示剂所指示的反应终点称为滴定终点。
滴定分析法是基于标准溶液与被测组分之间发生化学反应时,它们的量之间存在一定的化学计量关系,利用标准溶液的浓度和所消耗的体积来计算被测物质含量的一种方法。根据分析时所利用的化学反应不同,滴定分析又分为酸碱滴定法,氧化还原滴定法,配合滴定法和沉淀滴定法。
值得注意的是,并非所有的反应都可用于滴定分析,适合滴定分析的反应必须满足以下条件:第一,该反应必须按一定的反应式进行,即必须具有确定的化学计量关系;第二,反应必须能够定量地进行,通常要求达到99.9%以上;第三,必须有适当的方法确定反应的终点。此外要求反应能较快地进行。对于速度较慢的反应有时可通过加热或加入催化剂来加速反应。
二、滴定分析的操作程序
(一)标准溶液的配制
1.直接配制法
直接称取一定量的基准物质,溶解后转入容量瓶中,稀释定容。根据溶质的量和溶液的体积可计算出该溶液的准确浓度。
所谓基准物质是指那些能够直接用来配制溶液的物质。它们必须符合下列条件:
(1)物质的组成应与化学式相符。若含结晶水,其结晶水的含量也应与化学式相符。
(2)试剂要纯度高。一般含量在99.9%以上。
(3)试剂要稳定。如不易吸收空气中的水分及二氧化碳,不易被空气氧化等。
(4)有比较大的摩尔质量,以减少称量所引起的相对误差。
常用的基准物质有邻酸氢钾、草酸、碳酸钠等。
2.间接配制法
由于大多数试剂不能满足基准物质的条件,也就不能直接用来配制标准溶液。这时可先将它们配成近似所需浓度的溶液,再用下述方法标定其浓度,这种方法称为间接配制法。
(二)标准溶液浓度的标定
标定是指用滴定方法确定溶液准确浓度的过程。可以用待标定溶液一定量的基准浓度,亦可以用待标定溶液和已知准确浓度的标准溶液进行相互滴定,比较出待测溶液的浓度。例如,欲标定盐酸溶液的浓度,可称取一定量的分析纯碳酸钠(基准物质)溶于水中,然后用此盐酸溶液进行滴定:
2HCL+Na2CO3→2NaCL+H2O+CO2
当反应完全时,从用去此盐酸溶液的体积和碳酸钠的质量,即可求出盐酸溶液的准确浓度。
(三)被测物质含量的测定
标准溶液的浓度确定后,即可对待测物质进行含量测定。例如,已标定的盐酸溶液可以用来测定某些碱性物质含量;已标定的氧化剂溶液可以用来测定某些还原性物质相对含量。
三、滴定分析的计算方法
(一)方向方法
滴定分析中的计算主要包括标准溶液浓度的计算和被测定物质含量的计算。标准溶液的浓度常用物质的量浓度表示。物质B的浓度即可用下式求得:
cB=nB/Vb (7-1)
或 cBVB=mB/MB(7-2)
在上面式子中,mb 为物质B的质量(g);MB 为物质B的摩尔质量(g˙mol-1);VB为物质B溶液的体积(L);cB即为物质B的量浓度(mol˙L-1)。
对于任一滴定反应:
aA+bB=dD+eE
若选取aA和bB作为基本单元,则有如下关系:
n(aA)=n(bB)(7-3)
上式表示:当达到化学计量点时,aA与bB的物质的量相等,即等物质的量规则。该规则是进行滴定分析计算的主要根据之一,由式(7-1)和式(7-3)得:
c(aA)˙V(A)=c(bB)˙V(B)
在实际工作中,为方便起见,常将A和B选作基本单元。
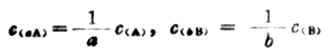
故式(7-4)又可写成:
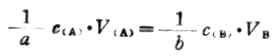
式(7-2)和(7-5)是滴定分析中两个常用的计算式,下面通过实例介绍它们的应用。
例1 准确称取基准物质K2Cr2O72.4530g,溶解后移入500ml容量瓶中,加水稀释至刻度。求c(K2Cr2O7)和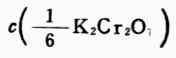 。
。
解:K2Cr2O7的摩尔质量为294.2g.mol-1
故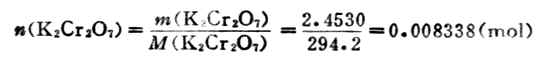
则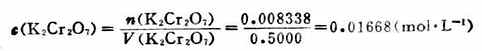
![]()
例2 称取分析纯Na2CO31.2738g,溶于水后稀释成250mL,取该溶液25.00mL,用HCl溶液进行滴定,以甲基橙为指示剂。当达终点时,用去HCl溶液24.80mL,求此溶液的准确浓度。
解:滴定反应为
Na2CO3+2HCl→2NaCl+CO2+H2O
由式(7-5)得
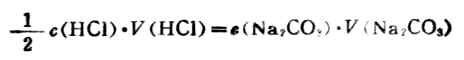
因为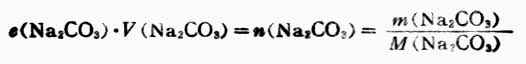
所以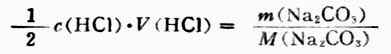
在上式中溶液的体积是以升为单位,若体积V指定以毫升为单位,则上式可化为
则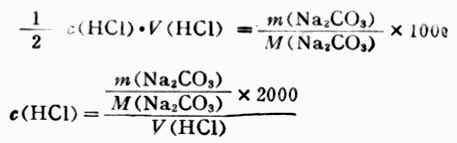
在25.00mL Na2CO3溶液中Na2CO3的质量为:
所以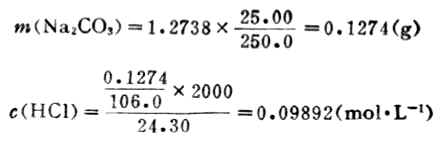
例3 称取草酸0.1670g溶于适量的水中,用0.1000mol.L-1的NaOH标准溶液滴定,用去23.46mL,求样品中H2C2O4.2H2O的质量百分数。
解:滴定反应为
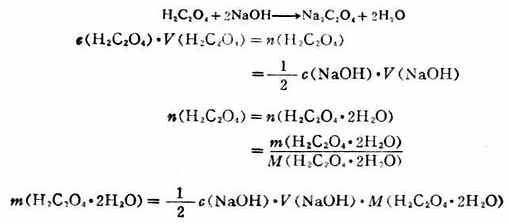
则草酸的质量百分数:
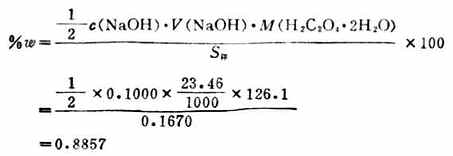
(二)有效数字和计算规则
有效数字是指实际上能测量到的数值,在该数值中只有最后一位是可疑数字,其余的均为可靠数字。它的实际意义在于有效数字能反映出测量时的准确程度。例如,用最小刻度为0.1cm的直尺量出某物体的长度为11.23cm,显然这个数值的前3位数是准确的,而最后一位数字就不是那么可靠,因为它是测试者估计出来的,这个物体的长度可能是11.24cm,亦可能是11.22cm,测量的结果有±0.01cm的误差。我们把这个数值的前面3位可靠数字和最后一位可疑数字称为有效数字。这个数值就是四位有效数字。
在确定有效数字位数时,特别需要指出的是数字“0”来表示实际测量结果时,它便是有效数字。例如,分析天平称得的物体质量为7.1560g,滴定时滴定管读数为20.05mL,这两个数值中的“0”都是有效数字。在0.006g中的“0”只起到定位作用,不是有效数字。
在计算中常会遇到下列两种情况:一是化学计量关系中的分数和倍数,这些数不是测量所得,它们的有效数字位数可视为无限多位;另一种情况是关于pH、pK和lgK等对数值,其有效数字的位数仅取决于小数部分的位数,因为整数部分只与该真数中的10的方次有关。例如,pH=13.15为两位有效数字,整数部分13不是有效数字。若将其表示成[H+]=7.1×10-14,就可以看出13的作用仅是确定了[H+]在10-14数量级上,其数学意义与确定小数点位置的“0”相同。
在滴定分析中,实验数据的记录只应保留一位可疑数字,结果的计算和数据处理均应按有效数字的计算规则进行。
在进行加减运算时,有效数字取舍以小数点后位数最少的数值为准。例如,0.0231、24.57和1.16832三个数相加,24.57的数值小数点后位数最少,故其他数值也应取小数点后两位,其结果是
0.02+24.57+1.17=25.76
在乘除运算中,应以有效数字最少的为准。例如,0.0231、24.57和1.16832三个数相乘,0.0231的有效数字最少,只有3位,故其他数字也只取3位。运算的结果也保留3位有效数字:
0.0231×24.6×1.17=0.665
在对数运算中,所取对数的位数应与真数的有效数字位数相同。例如,lg9.6的真数有两位有效数字,则对数应为0.98,不应该是0.982或0.9823。又如[H+]为3.0×10-2mol·L-1时,PH应为1.52。
正确运用有效数字规则进行运算,不但能够反映出计算结果的可信程度,而且能大大简化计算过程。在滴定分析中一般常采用四位有效数字。
四、滴定分析的误差
(一)误差及其来源
在滴定分析中,分析结果的准确度常用误差来表示。误差是测量值与真实值之间的差异,它反映出分析结果与真实值间的符合程度。努力减少测量误差,提高分析结果的准确性是定量分析中的一项重要课题。
滴定分析中最常见的误差有系统误差和偶然误差。
1.系统误差
系统误差是由某些必然的或经常的原因造成的。其来源有方法误差,仪器、试剂误差及操作误差等。系统误差对分析结果的影响有一定的规律性,在重复测量时误差的大小常常比较接近,并且会反复出现。与理论值相比,实验值要么都提高,要么都偏低。系统误差常用作空白试验和对照实验的方法消除或克服。
在不加试样的情况下,按照样品分析步骤和条件进行分析试验称为空白试验,所得结果称为空白值。从试样测定结果中扣除空白值,便可以消除因试剂、蒸馏水及实验仪器等因素引起的系统误差。
将组分含量已知的标准样品和待测样品在相同条件下进行分析测定。用标准样品的测定值与其真实值的差值来校正其他测量结果,这种方法称为对照试验。
除此之外,还可以通过校准仪器来消除仪器误差,通过制订正确的操作规程克服操作误差。
2.偶然误差
偶然误差是由一系列微小变化的偶然原因造成的。例如,称量同一物体时,室温或湿度如有微小变动都会引起偶然误差,使得称量结果不一致。这种误差大小不定,时正时负,往往找不出确定的原因,因些很难控制、校正和测定它。但偶然误差符合统计规律,表现为正负误差出现的机会相等,小误差出现的机会多而大误差出现的机会少。因此,在消除了系统误差的前提下,可以通过增加测定次数取平均值的办法克服偶然误差。
(二)误差与准确度
准确度指实验测定值(X)与真实值(T)之间的符合程度,常用误差的大小来衡量。误差的绝对误差和相对误差。绝对误差指测定值与真实值之间的差值,用“E”来表示。相对误差指的是绝对误差占真实值的百分率,用“%RE”表示。即
绝对误差:E=X-T
相对误差:(%)RE=E/T×100
误差越小,表示实验结果与真实值越接近,测定的准确度也越高。而与绝对误差相比,相对误差更能反映出实验结果的准确程度。因此在滴定分析中一般多采用相对误差来表示测量的准确度。
(三)偏差与精密度
在实际工作中真实值往往是不知道的,此时便不好用误差来评价分析结果,通常用相同条件下多次测定结果的平均值(X) 来代替真实值,用偏差来衡量所得结果的精密试。
精密度指多次重复测定的结果相互接近的程度,是保证准确度的前提。偏差是指各次测定的结果和平均值之间的差值。偏差越小,精密度越高。
偏差分为绝对偏差(d)、相对偏差(Rd)、平均偏差(d)和相对平均偏差 (Rd),它们的表达式为:
绝对偏差![]()
相对偏差![]()
平均偏差![]()
相对平均偏差![]()
式中d1,d2…dn为第1,2…n次测量结果的偏差,X为单次测定值,x为测定平均值。
对于一般的滴定分析来讲,因测定次数不多,故常用相对平均偏差来表示实验的精密度。
第二节 酸碱滴定法
酸碱滴定法是以酸碱反应为基础的滴定分析方法。利用该方法可以测定一些具有酸碱性的物质,也可以用来测定某些能与酸碱作用的物质。有许多不具有酸碱性的物质,也可通过化学反应产生酸碱,并用酸碱滴定法测定它们的含量。因此,在生产和科研实践中,酸碱滴定法的应用相当广泛。
一、滴定曲线与指示剂的选择
(一)强碱滴定强酸
强碱滴定强酸时发生的反应为
![]()
上述反应的平衡常数为Kt为
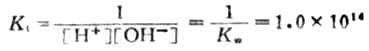
现以0.1000mol·L-1NaOH溶液滴定20.00mL,0.1000mol·L-1HCL.溶为例,讨论滴定过程中溶液pH值的变化情况。
1.滴定前
溶液[H+]等于HCL的初始浓度:
[H+]=c(HCl)=0.100mol.L-1
pH=-lg[H+]=1.00
2.化学计量点前
溶液的[H+]决定于剩余HCL的浓度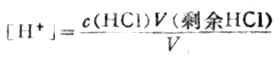
例如,当滴入18.00mLNaOH溶液时,有90%的HCL被中和,剩余HCL物质的量为0.1000×20.00-0.1000×18.00=0.2000mmol,此时溶液的总体积为38.00mL,则溶液的[H+]为:
[H+]=0.2000/38.00=5.3*10-3(mol.L-1)
pH=-lg[H+]=-lg5.3*10-3=2.28
用类似的方法可求得当加入19.98mL NaOH时溶液的PH值为4.30。
3.化学计量点时
当加入20.00mLNaOH溶液时,HCL溶液被100%的中和,变成了中性的NaCL水溶液,故溶液的PH值由水的离解决定。
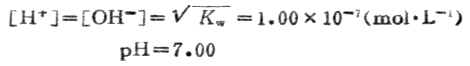
4.化学计量点后
溶液的PH值由过量的NaOH的量和溶液的总体积决定。即
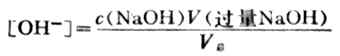
例如,当加入20.02ml NaOH溶液时, NaOH溶液过量0.02ml,溶液的总体积为40.02ml,则溶液的[OH-]为:
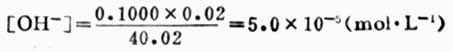
pOH=4.30
pH=14.00-4.30=9.70
根据上述方法可以计算出不同滴定点时溶液的PH值,部分结果列于表7-1。根据表中的数据作图,即可得到强碱滴定强酸的滴定曲线图7-1中的a。
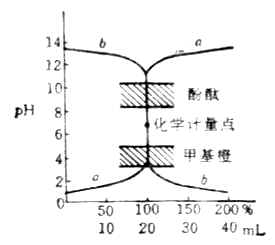
图7-1 NaOH与HCL的滴定曲线
c(NaOH)=c(HCl) =0.1000mol.L-1
图7-1
表7-1 用NaOH滴定HCL时溶液PH的变化(c(NaOh )=c(HCL)=0.1000mol·L-1)
| V(加入NaOH) ml |
被滴定HCL的百分含量% | V(剩余HCL) ml |
V(过量NaOH) ml |
[H3O+] mol·L-1 |
PH |
| 20.00 | 1.00×10-1 | 1.00 | |||
| 19.00 | 90.00 | 2.00 | 5.26×10-3 | 2.28 | |
| 19.80 | 99.00 | 0.20 | 5.02×10-4 | 3.30 | |
| 19.98 | 99.90 | 0.02 | 5.00×10-5 | 4.30 | |
| 20.00 | 100.00 | 0.00 | 1.00×10-7 | 7.00 | |
| 20.02 | 100.1 | 0.02 | 2.00×10-10 | 9.70 | |
| 20.20 | 101.0 | 0.20 | 2.01×10-11 | 10.70 |
滴定曲线不仅说明了滴定时溶液PH值的变化方向,而且也说明了各个阶段的变化速度。从图中可以看出,曲线自左至右明显分成三段。前段和后段比较平坦。溶液的PH值变化缓慢,中段曲线近乎垂直。在化学计量点附近PH值有一个突变过程。这种PH值突变称之为滴定突跃,突跃所在的PH值范围称为滴定突跃范围(常用化学计量点前后各0.1%的PH范围表示,本例的突跃范围是(4.30-9.70)。
最理想的指示剂应该能恰好在反应的化学计量点发生颜色变化,但在实际工作中很难使指示剂的变色范点和化学计量点完全统一。因此,指示剂的选择主要以滴定的突跃范围为依据,通常选取变色范围全部或部分处在突跃范围内的指示剂滴定终点,这样产生的疑点误差不会超过±0.1%。在上述滴定中,甲基橙(PH3.1-4.4)和酚酞(PH8.0-10.0)的变色范围均有一部分在滴定的突跃范围内,所以都可以用来指示这一滴定疑点此外,甲基红、溴酚蓝和溴百里酚蓝等也可用作这类滴定的指示剂。
滴定突跃的大小与溶液的浓度密切相关。若酸碱浓度均增大10倍,滴定突跃范围将加宽2个PH单位;反之,若酸碱浓度减小10倍,相应的突跃范围将减小2个PH单位。可见浓度愈高突跃范围越大,浓度越低突跃范围越小,如果滴定时所用的酸碱浓度相等并小于2×10-4mol ·L-1,滴定突跃范围就会小于0.4个PH单位,用一般的指示剂就不能准确地指示出终点。故将c≥2×10-4mol ·L-1作为此类滴定能够准确进行的条件。
强酸滴定强碱的滴定曲线如图7-1中的曲线b所示。指示剂的选择及滴定反应用及其滴定条件等与前述滴定相似。
(二)强碱滴定弱酸
在这类滴定反应中,由于强碱完全离解而弱酸(HA)部分离解,故滴定反应及其反应常数Kt可表述为:
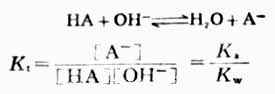
同强碱滴定强酸的反应常数相比较,上述的Kt值要小得多,说明反应的完全程度较前类滴定差。且弱酸的Ka越大,反应的完全程度就越高。
现以0.1000 mol ·L-1NaOH溶液滴定20.00ml0.1000 mol ·L-1HOAc溶液为例讨论这类滴定的特点。
NaOH 滴定HOAc 的滴定曲线如图7-2所示。它和强碱滴定强酸的滴定曲线不同。首先是曲线起始点的PH值为2.87而非1.00。这是由于HOAc 部分离解,其[H+]=√ KaC的结果。其次是起始点至化学计量点前这段曲线先较快地上升,后转入平衡,在临近终点时又较快地上升。这是HOAc –NaOAc缓冲对缓冲作用的表现。在滴定开始后,反应产生的OAc-抑制了HOAc的离解,使得[H+]有较快地下降,PH值上升较明显。当[HOAc]/[ NaOAc]=1时,该缓冲体系的缓冲能力最大,曲线平坦。继续加入NaOH,缓冲能力下降,PH值的上升速度又增加。近化学计量点时几乎无缓冲作用,故PH值上升较快。第三是化学计量点时溶液的PH=8.73,这是NaOAc水解的结果。此外,在化学计量点附近产生的滴定突跃范围明显小于强碱滴定强酸所产生的突跃范围。在化学计量点后,过量的NaOH存在抑制了盐的水解,溶液的PH值由过量的NaOH决定。故滴定曲线与强碱滴定强酸的滴定曲线相似。
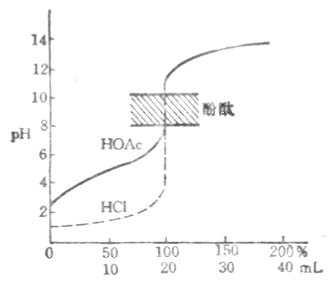
图7-2 用NaOH滴定HOAc的滴定曲线c
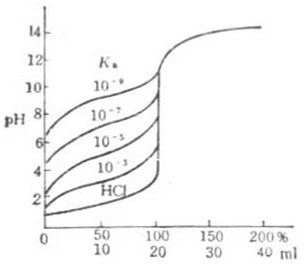
图7-3 NaOH滴定各种不同强并能弱
(NaOH)=c(HOAc)=0.100mol.L-1c(NaOH)=c(HB)=0.1000mol.L-1
根据强碱滴定弱酸时PH值的变化,一般选用变色范围处于碱性范围内的指示剂。较常用的有酚酞和百里酚蓝等。在实际应用时,仍必需依据滴定的突跃范围大小来决定指示剂。
滴定的突跃范围不仅与酸碱浓度有关,还受到弱酸强度的影响。因此在进行此类滴定时必须考虑这两个因素。图7-3是用0.1000mol ·L-1NaOH溶液滴定20.00ml0.1000 mol ·L-1各种不同强度弱酸的滴定曲线.当弱酸的浓度一定时,Ka越大,滴定的突跃范围越大;Ka越小滴定的突跃范围就越小。当c(HB)=0.1000mol ·L-1时,Ka≤10-9,已无明显的滴定突跃,也无法用一般的指示剂确定反应终点。只有当cKa≥10-8时方可用指示剂判别滴滴定突跃(约0.4个PH单位),所以常将c Ka≥10-8作为弱酸能被强碱准确滴定的先决条件。
(三)强酸滴定弱碱
强酸滴定弱碱与强碱滴定弱酸相类似,现以0.1000mol ·L-1HCL溶液滴定20.00ml0.1000 mol ·L-1氨水为例,说明滴定过程中PH值的变化及指示剂的选择.上述滴定的反应和反应常数可表述为:
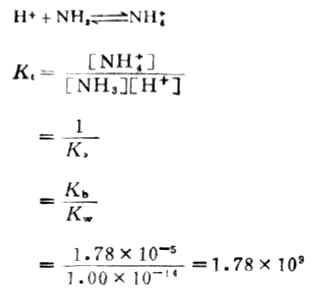
该反应的反应常数较大,可以预计反应能较完全进行.各滴定点PH值可通过计算求得滴定曲线如图7-4。由图可以看出,强酸滴定弱碱时,滴定突跃在酸性范围内,化学计量点时,溶液的PH值小于7.00,对于该例来说,化学计量点时溶液的PH值为5.28,突跃范围是6.25-4.30。对于这种类型滴定所选指示剂的变色范围应在酸性范围内。甲基红或溴甲酚绿是这类滴定中常用的指示剂。
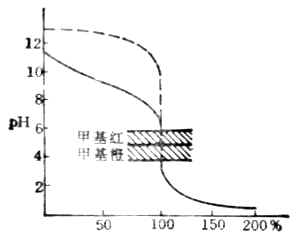
图7-4 用HCl滴定NH3.H2O的滴定曲线c(HCl)=c(NH3.H2O)
=0.1000mol.L-1
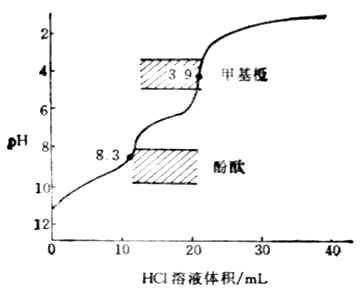
图7-5 HCl滴定Na2CO3的滴定的曲线
在强酸滴定弱碱时,弱碱的Kb值与浓度也应满足cKb≥10-8的条件,方可进行准确滴定。
(四)多元酸盐的滴定
能够用于滴定的多元酸盐一般为强碱弱酸盐,因为它们水解使溶液呈碱性,故可用强酸进行滴定。
Na2CO3是二元弱酸H2CO3的钠盐,由于H2CO3的两级离解常数都很小,CO2-3、HCO-3水解后溶液的碱性足以用HCL直接滴定。因此,常将Na2CO3作为基准物质标定HCL溶液的浓度,工业碱纯度的测定也是基于它与HCL反应。
滴定反应分两步进行,在第一步时Na2CO3全部转变为Na2CO3。
Na2CO3+HCl→NaHCO3+NaCl
所以到达第一化学计量点时,溶液的PH值主要由NaHCO3决定,可按下式计算溶液的酸度:
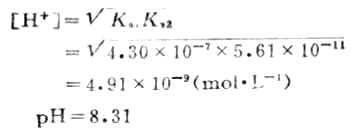
继续用HCL溶液滴定时,发生第二步滴定反应,NaHCO3全部变成H2CO3而达到第二化学计量点:
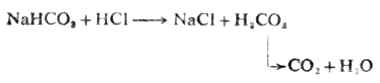
这时的溶液为H2CO3的饱和溶液,在通常的情况下为0.04mol·L-1,则第二化学计量点时溶液的[H+]为:
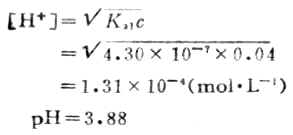
滴定过程中溶液的PH值的变化如图7-5所示。
在PH为8.31和3.88附近各有一个滴定突跃。前一个突跃不大明显,这是由于第一步滴定反应的产物NaHCO3具有一定的缓冲作用以及碳酸的Ka1和Ka2相差不太大的缘故。这步滴定的指示剂常选用酚酞。第二个突跃范围较明显,通常用甲基橙指示剂。终点前溶液中H2CO3能与HCO-3组成缓冲体系,终点不易掌握。故在实际操作时,当反应接近第二化学计量点前,采用加热或不断振摇的办法驱逐溶液中的CO2,这样可以得到较为准确的滴定终点。
二、酸碱滴定法的应用实例
在实际工作中常用的酸溶液主要是HCL溶液,有时也用H2SO4标准溶液。常用的碱溶液是NaOH标准溶液。由于这些试剂价廉易得,加之酸碱滴定法操作简便,分析速度快和结果准确。因而在工农业生产及科学实践中得到广泛应用。在临床检验上常用以测定尿液、胃液及其他体液的酸度。在卫生分析方面也常用以测定各种食品的酸度等。下面介绍一些实例。
(一)食醋中总酸度的测定
食醋约含3%-5%的HOAc,此外,还含有少量其他有机酸。当用NaOH滴定量,所得结果为食醋的总酸度,通常用含量较多的HOAc来表示。滴定反应如下:HOAc+NaOH→NaOHc+H2O
达到化学计量点时溶液显碱性,因此常选酚酞作为指示剂。
操作步骤:用移液管吸取Vml食醋置于250ml容量瓶中,用蒸馏水稀释至刻度,充分摇匀。再用移液管吸出25.00ml放在250ml锥形瓶中,加酚酞指示剂2滴,用NaOH标准溶液滴定,不断振摇,当滴至溶液呈粉红色且在半分钟内不退色即达终点。重复操作2-3次,按下式计算食醋中HOAc的质量分数。
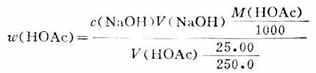
(二)氧化镁含量的测定
因为固体氧化镁难溶于水,所以在测定试样中氧化镁含量(质量分数)时,采用剩余量滴定法。即先称取一定量的待测样品溶于过量且已知准确体积的酸标准溶液中,待反应完全后,用标准碱溶液滴定剩余的酸,反应如下:
MgO+H2SO4(过量)→MgSO4+H2O
2NaOH+H2SO4(乘余) →H2SO4+2H2O
操作步骤:称取约1g(准至0.1mg)左右样品置于锥形瓶中,加入c(H2SO4)=0.5000mol·L-1标准溶液50.00ml,振荡使其溶解,加入甲基橙指示剂2滴,用0.1000mol·L-1NaOH标准溶液滴定剩余的硫酸。当溶液由红变为橙色即为终点。
加入硫酸的总量为:
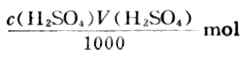
与NaOH反应硫酸的量为:
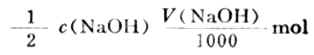
氧化镁的质量分数为:
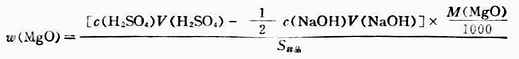
第三节 氧化还原滴定法
一、概述
氧化还原滴定法是以氧化还原反应为基础的滴定分析方法。氧化还原反应较为复杂,一般反应速度较慢,副反应较多,所以并不是所有的氧化还原反应都能用于滴定反应,应该符合滴定分析的一般要求,即反应完全,反应速度快;无副反应等。因此,必须根据具体情况,创造适宜的反应条件。
(1)根据平衡常数的大小判断反应进行程度。一般K≥106或![]()
时,该反应进行得完全。
(2)反应速度快。一般可通过下列几种方法增加反应速度。
①加催化剂。例如,用MnO-4氧化Fe2+时,加入少许Mn2+作为催化剂,可使反应迅速进行。
②升高温度。例如,用MnO-4氧化C2O2-4时,室温下反应进行得很慢,温度升高到80℃时反应能够很快地进行。
(3)无副反应。若用于滴定分析的氧化还原反应伴有副反应发生,必须设法消除。如果没有抑制副反应的方法,反应就不能用于滴定。
按照氧化还原滴定中所用氧化剂的不同,将氧化还原法分为高锰酸钾法、碘量法、重铬酸钾法等。本节主要讨论高锰酸钾法和碘量法。
二、高锰酸钾法
(一)基本原理
![]()
在微酸、中性或弱碱性溶液中,MnO-4被还原为棕色不溶物MnO2:
![]()
因MnO2能使溶液混浊,妨碍疑点观察,所以高锰酸钾法通常在较强的酸性溶液中进行。滴定时使用H2SO4控制酸度,避免使用HNO3(有氧化性)和HCL(有还原性)。
KMnO4还原为Mn2+的反应在常温下进行得较慢。因此,滴定较难氧化的物质时,常需要加热或加催化剂。例如,用KMnO4滴定C2O2-4时,即使在强酸性溶液中加热的情况下,开始时反应也不会迅速进行。只有待最初加入的1-2滴KMnO4溶液的紫色退去后,溶液中就有了Mn2+,接着的反应能较快地进行。这种由于反应生成物本身引起的催化作用称为自动催化作用。
高锰酸钾法的指示剂是KMnO4本身,在100ml水中只要加1滴0.1mol·L-1KMnO4溶液就可以呈现明显的紫红色.而它的还原产物Mn2+则近无色.所以高锰酸钾法不需另加指示剂。
KMnO4氧化性强,在强酸性溶液中可直接滴定一些还原性物质,如Fe2+,AsO3-3,NO-2,Sb3+,H2O2,C2O2-4,甲醛,葡萄糖和水杨酸等;也可间接滴定一些氧化性物质,如MnO2,PbO2,CrO-3,CLO-3等;还可测定一些能与氧化剂或还原剂起反应,但无氧化性或还原性的物质,如Ca2+,Ba2+,Zn2+和Cd2+等。例如,Ca2+能与C2O2-4形成沉淀溶于H2SO4中,然后用KmnO4溶液滴定生成H2C2O4,从而测出Ca2+的含量。
高锰酸钾法的主要缺点是选择性较差,标准溶液不够稳定等。
(二)高锰酸钾的应用示例——市售过氧化氢中H2O2含量的测定
在酸性溶液中,H2O2被KmnO4氧化。
2MnO-4+5H2O2+6H+→2Mn2+5O2+8H2o
氧化还原滴定同样也要经过标准溶液的配制、标定和被测物质含量测定三个过程:
1.KMnO4标准溶液的配制
称取约0.86g KMnO4加蒸馏水配成500ml0.01mol·L-1的标准溶液。加热至沸,并保持微沸约1h。冷却,放暗处约一周后用垂熔玻璃漏斗或玻璃丝过滤。将滤液移至棕色瓶内暗处保存。
2.KMnO4溶液浓度的标定
可用基准物质Na2CO3标定KMnO4溶液的浓度,反应式如下:
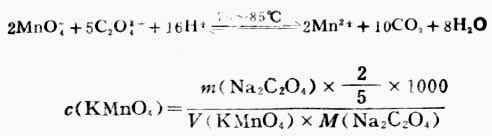
3.过氧化氢含量的测定
用移液管吸取市售过氧化氢1.00ml,放入250ml容量瓶中,稀释25.00ml于锥形瓶中,加6ml3mol·L-1H2SO4,用KMnO4标准溶液滴定溶液呈粉红色,设稀释后H2O2的密度为1,H2O2的含量可按下式计算:
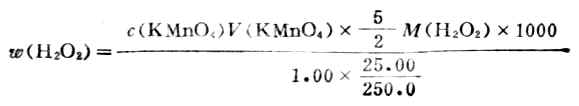
三、碘量法
(一)基本原理
碘量法是利用I2的氧化性和I-的还原性进行滴定的分析方法。
I2+2e-φ2I-φ=0.535V
从φ值可知,I2是一种较弱的氧化剂,而I-是中等 强度的还原剂。低于φ电对的还原性物质如S2-,SO2-3,AsO3-3,SbO3-3,维生素C等,能用I2标准溶液直接滴定,这种方法叫直接碘量法或碘滴定法。高于φ电对的氧化性物质如Cu2+,Cr2O2-7,CrO2-4,MnO2-4,NO-2,CL2,H2O2,漂白粉等,可将I-氧化成I2,再用Na2S2O3标准溶液滴定生成的I2。这种滴定方法叫间接碘量法或滴定碘量法。
1.直接碘量法
用直接碘量法来测定还原性物质时,一般应在弱碱性、中性或弱酸性溶液中进行,如测定AsO3-3需在弱碱性NaHCO3溶液中进行。
![]()
若反应在强酸性溶液中进行,则平衡向左移动,且I-易被空气中的O2氧化:
4I-+O2+4H+→2I2+2H2O
如果溶液的碱性太强,I2就会发生歧化反应:
![]()
I2标准溶液可用升华法制得的纯碘直接配制。但I2具有挥发性和腐蚀性,不宜在天平上称量,故通常先配成近似浓度的溶液,然后进行标定。由于碘在水中的溶解度很小,通常在配制I2溶液时加入过量的KI以增加其溶解度,降低I2的挥发性。直接碘量法可利用碘自身的黄色或加淀粉作指示剂,I2遇淀粉呈蓝色。
2.间接碘量法
间接碘量法测定氧化性物质时,须在中性或弱酸性溶液中进行。例如,测定K2Cr2O7含量的反应如下:
Cr2O72-+6I-+14H+→2Cr3+3I2+7H2O
I2+2S2O22-→2I-+S4O2-6
若溶液为碱性,则存在如下事反应:
I2+S2O22-+10OH-→8I-+2SO42-+5H2o
在强酸性溶液中,S2O2-3易被分解:
S2O22-+2H-→S↓+SO2+H2O
间接碘量法也用淀粉作指示剂,但它不是在滴定前加入,若指示剂加得过早,则由于淀粉与I2形成的牢固结合会使I2不易与Na2S2O3立即作用,以致滴定终点不敏锐。故一般在近终点时加入。应用碘量法除须掌握好酸度外,还应注意以下几点:
(1)防止碘挥发。其办法有:
①加入过量的KI,使I2变成I-。
②反应时溶液不可加热。
③反应在碘量瓶中进行,滴定时不要过分摇动溶液。
(2)防止I-被空气氧化。方法有:
①避免阳光照射。
②Cu2+、NO-2等能催化空气对I-的氧化,应该设法除去。
③滴定应该快速进行。
(二)碘量法应用示例
1.维生素C含量测定
维生素C分子中含有烯二醇基,易被I2定量氧化成含二酮基的脱氢维生c,故可用直接碘量法测定定含量。
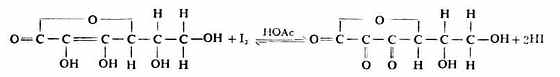
从上式可以看出,在碱性条件下有利于反应向右进行,但维生素C的还原性很强,在碱性环境中易被空气中的O2氧化,故滴定时加一些HOAc使滴定在弱酸性溶液中进行,以减少维被空气氧化所造成的误差。操作如下:
(1)配制0.05mol·L-1I2标准溶液称取6.5gI2和12.5gKI,置于小研钵中,加水少许,研磨至全部溶解后移入棕色瓶中,加水500ml,摇匀后避光阴凉处放置过夜。
(2)标定I2溶液浓度吸取25.00mlI2溶液置于250ml锥形瓶中,加水50ml,用标定过的Na2S2O3标准溶液滴定至浅黄色后,加入0.2%淀粉溶液2-4滴,继续用Na2S2O3溶液滴定至蓝色恰好退去,根据下式计算I2溶液的浓度。
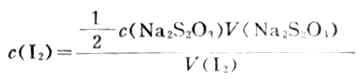
(3)维生素C含量的测定准确称取约0.2g维生素C,放入锥形瓶中,加入新蒸过的蒸馏水50ml2mol·L-1HOAc使其溶解,加淀粉指示剂1ml,立即用I2标准溶液滴定至浅蓝色,按下式计算维生素C的含量
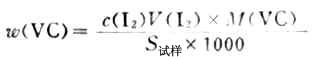
2.漂白粉中有效氯含量的测定
漂白粉的主要成分为CaCL(OCL)和CaCL2的混合物,前者与酸反应放出CL2具有漂白、杀菌和消毒作用,故称之为有效氯。漂白粉的质量是以有效氯的含量为衡量标准的。
CoCl(OCl)+2H+→Ca2++HOCl+HCl
HOCl+HCl→Cl2+H2O
操作步骤如下:
(1)配制0.1mol·L-1Na2S2O3标准溶液 称取约2.5g Na2S2O3溶于500ml新煮并冷却的蒸馏水中,加少许Na2CO3,将溶液贮于棕色瓶中,在暗处放一周后标定其浓度.
(2)标定Na2S2O3标准溶液浓度准确称取约0.15g在130-140℃烘干的分析纯K2Cr2O7,加水溶解后加过量KI和一定量的硫酸,加水稀释至约100ml。用待标定的Na2S2O3溶液滴定至呈黄绿色后,滴加淀粉指示剂,继续滴之下至溶液蓝色消失而呈亮绿色为止。根据下式计算溶液的浓度:
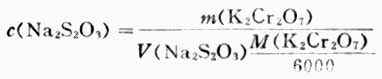
3.漂白粉中有效氯的测定 在漂白粉试样的酸性溶液中,加入过量的KI,然后用Na2S2O3标准溶液滴定生成I2,从而计算出有效氯含量。
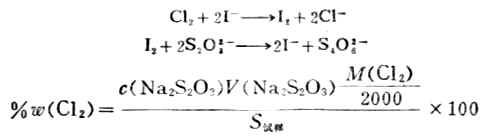
第四节 配合滴定法
在化学分析中,常利用金属离子与某些配合剂生成配合物的反应来测定某成分的含量。利用配合反应滴定分析方法配合滴定法。能用于配合滴定的配合剂有很多种,其中最常用的是氨羧配合剂,而氨羧配合剂中以EDTA应用最广。
一、EDTA配合沆定的基本原理
(一)EDTA配合滴定的基本原理
EDTA(用H4Y表示)是一个多元酸,在溶液中以H4Y,H3Y-,HY3-,Y4-等形式存在。其中Y4-能与多种金属离子直接配合生成稳定的配合物,配合比为1:1。
金属离子与EDTA形成的配合物的稳定性常用稳定常数的对数表示。EDTA与金属离子形成配合物的反应如下(为简单起见略去电荷):
![]()
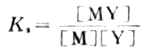 (7-6)
(7-6)
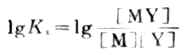 (7-7)
(7-7)
Ks或lgKs越大,配合物越稳定。表7-2列举了一些常见金属离子与EDTA形成配合物的lgKs值,
表7-2 EDTA金属离子配合离子lgKs值
| 金属离子 | 配合离子 | lgKs | 金属离子 | 配合离子 | lgKs | 金属离子 | 配合离子 | lgKs |
| Na+ | NaY3- | 1.66 | Fe2+ | FeY2- | 14.33 | Cu2+ | CuY2- | 18.7 |
| Li+ | LiY3- | 2.79 | Al3+ | AlY- | 16.11 | Hg2+ | HgY2- | 21.8 |
| Ag+ | AgY3- | 7.32 | Co2+ | CoY2- | 16.31 | Sn2+ | SnY2- | 22.1 |
| Ba2+ | BaY2- | 7.78 | Cd2+ | CdY2- | 16.40 | Bi3+ | BiY- | 22.8 |
| Mg2+ | MgY2- | 8.64 | Zn2+ | ZnY2- | 16.40 | Cr3+ | CrY- | 23.0 |
| Ca2+ | CaY2- | 11.0 | Pb2+ | PbY2- | 18.30 | Fe3+ | FeY- | 24.23 |
| Mn2+ | MnY2- | 13.8 | Ni2+ | NiY2- | 18.56 | Co3+ | CoY- | 36.0 |
式(7-6)中的[Y]是指平衡时的[Y4-],不包括EDTA其他存在形式,故称Ks为配合物的绝对常数,它与溶液的酸度无关。表7-2中所列数据均为绝对稳定常数。由于EDTA是弱酸性的配合剂,因此溶液的酸度对EDTA配合物的稳定性有很大的影响。
1.酸度的影响
酸度的影响可用下式表示:
![]()
可见溶液的酸度越高,[Y4-]越低,越不利于配合滴定的进行;溶液的酸度越低[Y4-]越高,配合滴定进行得越完全。EDTA溶液中除了Y4-外,还存在其他形式。设EDTA总浓度为[Y]总,则
[Y]总=[H4Y]+[HY-]+[HY2-]+[HY3-]+[Y4-](7-8)
[Y]总与[Y4-]之间存在着一定的比例关系。
[Y]总=αH·[Y-4]
αH=[Y]总/[Y4-]
比例系数aH叫做酸效应系数,它是随酸度的增大而增大,aH可以从EDTA的各级电离常数和溶液中[H+]计算出来。
将式(7-9)代入式(7-6)可得
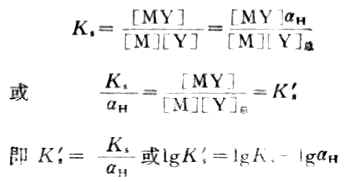 (7-10)
(7-10)
式中Ks'是考虑了酸效应的稳定常数,叫做条件稳定常数或表观稳定常数,在不同酸度下,KS是不变的,但由于aH随酸度增大而增大,故Ks'则随酸度的增大而减小。在配合滴定中,要求反应量的完成,Ks'越大,反应进行得越完全。
如被测金属离子的初始浓度为0.02mol·L-1,当反应完全时,金属离子基本都配合成MY,即得[MY]=1.0×10-2mol·L-1,设测定的允许误差为0.1%,则滴定达到平衡时,
[M=[Y]≤1.0*10-2*0.1%=1.0*10-5(mol·L-1)
将这一关系代入式(7-10)则得
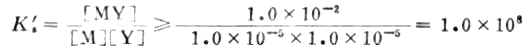
或lgKs'≥8 (7-11)
可见MY配合物的 Ks'必须等于或大于1.0×108,才能满足滴定误差小于0.1%的要求
由式(7-10)可得
lgαH≤lgKs-8 (7-12)
利用上式,再根据7-3可以求得滴定各种多金属离子所允许的最低PH值。
7-3 不同PH时EDTA的lgaH
| pH | lgaH | pH | lgaH | pH | lgaH |
| 21.18 | 4 | 8.44 | 8 | 2.26 | |
| 1 | 17.20 | 5 | 6.45 | 9 | 1.28 |
| 2 | 13.52 | 6 | 4.65 | 10 | 0.45 |
| 3 | 10.60 | 7 | 3.32 | 11 | 0.07 |
在滴定过程中也应控制一定的酸度,因为EDTA在滴定中不断有H+释放出来,使溶液的PH值降低。例如用EDTA二钠溶液滴定Ca2+时,其反应式如下:
![]()
因此配合滴定常需用缓冲控制酸度。
2.其他配合剂的影响
溶液中存在其他配合剂时的影响用下式表示:
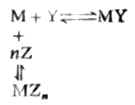
Z代表其他配合剂,n为Z的系数。由于其他配合剂的存在,降低了金属离子的浓度,使平衡向左移动。配合滴定中常常利用这个原理消除干扰离子。例如,用EDTA滴定Mg2+和Cd2+、Zn2+混合液中的Mg2+时,可在滴定前向混合液中加入KCN,使Cd2+和Zn2+与CN-形成稳定的[Zn(CN)4]2-和[Cd(CN)4]2-(Mg2+不与CN-配合),从而消除了Cd2+和Zn2+对滴定的干扰。这种消除干扰的作用叫掩蔽作用,起掩蔽作用的配合剂叫掩蔽剂。
(二)金属指示剂
配合滴定中指示终点的方法很多,其中最重要、应用最多的是金属指示剂。它常常是一种配合剂,能与金属离子形成可溶于水的有色配合物。

在滴定前,溶液中金属指示剂与金属离子形成有色配合物,溶液的颜色就是这种酏合物的颜色。滴不定期开始后,EDTA与溶液中自由金属离子配合。滴定接近并达到终点时,与指示剂配合的金属离子浓度剧烈降低,MIn转变为In,溶液的颜色由MIn的颜色转变为指示剂In的颜色。
值得注意的是金属指示剂与金属离子形成的配合物要有适当的稳定性。稳定性太低,配合物易离解,会使终点提前出现。稳定性太高,稍过终点时,EDTA仍不能夺取MIn中的金属离子,就无法指示终点,使终点出现过迟。
常见的金属指示剂有铬黑T(EBT)、钙试剂等。现以铬黑T为例进行介绍。铬黑T(用NaH2In表示)是一个具有弱酸性酚羟基的有色配合剂,在不同的酸度下为不同的颜色。
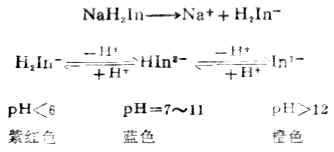
在PH<6或PH>12时,游离的指示剂与形成金属离子配合物的颜色没有明显的区别,在PH=7~11的溶液里指示剂显蓝色,而与金属离子生成的配合物为红色,颜色有极明显的差别。所以用铬黑T作指示剂时,PH值应控制在7~11的范围内,最适宜的PH值为9~10.5。例如,用EDTA滴定Mg2+时,先在被测溶液中加入NH+4-NH3·H2O缓冲溶液,将PH值控制在10左右,然后加铬黑T作指示剂数滴,用0.02mol·L-1EDTA标准溶液滴定。
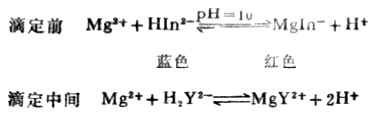
滴定终点时,由MgIn-的红色转变为HIn2-的蓝色。
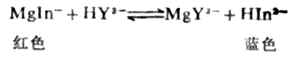
在滴定过程中,颜色的变化为:红色→紫色→蓝色。当溶液的颜色由红色转变成紫色时,说明滴定已接近终点,再稍许滴定几滴即达到终点。
二、EDTA配合滴定应用示例——水的总硬度测定
水的总硬度是指水中Ca2+、Mg2+的总含量。水中钙镁酸式碳酸盐形成的硬度称为暂时硬度,钙镁的其他盐类如硫酸盐、氯化物等形成的硬度称为永久硬度。暂时硬度和永久硬度的总和称为总硬度,其单位用每升水中含CaO或CaCO3的毫克数来表示,可写成CaOmg·L-1或CaCO3 mg·L-1。
操作步骤如下;
(一)配制0.01 mol·L-1的EDTA标准溶液
称取约0.19gEDTA二钠,用蒸馏水配成500ml溶液,然后用MgCO3作基准物质标定其浓度。
(二)EDTA溶液的浓度的标定
称取在110℃烘干过的基准物质MgCO30.21g(准至0.1mg),置于烧杯中,用稀盐酸溶解后配成250ml溶液,吸取25.00ml于锥形瓶中,加浓氨水至溶液呈碱性,再加5mlPH约为10的NH+-NH3·H2o 缓冲溶液,加铬黑T指示剂,用EDTA标准溶液滴定至溶液呈蓝色.
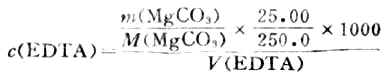
(三)水的总硬度测定
取水样50ml,加入5mlPH=10的NH+-NH3·H2O 缓冲溶液,再加铬黑T指示剂数滴,用0.01ml mol·L-1的EDTA标准溶液滴定至溶液呈蓝色。按下式计算出每升水中CaCO3的含量作为总硬度(单位mg·L-1)。
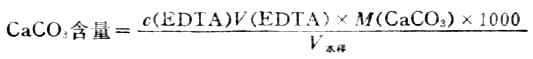
第八章 比色分析
第一节 比色分析的基本原理
比色分析是基于溶液对光的选择性吸收而建立起来的一种分析方法,又称吸光亮度法。
有色物质溶液的颜色与其浓度有关。溶液的浓度越大,颜色越深。利用光学比较溶液颜色的深度,可以测定溶液的浓度。
根据吸收光的波长范围不同以及所使用的仪器精密程度,可分为光电比色法和分光亮度法等。
比色分析具有简单、快速、灵敏度高等特点,广泛应用于微量组分的测定。通常中测定含量在10-1~10-4mg·L-1的痕量组分。比色分析如同其他仪器分析一样,也具有相对误差较大(一般为1%~5%)的缺点。但对于微量组分测定来说,由于绝对误差很小,测定结果也是令人满意的。在现代仪器分析中,有60%左右采用或部分采用了这种分析方法。在医学学科中,比色分析也被广泛应用于药物分析、卫生分析、生化分析等方面。
一、物质的颜色和光的关系
光是一种电磁波。自然是由不同波长(400~700nm)的电磁波按一定比例组成的混合光,通过棱镜可分解成红、橙、黄、绿、青、蓝、紫等各种颜色相连续的可见光谱。如把两种光以适当比例混合而产生白光感觉时,则这两种光的颜色互为补色。图8-1中处于同一直线关系的两种色光(如绿与紫、黄与蓝)互为补色。
当白光通过溶液时,如果溶液对各种波长的光都不吸收,溶液就没有颜色。如果溶液吸收了其中一部分波长的光,则溶液就蜈现透过溶液后剩余部分光的颜色。例如,我们看到KMnO4溶液在白光下呈紫红色,就是因为白光透过溶液时,绿色光大部分被吸收,而其他各色都能透过。在透过的光中除紫红色外都能两两互补成白色,所以KMnO4溶液呈现紫红色。
同理,CuSO4溶液能吸收黄色光,所以溶液呈蓝色。由此可见,有色溶液的颜色是被吸收光颜色的补色。吸收越多,则补色的颜色越深。比较溶液颜色的深度,实质上就是比较溶液对它所吸收光的吸收程度。表8-1列出了溶液的颜色与吸收光颜色的关系。
表8-1 溶液的颜色与吸收光颜色的关系
| 溶液颜色 | 绿 | 黄 | 橙 | 红 | 紫红 | 紫 | 蓝 | 青蓝 | 青 | |
| 吸收光 | 颜色 | 紫 | 蓝 | 青蓝 | 青 | 青绿 | 绿 | 黄 | 橙 | 红 |
| 波长/nm | 400~450 | 450~480 | 480~490 | 490~500 | 500~560 | 560~580 | 580~600 | 600~650 | 650~760 | |
二、朗伯-比尔(Lambert-Beer)定律
当一束平行单色光(只有一种波长的光)照射有色溶液时,光的一部分被吸收,一部分透过溶液(图8-2)。
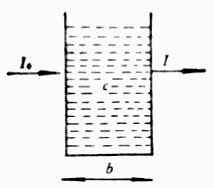
图8-2 光吸收示意图
设入射光的强度为I0,溶液的浓度为c,液层的厚度为b,透射光强度为I,则
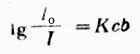 (8-1)
(8-1)
式中lgI0/i 表示光线透过溶液时被吸收的程度,一般称为吸亮度(A)或消亮度(E)。因此,上式又可写为:
A=Kcb(8-2)
上式为朗伯-比尔定律的数学表示式。它表示一束单色光通过溶液时,溶液的吸光度与溶液的浓度和液层厚度的乘积成正比。
式中,K为吸光系数,当溶液浓度c和液层厚度b的数值均为1时,A=K,即吸光系数在数值上等于c和b均为1时溶液的吸光度。对于同一物质和一定波长的入射光而言,它是一个常数。
比色法中常把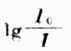
称为透光度,用T表示,透光度和吸光度的关
系如下:
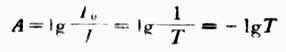 (8-3)
(8-3)
当c以mol·L-1为单位时,吸光系数称为摩尔吸光系数,用ε表示,其单位是L·mol-1·cm-1。当c以质量体积浓度(g·ml-1)表示时,吸光系数称为百分吸光系数,用E1%1cm表示,单位是ml·g-1·cm-1。吸光系数越大,表示溶液对入射光越容易吸收,当c有微小变化时就可使A有较大的改变,故测定的灵敏度较高。一般ε值在103以上即可进行比色分析。
如果测定某种物质对不同波长单色光的吸收程度,以波长为横坐标,吸光度为纵坐标作图可得一条曲线,即物质对光的吸收曲线,可准确地描述物质对光的吸收情况。
图8-3是几种不同浓度的KMnO4溶液的吸收曲线,溶液对波长525nm附近的绿光吸收量最强,而对其他波长的光吸收较弱。光吸收程度最大处的波长叫做吸收波长,用λmax表示。不同浓度的KMnO4溶液所得的吸收曲线,最大吸收波长都一致,只是相应的光被吸收的程度不同。
吸收曲线可作为比色分析中波长选定的依据,测定时一般选择λmax 的单色光作为入射光。这样即使被测物质含量较低也可得到较大的吸光度,因而可使分析的灵每度较高。
若所测定的溶液无色,可在测定前加入适当的显色剂,通过与待测成分的化学反应使溶液晱色即可测定此待测成分。
例如, 已知在525nm处KnO4溶液的ε=2235L· mol-1·cm-1,若用2cm比色皿,为使所测得的透光率介于20%~65%之间,溶液的浓度范围应是多少?
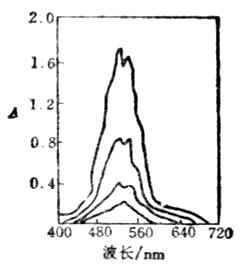
图8-3 KMnO4液的吸收光谱曲线
解:若T=20%
则
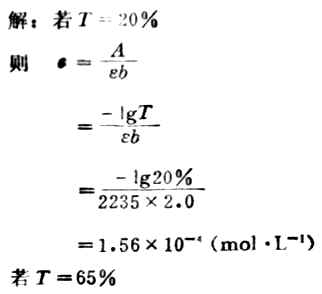
则 c=-lg65%/2235*2.0=4.19*10-5(mol·L-1)
第二节 比色分析测量仪器和测量方法
比色分析法通过比较溶液对光的吸收程度以测定物质的含量。
一、比色测量仪器
(一)比色测量仪器的基本部件
比色测量仪器一般包括以下五大部件(图8-4)。

图8-4 比色测量仪器部件示意图
1.光源
在光电比色计和可见光分光亮度计中,采用6~12V的钨灯,其最适宜的波长范围是360~1000nm,为使光的强度稳定,须用稳压装置来稳定电压。
2.波长控制器
在光电比色计中采用滤光片作为波长控制器。滤光片是有色玻璃片,其作用是从光源发出的连续光谱中分出实验所需的某一特定波长范围的光,即获得适当波长的近似单色光。
选择滤光片的原则是滤光片最易透过的光,也就是溶液最易吸收的光。即滤光片的颜色与溶液的颜色应互为补色,这是因为有色溶液对它的互补色光有最大的吸收。581-G型光电比色计通常只有红、绿和蓝三块滤光片。例如,要测定KMnO4溶液,就应选用绿色滤光片。
分光光度计采用单色器来控制波长。它可以把连续波长的光分解,从中得出任一所需波长的更纯的单色光。单色器包含有狭缝调节、透镜系统以及色散元件。
图8-5为自准式单色光器。光源发出的光经入射狭缝由凹面准直镜反射后的平行光投在棱镜上,经棱镜色散后的光又经准直镜反射到出射狭缝,转动棱镜便可在出射狭缝得到所需波长的单色光。
图8-5 自准式单色光器示意图
图8-6 硒光电效应示意图
3.吸收池
吸收池供比色时盛溶液用,它是用无色透明、厚度均匀的玻璃制成的。其透光的两面严格平行。同一系列的测定中,所用的比色皿必须配套,即同一配套比色皿盛有同一溶液在同一波长时测得的透光率误差不得越过0.5%。实验时可根据溶液的浓度不同选择。0.5,1.0,2.0,3.0cm不同规格的比色皿。比色皿要保持清洁,透光面要注意保护,不得用手直接接触或用粗糙的滤纸擦拭,以免划伤表面,影响吸收程度。若外壁有液珠,应用滤纸吸干后再用擦镜纸擦净。
4.光电转换器
它是将光能转换成电信号的器件,常用的有光电池和光电管。
光电池常用的硒光电池如图8-6,适用 于380~750nm波长范围。当光线照射到光电池时,电子从半导体表面逸出。由于硒的半导体特性而在电路中产生光电流。将光电池与一个灵敏检流计相联,在照射光强度不太大且外电路电阴很小时,光电流大小与照射光的强度成正比。因此可根据光电流的大小测量透过溶液的光强度。
硒光电池的优点是光电流较大,可不必经过放大而直接用灵敏检流计测量。有时当光电池受强光照射或连续使用时间太长时,容易产生“疲劳”,这时需使其在暗的状态下暂作恢复,方可继续使用。
光电管由封装在真空透明管中的一个半圆柱型阴极和一个丝状阳极组成(图8-7)。阴极凹面有光电发射材料层,被光照射可发电子。当两极间加有电压时,发射出来的电子就流向阳极产生光电流。发射出的电子数目与射在该表面上光束的强度成正比。光电管产生的电流啼弱,经放大器放大后可由微安电表直接指示出吸光度或透光率。
图8-7 光电管线路示意图

图8-8 吸光度和透光率标尺
5.检流计
用光电池作光电转换器的比色测量仪器中,检流计一般采用悬镜式光电反射检流计,其灵敏度较高,能测量10-9A(安培)的电流。检流计有吸光度A和百分透光率T(%)两种刻度标尺,可直接读数(图8-8)。
标尺上透光率T是等分的而吸光度A的刻度是不均匀的。透光率T可用小数或百分率表示。A与T的关系可推导为:
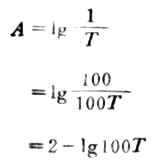
例如,已知某溶液对某一波长的光吸光度为0.04,其透光率可由下面方法求得。
0.04=-lgT
lgT=-0.40
T=0.398=39.8%
又如,已知某溶液对某一波长光的透光率为65%,吸光度为:
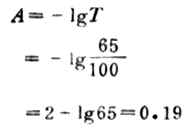
对于用光电管作光电转换器的仪器,由于加了放大器,可方便地连接微安电表、记录仪,数字显示器等指示器,也可以调节电桥平衡的方式读数取数据。
(二)比色测量仪器
1.光电比色计
光电比色计用光电池和检流计测量透射光的强度并直接可读出百分透光率T(%)或吸光度A。图8-9是581-G型光电比色计的示意图。它是利用滤光片把钨灯产生的白光中与测定无关的光除去,使入射光尽可能是接近溶液补色的单色光,从而提高了比色分析的准确度。
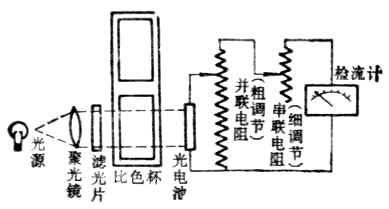
图8-9 581-G型光电比色计光学线路示意图
图8-10 721型分光光度计光学系统示意图1.光源 2.,8.聚
光透镜 3.棱镜 4.准直镜5.,11.保护玻璃 6.入射狭缝 7.
平面镜 9.吸收池10.光门 12.光电管 13.光栅
2.721型分光光度计
721型分光光度计的工作波长范围为360-800nm。采用真空光电管作为光电能量转换元件,在整个可见光区都比较灵敏。同时采用晶体管放大电路和电表直读结构,仪器的灵敏度和稳定性都比较好。
图8-10为721型分光光度计的光学系统示意图。由光源发出的连续辐射于聚光镜上,经平面镜转角90度反射到入射狭缝,射入单色器。入射光经过准直镜反身射在出射狭缝上,再经过聚光透镜后进入比色皿。经溶液吸收后的透射光通过光门照射在光电管上转换为光电流信号,经过入大后输入检流计,由电表直接显示吸光度。
二、比色分析的测量方法
无论是光电比色计还是分光亮度计,最常用的测量方法有如下两种。
(一)标准曲线计
先配制一系列不同浓度的标准溶液,用选定的显色剂显色。选用合适波长的入射光(光电比色计用滤光片,分光亮度计可转动波长调节器)。测定时先以空白溶液调节透光率100%,然后分别测定标准系列的吸亮度。以吸亮度为纵坐标,浓度为横坐标作图得到一条通过原点的直线,叫做标准曲线(或称工作曲线)。
例如,测定维生素B12时,可预先绘制维生素B12的A-c标准曲线(图8-11),再用完全相同的方法和步骤测定被测溶液的吸亮度,即可从标准曲线上找出被测溶液的浓度或含量。
这种方法叫做标准蛐线法。标准曲线可在固定仪器和方法的条件下多次使用,适合于经常性工作。但若仪器不同或测定方法及条件改变,测得的标准曲线不同。因此在更换任何测定条件时都需重新绘制标准曲线。
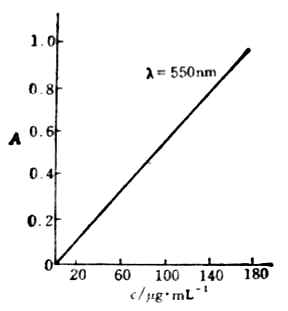
图8-11 维生素B12的标准曲线
(二)直接比较计算法
若仅对个别样品进行测定,且A-c曲线线性良好,可水作标准曲线而直接比较测定结果。
先配制一个被测物质溶液浓度相近的标准溶液,与被测溶液在相同条件下测定吸光度。根据下式可以计算。
A标=K标c标b标
A测=K测c测b测
由于使用同一波长的入射光,采用同样的比色皿,测定同样的物质。所以
K标=K测
b标=b测
因此A标/A测=c标/c测
则c测=A测/A标×c标
第二节 比色分析应用示例——铁的含量测定
一、原理
应用比色分析测定溶液中伯的含量有硫氰酸盐显色法、磺基水杨酸法及邻菲罗啉显色法等各各种方法。现以磺基水杨酸法为例介绍铁的含量测定。
在不同酸度下,Fe3+和磺基水杨酸生成组成不同的配合物。若控制溶液PH值在8-11.5的条件下显色,可生成配位数为6的黄色三磺基水杨酸合铁配合物。反应式如:
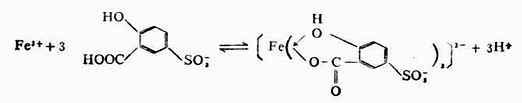
上式可简写为
![]()
溶液的最大吸收波长λmax=420nm,因此可在420nm 处进行测定(若用光电比色计测定可选择蓝色光片)。此方法适合于测定无大量Cu2+、Ca2+、Cr3+、Ni2+等离子存在的溶液中铁离子的含量。
二、操作步骤
(一)标准曲线的绘制
称取一定量硫酸铁铵[NH4Fe(SO4)2·12H2O]用蒸馏水溶解,加适量配制成含 Fe3+0.1lg·L-1的标准溶液,再稀释成含Fe3+0.025mg·L-1的操作溶液。
取25ml容量瓶6只,编号后分别加入操作溶液0.00,1.00,2.00,3.00,4.00及5.00ml,各加入10%NH4CL溶液2ml和10%磺基水杨酸溶液2ml,滴加氨水至溶液由紫红色变为黄色,并使氨水稍过量,然后用NH4CL-NH3缓冲溶液稀释至刻度,摇匀,以1号为空白,在420nm处依次测定吸光度。以Fe3+含量为横坐标,吸光度为纵坐标绘制标准曲线。
(二)样品的测定
取25ml容量瓶1只,准确加入经过处理的浓度在标准范围内的被测溶液,按上面标准系列配制的同样加入等量的显色剂和缓冲溶液,在相同条件下测定被测溶液的吸光试,利用标准曲线找出样品溶液的浓度,根据样品溶液的稀释倍数,求出样品的含量。
例如,用磺基水劣根性酸法比色测定微量铁含量。称取0.432g硫酸铁铵溶于水,加18%硫酸溶液1ml,转移至500ml容量瓶中,用水定容,作为标准溶液,其浓度为0.1g·L-1。取下列不同体积的上述溶液于50ml容量瓶中,加入显色剂后定容,在420nm处测定吸光度,结果如下:
| 溶液体积/ml | 1.00 | 2.00 | 3.00 | 4.00 | 5.00 |
| 吸光度A | 0.097 | 0.200 | 0.304 | 0.408 | 0.510 |
| c/(g·L-1)×103 | 2.00 | 4.00 | 6.00 | 8.00 | 10.00 |
以吸光度A值为纵坐标,标准溶液中Fe3+含量为纵坐标作图,即得如图8-12的标准曲线。
吸取待测液样品5.00ml于50ml容量瓶中,加入显色剂后定容,其方法与绘制标准曲线相同,测得吸光度为0.341。由标准曲线查得A为0.341时,c为6.60×10-3g·L-1。故样品溶液中铁离子的浓度为
c=6.60×10-3×50.00×1/5.00
=6.6×10-2(g·L-1)
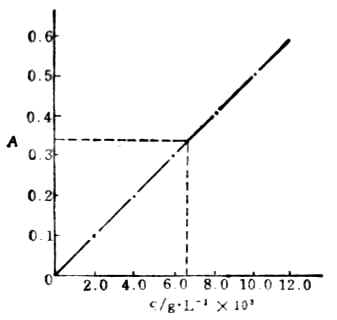
图8-12 磺基水杨酸法测定铁的标准曲线
第九章 胶体溶液
胶体化学是研究胶体分散系-物理化学性质的一门科学。它不仅和工农业生产有着密切的关系,而且和生命科学紧密相关。在研究动植物的生命现象时,随处都会遇到胶体体系。从胶体化学的观点来说,人体就是典型的胶体体系。因为细胞、血液、淋巴液、肌肉、脏器、软骨、皮肤、毛发等都属于胶体体系。因此,生物体内发生的许多生理变化和病理变化与胶体的性质有联系。另外,许多药物、消毒剂、杀虫剂等也是以胶体形式生产和使用。因而对于医学工作者来说,学习一些胶体体系的基本知识是很有必要的。
第一节 分散系
一种或几种物质分散在另一种介质中所形成的体系称为散体系。被分散的物质称为分散相,而连续介质称为分散介质。例如食盐水溶液,食盐是分散体系又分为均相分散系和多相分散系。低分子溶液与高分子溶液为均相分散系。溶胶与粗分散系为多相分散系。
分散体系的某些性质常随分散相粒子的大小而改变,因此,按分散相质点的大小不同可将分散系分为三类(表9-1):低分子(或离子)分散系(其粒子的线形大小在1nm以下);胶体分散系(其粒子的线形大小在1-100nm之间);粗分散系(其粒子的线形大小在100nm以上)。三者之间无明显的界限。
一、粗分散系
在粗分散系中,分散相粒子大于100nm,因其粒子较大用肉眼或普通显微镜即可观察到分散相的颗粒。由于其颗粒较大,能阻止光线通过,因而外观上是浑浊的,不透明的。另外,因分散相颗粒大,不能透过滤纸或半透膜。同时易受重力影响而自动沉降,因此不稳定。
粗分散系按分散相状态的不同又分为悬浊液(固体分散在液体中——如泥浆)和乳浊液(液体分散在液体中——如牛奶)。
二、低分子分散系
分散相粒子小于1nm,因分散相粒子很小,不能阻止光线通过,所以溶液是透明的。这种溶液具有高度稳定性,无论放置多久,分散相颗粒不会因重力作用而下沉,不会从溶液中分离出来。分散相颗粒能透过滤纸或半透膜,在溶液中扩散很快,例如盐水和糖水等。
三、胶体分散系
胶体分散系即胶体溶液,分散相粒子大小在1-100nm之间,属于这一类分散系的有溶胶和高分子化合物溶液。由于此类分散系的胶体粒子比低分子分散系的分散相粒子大,而比粗分散系的分散相粒子小,因而胶体分散系的胶体粒子能透过滤纸,但不能透过半透膜。外观上胶体溶液不浑浊,用肉眼或普通显微镜均不能辨别。
胶体是物质的一种分散状态,不论在任何物质,只要以1-100nm之间的粒子分散于另一物质中时,就成为胶体。例如,氯化钠在水中分散成离子时属低分子分散系。而在苯中则分散成离子的聚集体,聚集体粒子的大小在1-100nm之间,属胶体溶液。许多蛋白质、淀粉、糖原溶液及血液、淋巴液等属于胶体溶液。
表9-1 分散体系的分类
| 粒子大小 | 类型 | 分散相 | 性质 | 实例 | |
| <1nm | 低分子分散系 | 原子、离子或小分子 | 均相,稳定体系,扩散快,能透过滤纸、半透膜,形成真溶液 | 蔗糖,氯化钠,醋酸水溶液等 | |
| 1~100nm | 胶体分散系 | 高分子 | 高聚物大分子 | 均相,稳定体系,扩散慢,不能透过半透膜,能透过滤纸,超显微镜下看不见,形成真溶液 | 蛋白质,核酸水溶液等 |
| 溶胶 | 胶粒(原子或分子的聚集体) | 多相,不稳定体系,扩散慢,不能透过半透膜,能透过滤纸,超显微镜下看不见,形成真溶液 | Fe(OH)3,As2S3,金溶胶等 | ||
| >100nm | 粗分散体系 | 粗粒子 | 多相,不稳定体系,扩散很慢或不扩散,较快地下沉,不能透过滤纸和半透膜,形成悬浊液、乳浊液 | 混浊泥水,牛奶,豆浆等 | |
第二节 溶胶
溶胶的分散相粒子即胶体粒子,是由许多分子或原子聚集而成的,因此分散相与分散介质之间存在着相界面,形成多相体系,于是出现了大量界面现象。
一、界面现象
物体的表面是指它与空气或与本身的蒸气接触的面,而物体的表面与另一相接触的面则称为界面。凡是界面上发生的一切物理化学现象统称为界面现象。
(一)界面张力和界面能
由于物质分子与分子间存在相互吸引力的作用,位于表面层的分子和它的内部分子所处的情况是不同的。以液体为例来说明。图9-1中A为处于液体内部的分子,它从各方向所受到相邻分子的引力是均衡的,即作用于该分子上的吸引力的合力等于零。B处于液体表面层的分子,它所受到相邻分子吸引力的合力等于零,而且其合力是指向液体内部并与液面相垂直的。液体表面层的其它分子也都受到同样力的作用,其结果是这种合力企图把表面层的分子拉入液体内部,因面液体表面有自动缩小的倾向。如果想使表面增大,就必须使分子从液体内部反抗引力将其拉到表面,这一过程需要消耗一定量的功,这种功成为表面层分子多余的能量贮藏在表面上。这种液体表面层的分子比内部分子所多余的能量叫界面能(液体——空气),单位是J·m-2。
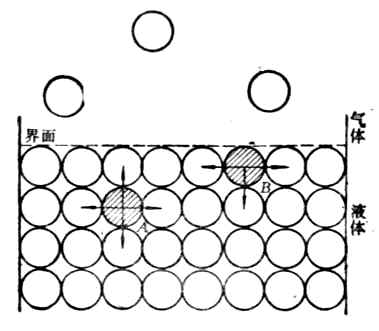
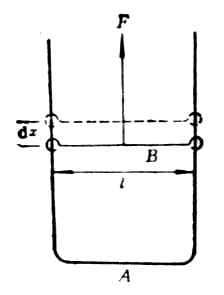
图9-1 表面张力来源 图9-2 表面张力的测量
在图9-2中,线圈A上面有一个无磨擦的滑动线B,将它们浸在(具有一定界面张力的)液体中,在线圈A和滑动线B围绕的平面上形成一层薄膜。因为液体表面有缩小的趋势,滑动线B将自动地向下移动。现在,我们从相反方向施以外拉力F以阻止其移动。这个力F将作用于薄膜的整个边缘l,力的大小随着长度l而改变。从实验中可以看到,作用于这个薄膜整个边缘的是每单位长度的力,这个力称界面张力,单位是N·m-1。也可用单位面积的能表示,称比表面能,单位是J·m-2。故界面张力又称比表面能。
(∵1J=1N·m ∴1J·m-2=1N·m·m-2=1N·m-1)
界面能等于界面张力(σ)与界面积(S)的乘积:
E=σ·S
物体的界面能有自动降低的趋势。界面能愈大,降低的趋势也愈大。液体界面能的减小可以通过一种自动过程来实现,即自动减小S或自动减小σ,或者S和σ两者同时减小。
恒温下,液体的σ是一个常数,因此界面能的减小只能通过减小S的办法进行。如水滴常呈球形——界面能最小。在溶液中界面积不变的情况下,界面能的减小只能用减小σ的办法进行,即液体界面从周围介质中自动吸引其它物质分子、原子或离子填入表面层来降低它的σ,即吸附作用。
(二)吸附
溶胶属多相分散系,分散相和分散介质之间有界面存在,对于一定体积的物质,分散粒子愈小,个数愈多,其总面积就愈大,比表面积(即单位体积物质的表面积)也就愈大。例如,当1cm3的物质分割到每边长10-5-10-7cm大小的立方体时,其比表面积达到60-600m2,因此大大改变了界面性质。
1.固体界面上的吸附
固体的表面不能自动缩小,它只能依赖于吸附其它物质以降低界面能。具有吸附作用的物质叫吸附剂,被吸附的物质叫吸附质。疏松多孔的固体,如活性炭、硅胶、活性氧化铝、铂黑等都是良好的吸附剂。1g良好活性炭的微孔界面积可达1000m2,常用于防毒面具中,也可用作蔗糖脱色。硅胶和活性氧化铝都可用作色层分析中的层析中的层析柱或薄层的吸附剂。铂黑用于氢电极以吸附氢。
2.固体-气体界面上的吸附
气体在固体界面上的吸附作用是可逆的。气体分子可被吸附到吸附剂的界面上,但由于分子的热运动,气体又可能挣脱界面进入气相,这种过程叫解吸。当吸附与解吸达到平衡时,单位质量吸附剂所能吸附气体的量叫做吸附量。吸附是放热过程,解吸是吸热过程。
当温度不变时,增加气体压力,吸附量增加。当气体的压力增加到一定程度时,吸附量达到一极限值,这时吸附剂界面的吸附已达到饱和,这种在给定温度下,以吸附量为纵坐标,以气体压力为横坐标作图所得的曲线,叫等温吸附线(图9-3)。
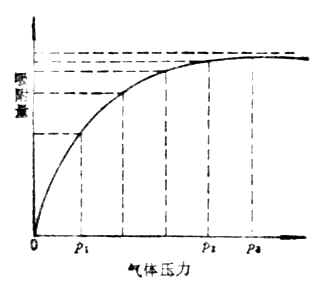
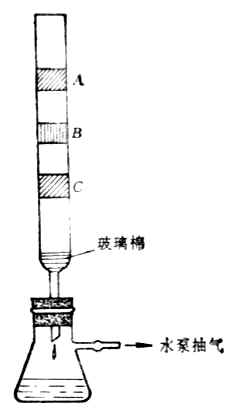
图9-3 吸附等温曲线 图9-4 柱层析法简单装置图
3.固体-液体界面上的吸附
固体-液体界面上的吸附,可能是溶质吸附,也可能是溶剂吸附,通常两者兼有只是程度不同。例如,活性炭从色素水溶液中吸附的色素就远比吸附的水多,因此可以用活性炭使溶液脱色。但是如果把活性炭放入色素的酒精溶液中,由于活性炭对酒精的吸附大于对色素的吸附,故不能用于在酒精溶液中对色素的脱色。
在固体-液体界面上的吸附中,吸附的溶质可以是电解质,也可以是非电解质。
分子吸附指吸附物质的整个分子被吸附在固-液界面上。被吸附物质是非电解质或弱电解质的分子型物质。利用各物质吸附能力的不同,选用适当的吸附剂,可将溶液中的各种溶质的混合物加以分离。利用各种溶质与吸附剂之间吸附能力的不同,使溶质得到分离的方法叫色谱法或层析法。如在一玻璃管(柱型)中,装入某种吸附剂(如氧化铝或硅胶)作为吸附柱。当把含各种溶质的溶液流经管中的吸附柱时,由于不同物质在吸附柱上的吸附能力不同,因而被吸附在柱的不同高度的位置上,最容易吸附的物质在柱的上部,其余依次向下。随后取出吸附柱,分层切开,再用溶剂分别提取,即被分离。或者用溶剂把被吸附物质由吸附柱上洗脱下来。在洗脱过程中,吸附力弱的先被洗出,吸附力强的后被洗出,将洗出液分段收集,同样达到分离的目的。。
例如,用石油醚提取绿叶中的成分:将石油醚加到绿叶中,使其作用后,把渣子滤去,将溶液倒入吸附柱,在柱上依次显出叶绿素、叶红素、胡萝卜素等色层(图9-4中的A,B,C)。然后分别提取即可得各种成分。
二、溶胶的性质
当光波投射到粒子上时,如果粒子大于波长,则光波以一定的角度从粒子表面反射出来。如果粒子远小于光波的波长,则光波绕过粒子前进不受阻碍。当粒子的大小和光波波长接近或稍小时,光波产生散射。溶胶粒子的大小在1-100nm之间,与普通光波波长接近,因此有一定强度的散射现象,称为丁铎尔(Tyndall)现象。即当一束强光投射到溶胶上,在暗室或黑暗背景下,从光束的垂直方向观察,可以清楚地观察到一条光带(图9-5),这是胶体溶液的特点。
溶胶中胶体粒子和溶液中溶质的粒子相似,也处于不停的运动状态,这种不停的无规则的运动称为布朗(Brown)运动(图9-6)。由此表现出与胶体粒子运动有关的性质,称为胶体的分子动力学性质,如扩散、渗透、沉降等。它们和胶体粒子的大小和形状有密切的关系。所以从分子动力学性质出发,可以研究胶体粒子的大小和形状。其次,溶胶由于分子动力学性质,可以保持胶体粒子不因重力作用而沉集在容器底部。这种保持分散相不从分散介质中分离出来的性质,称为动力学稳定性。
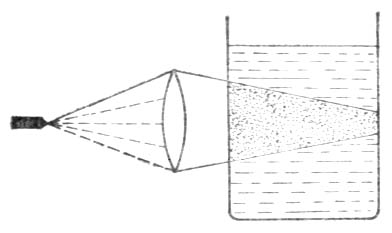
图9-6 丁铎尔现象

图9-6 布朗运动
(一)电泳
1.电泳
在一U形管中,加入棕色的氢氧化铁溶胶(图9-7左),然后插上电极并通直流电,阴极附近颜色逐渐变深,表示氢氧化铁胶体粒子向阴极移动(图9-7右)。如果在U形管中换上硫化砷溶胶并通电,胶体粒子向阳极移动。这种胶体粒子在电场作用下向阳极或阴极移动的现象叫电泳。
2.胶粒带电的原因
(1)选择吸附由于溶胶胶核常常选择性地吸附作为稳定剂的某种离子,而使其表面带有电荷。溶胶胶核总是选择吸附与其组成相类似的离子。例如Fe(OH)3溶胶,其胶核吸附稳定剂FeO+CL-中的FeO+而带正电荷。
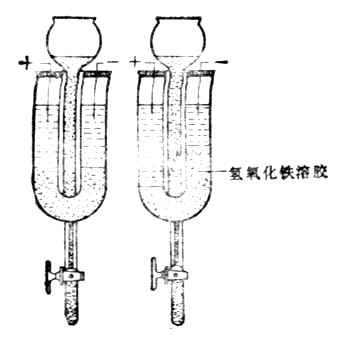
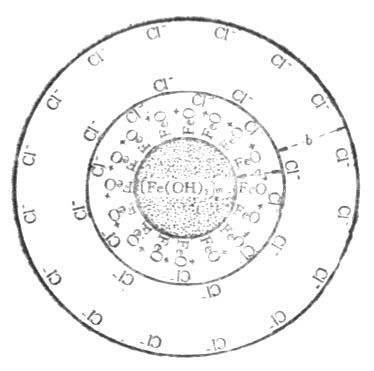
图9-7 氢氧化铁溶胶电泳向负极 图9-8 氢氧化铁胶团结构示意
图α-吸附层,b-扩散层
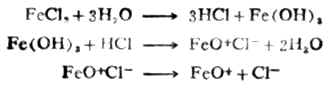
cl-则留在介质中。
在硫化砷溶胶中,其溶胶胶核吸附HS-而带负电荷。
As2O3+3H2S →As2S3+3H2O
H2S![]()
H++HS-
H+留在介质中。
(2)表面分子离解 胶体粒子与分散介质接触后,表面上的分子与介质作用而离解,某种离子将扩散到介质中去,因此胶体粒子带有和扩散离子符号相反的电荷。例如,硅胶的胶粒是由很多SiO2分子组成的。粒子表面上的SiO2分子和水接触形成硅酸H2SiO3,随后离解生成了SiO32-和H+,H+扩散到介质中成为反离子,胶体粒子则因保留有SiO32-而带负电荷。
3.胶团结构
现以Fe(OH)3溶胶为例来说明胶团的结构(图9-8)。
氢氧化铁溶胶是由许多Fe(OH)3分子构成的,其中心部分叫胶核。胶核的外边是由FeO+和一部分CL-所形成的吸附层,胶核和吸附层统称为胶粒。另一部分CL-借扩散作用而分布于离胶核较远处,形成扩散层。带有相反电荷的吸附层和扩散层电荷符号相反,电量相等,所以胶团是电中性的。胶团的结构可用下式表示。
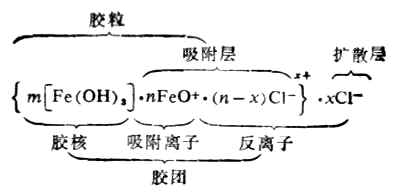
Fe(OH)3胶粒包括胶核(设为m个Fe(OH)3分子组成)和吸附层。胶粒和扩散层合称为胶团,胶团分散在介质中乃是胶体体系。
(二)溶胶的稳定性和聚沉
由于溶胶是高度分散的多相体系,胶粒有自动聚结的趋势,是一个聚结不稳定体系。但在某种条件下,它又具有聚结的稳定性,胶粒并不合并变大。决定聚结稳定性的主要因素是溶胶胶粒表面的双电层结构,它使胶粒在碰撞时不致相互接触,同时双电层有水化离子,好像胶粒外面包上一层水化膜或溶剂化膜,这层膜就起到阻碍胶粒合并的作用。
凡是使溶胶的分散度降低,分散相颗粒变大,最后从介质中沉淀析出的现象叫聚沉。促使溶胶聚沉的因素有电解质,反电荷的胶体,温度等。溶胶对电解质的影响非常敏感,这是由于电解质中反离子的加入促使胶粒周围的扩散层被“压缩”,扩散层厚度迅速变薄,当电解质的量达到一定程度后,扩散层消失,胶粒变成电中性,同时水化膜也随之消失,这样胶粒就能迅速凝集而聚沉。例如,在氢氧化铁中加入少量K2SO4溶液,溶胶内立即发生聚沉作用,析出氢氧化铁沉淀。
不同的电解质,对溶胶的聚沉能力是不同的,通常用聚沉值来衡量电解质对溶胶聚沉能力的大小。聚沉值是指一定溶胶,在一定时间内完全聚沉所需电解质的最低浓度(mmol·L-1)。聚沉值越小,表示聚沉能力越大。
可以使溶胶聚沉的电解质的有效部分是与胶粒带有相反电荷的离子,这些离子称为反离子。根据叔尔采-哈迪(Schulze-Hardy)规则,反离子的价数越高,聚沉能力也越大。一般说来,一价反离子的聚沉值在25-150之间,二价的约在0.5-2之间,三价的约在0.01-0.1之间。
对于给定的溶胶,反离子为1,2,3价的电解质,其聚沉值的比约为(1/1)6:(1/2)6:(1/3)6。
带有相反电荷的不同溶胶,可以相互聚沉。例如,将带有正电荷的氢氧化铁溶胶和带负电荷的As2S3溶胶混合,可以相互聚沉。
明矾的净水作用,是利用明矾的水解生成AL(OH)3正溶胶,而与带负电荷的胶体污物发生相互聚沉。
温度对溶胶的稳定性影响不大。温度升高时,由于溶胶的布朗运动增强,溶胶粒子之间的碰撞加剧,使溶胶的稳定性下降。
第三节 高分子化合物溶液
一、高分子化合物的概念
在自然界中,存在着大量高分子化合物。随着科学技术的发展,人们又合成了大量的高分子化合物。它们的共同特点是都具有很大的相对分子质量。如生物体中的蛋白质、核酸、糖原、淀粉、纤维等都是高分子化合物。它们是由许多重复的原子团或分子残基所组成,这些较小的原子团或分子残基叫做单体。如淀粉分子是由成千上万个葡萄糖分子残基按一定方式联结而成的。天然橡胶分子是由许多异戊二烯(CH2=C(CH3)-CH=CH2)的单体联结而成的大分子。
高分子化合物是大分子,其粒子的形状是复杂的。不同高分子化合物,在溶液中分子的形状往往也有很大的差异。例如,γ-球蛋白的分子是球形分子,脱氧核糖核酸分子是线形分子。线形分子在不同条件下形状有时也不一样,有的是比较伸展的线条形,有的则是卷曲的无规则线团。由于分子形状不同,它们在运动中的相互干扰作用也不一样。球形分子互相干扰少,而线形分子则互相干扰大,因此线形分子的粘度就大。
高分子化合物粒子具有许多亲溶剂基团,质点表面结合着一层溶剂。溶剂化后的粒子在溶液中成为一个运动单体,降低了运动速度,影响了溶液的粘度。
当高分子化合物为电解质时,粒子带有电荷。例如蛋白质类高分子化合物,由于含有酸性基团(-COOH)和碱性基团(-NH2),在水溶液中,因溶液PH值的差异,蛋白质大分子可以带正电荷或负电荷。
大分子的这些特性,往往影响到高分子化合物溶液的性质。
二、高分子化合物溶液的性质
高分子化合物溶液中,溶质和溶剂有较强的亲和力,两者之间有没有界面存在,属均相分散系。由于在高分子溶液中,分散质粒子已进入胶体范围(1-100nm),因此,高分子化合物溶液也被列入胶体体系。它具有胶体体系的某些性质,如扩散速度小,分散质粒子不能透过半透膜等,但同时也具有自己的特征。
(一)稳定性
高分子化合物溶液属均相分散系,可长期放置而不沉淀。在稳定性方面它与真溶液相似。
另外,由于高分子化合物具有许多亲水基团(如-OH,-COOH,-NH2等),当其溶解在水中时,其亲水基团与水分子结合,在高分子化合物表面形成了一层水化膜,使分散质粒子不易靠近,增加了体系的稳定性。
(二)粘度
液体的一部分流过其他一部分所受到的阻力叫粘度。高分子化合物溶液的粘度比一般溶液或溶胶大得多,高分子化合物溶液的高粘度与它的特殊结构有关。
高分子化合物常形成线形、枝状或网状结构,这种伸展着的大分子在溶剂中的行动困难,枝状、网状结构牵制溶剂,使部分液体失去流动性,自由液体量减少,故表现为高粘度。由于粘度与粒子的大小、形状及溶剂化程度直接相关,所以测定蛋白质溶液的粘度就能推知蛋白质分子的形状和大小。
(三)盐析
盐析作用在高分子化合物溶液中,加入足够量的中性盐时,可使高分子化合物从溶液中析出,这就是盐析作用。使一升溶液出现盐析现象所需中性盐的最小量称盐析浓度,单位为mol·L-1。盐析浓度一般都比较大,如血浆中各种蛋白质盐析所需的盐一般不少于1.3-2.5mol·L-1。
盐析效应的特点是,同价同符号的不同离子,对盐析效应的能力不一样。
已发现各种盐的盐析能力,其阴离子的能力有如下次序:
1/2SO42->OAc->CL->NO2->Br->I->CNS-
其阳离子则有如下次序:
Li+>Na+>K+>NH4+>1/2Mg2+
盐析作用的实质,主要是高分子化合物与溶剂(水)间的相互作用被破坏,盐的加入使高分子化合物分子脱溶剂化。盐的加入还使一部分溶剂(水)与它们形成溶剂(水)化离子,致使这部分溶剂(水)失去溶解高分子化合物的性能。溶剂(水)被电解质夺去,高分子化合物沉淀析出。所以盐类的水化作用越强,其盐析作用也越强。上述离子盐析能力顺序,实质上反映了离子水化程度大小的次序。
分段盐析盐析时,相对分子质量大的蛋白质比相对分子质量小的蛋白质更容易沉淀。利用这一原理可以用不同浓度的盐溶液使蛋白质分段析出加以分离。例如,(NH4)2SO4使血清中球蛋白盐析的浓度是2.0mol·L-1,清蛋白盐析浓度是3-35mol·L-1。在血清中加(NH4)2SO4达一定量,则球蛋白先析出,滤去球蛋白,再加(NH4)2SO4则可使清蛋白析出,这个过程叫分段盐析。
(四)高分子化合物溶液的保护作用
在溶胶中加入适量高分子化合物溶液,可以显著的增加溶胶的稳定性,这种现象叫保护作用。在制备银溶胶的过程中,加入蛋白质所得的胶体银(称为蛋白银),较普通银溶胶稳定。将所得蛋白银蒸干后能重新溶于水。蛋白银比普通银溶胶浓度更高,银粒更细,它含胶体银8.5%-20%,是极强的防腐剂。当保护蛋白质减少时,这些微溶性盐就要沉淀,因而形成结石。
一般认为高分子化合物保护作用的机理是,高分子化合物的大分子为溶胶胶粒所吸附,并在胶粒表面形成保护膜,因而大大削弱了胶粒聚结的可能性。
(五)膜平衡
当用半透膜将高分子电解质(R-Na+)溶液和低分子电解质(Na+CL-)溶液隔开,其中高分子离子(R-)不能透过半透膜,其它低分子离子(Na+、CL-等)都能自由透过半透膜,结果会有一定量低分子电解质离子透过膜进入高分子电解质溶液中,当小离子透过速度相等,并保持膜两侧电中性时,即达平衡状态,这时所发生的平衡现象叫膜平衡或董南(Donnan)平衡。
设高分子电解质溶液的浓度为c1,NaCL溶液的浓度为c2,设膜内外的体积相等。
因为膜内没有CL-,扩散结果使 一部分CL-通过半透膜进入膜内,设达到平衡时进入膜内的CL-浓度为x,根据整个溶液保持电中性原则,就必须有相等数目(x)的Na+同CL-一道进入膜内。

在平衡时,Na+ 和CL-进出膜的速度应相等,则:
ν进=k进[Na]外·[Cl]外
ν出=k出[Na]内·[Cl]内
因 ν进=ν出,且k进=k出
故 [Na+]内·[Cl-]内=[Na+]外·[Cl-]外
将相应浓度代入上式:x(c1+x)=(c2-x)2
整理后,得:
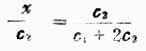
左边的x/c2说明膜外电解质进入膜内的百分率,称为扩散分数。
当c2c1,即外侧电解质过量时(c1可略去不计),则x/c2≈1/2说明电解质将平均分配在膜内外两侧。当 c2c1,即只有微量电解质时,x/c2≈0
(c2几乎等于零),说明电解质几乎留在外侧。
由此可见,在膜的一边存在的不能透过膜的高分子离子,对膜两侧的电解质浓度分布有很大的影响。当膜内高分子离子浓度很大时,电解质在膜两侧浓度分布的差值也很大。这时就表现为膜对Na++CL-好象完全不能透过,从而纠正了单纯从膜孔大小来解释生理上细胞膜对离子有选择透过性的看法。但是生物体内的活细胞膜的结构比较复杂,活细胞处于不断代谢过程中,故生物细胞膜是一种动态的体系,其组成、结构和性质也可随时改变,因此,在研究生理上膜的作用时,不能把它当作一种简单的半透膜来对待。
第四节 凝胶
在一定条件下,使高分子溶质或胶体粒子相互连接,形成空间网状结构,而溶剂小分子充满在网架的空隙中,成为失去流动性的半固体状体系,称为凝胶。这种凝胶化的过程称为胶凝。
一、凝胶的形成
当加酸于硅酸钠(水玻璃)后,可制成硅酸凝胶。将琼脂溶于热水中,配成2%琼脂高分子溶液,放冷后便形成凝胶。琼脂凝胶是一种常用的培养细菌的凝胶。
凝胶的形成是由于线形或分枝形高分子化合物或凝胶粒子连接起来形成的线状结构,经相互交联构成立体网架结构。溶剂分布在网眼之中,使其不能自由流动,成为半固体状。可见凝胶是处于溶液和固体高分子化合物之间的中间状态,兼有两者的性质,并有重要的实际意义。
生物体内的肌肉、脑髓、软骨、指甲、毛发、细胞膜等都是凝胶。
二、凝胶的几种性质
(一)弹性
凝胶的特点是具有网状结构,充填在网眼里的溶剂不能自由流动,而相互交联成网架的高分子或溶胶粒子仍有一定柔顺性,使凝胶成为弹性半固体。
各种凝胶在冻态时(溶剂含量多的叫冻)弹性大致相同,但干燥后就显出很大差别。一类凝胶在干燥后体积缩小很多,但仍保持弹性,叫做弹性凝胶。另一类凝胶烘干后体积缩小不多,但失去弹性,并容易磨碎,叫脆性凝胶。肌肉、脑髓、软骨、指甲、毛发、组成植物细胞壁的纤维素以及其它高分子溶液所形成的凝胶都是弹性凝胶。而氢氧化铝、硅酸等溶胶所形成的凝胶则是脆性凝胶。
(二)膨润(溶胀)
当弹性凝胶和溶剂接触时,便自动吸收溶剂而膨胀,体积增大,这个过程叫膨润或溶胀。有的弹性凝胶膨润到一定程度,体积增大就停止了,称为有限膨润。例如,木材在水中的膨润就是有限膨润。有的弹性凝胶能无限的吸收溶剂,最后形成溶液,叫无限膨润。例如,牛皮胶在水中的膨润就是无限膨润。
(三)离浆(脱水收缩)
新制备的凝胶搁置较久后,一部分液体可自动地从凝胶分离出来,而凝胶本身的体积缩小,这种现象叫做离浆,又叫脱水收缩。例如,硅酸冻放在密闭容器中,搁置一些时间,冻上就有水珠出现。血块搁置后也有血清分出。离浆本质上是膨润的相反过程,其发生的原因是由于高分子之间继续交联的作用将液体从网状结构中挤出。
第十章 有机化合物概述
一、有机化学和有机化合物
有机化学是研究有机化合物的组成、结构、性质及其制法的一门科学。
人们在很早以前就认识了有机化合物的应用和变化,但是对它们的研究只是在近代才有较大的发展。从前人们把来源于有生命的动物和植物的物质叫做有机化合物,而把从无生命的矿物中得到的物质叫无机化合物。有机化合物与生命有关,所以人们认为它们是“有机”的,故称为有机化合物。实际上,有机化合物不一定都来自有机物,也可以以无机化合物为原料在实验室中人工合成出来。
大量的研究证明,有机化合物都含有元素碳,所以人们就把含碳的化合物叫做有机化合物。然而,除了碳以外,绝大数的有机化合物还含有氢,有的也含有氧、硫、氮和卤素等。所以,现在有人把有机化合物定义为碳氢化合物及其衍生物。此外,含碳的化合物不一定都是有机化合物,如一氧化碳,二氧化碳,碳酸盐及金属氰化物等,由于它们的性质与无机化合物相似,因此习惯上仍把它们放在无机化学中讨论。所以,有机化学和有机化合物的“有机”二字,已不反映其固有的涵义,只是历史上的原因迄今仍沿用罢了。有机化合物与无机化合物之间没有绝对的界限,也不存在本质的区别。然而,由于元素碳在周期表中的特殊位置,使得有机化合物在组成、结构和性质等方面有着明显的特点,所以有必要把有机化合物与无机化合物分别进行讨论。
有机化合物主要具有下面一些特点:
1.有机化合物数目繁多,且自成系统
组成有机化合物的元素甚少,除碳以外,还有氢、氧、硫、氮、磷及卤素等为数不多的元素。但有机化合物的数目却极为庞大,迄今已逾1000万种,而且新合成或被新分离和鉴定的有机化合物还在与日俱增。由碳以外的其他100多种元素组成的无机化合物的总数,还不到有机化合物的十分之一。有机化合物数目繁多,也是我们把有机化学作为一门独立的学科进行研究的理由之一。
有机化合物之所以数目众多,主要有两个原因:(1)碳原子彼此之间能够进行多种方式的结合,生成稳定的、长短不同的直链、支链或环状化合物;(2)碳是周期表中第二周期第四族的元素,不仅能与电负性较小的氢原子结合,也能与电负性较大的氧、硫、卤素等元素形成化学键。
有机化合物的数目虽然很多,但根据它们之间的相互关系,可以统一在一个完整的体系中。
2.热稳定性差,容易燃烧
与典型的无机化合物相比,有机化合物一般对热是不稳定的,有的甚至常温下就能分解。虽然大多数的有机化合物在常温下是稳定的,但放在坩埚中加热,即炭化变黑,并且在完全燃烧后不留灰烬(有机酸的盐类等除外)。这是识别有机化合物的简单方法之一。
3.熔点较低
有机化合物的熔点通常比无机化合物要低,一般在300℃以下就熔化。
4.难溶于水,易溶于有机溶剂
多数有机化合物,易溶于有机溶剂而难溶于水。但是当有机化合物分子中含有能够同水形成氢键的羟基、磺基等时,该有机化合物也有可能溶于水中。
5.反应速度慢,常有副反应发生
虽然在有机酸和有机碱中,也有一些电离度较大的物质,但大多数的有机化合物电离度很小。所以,很多有机反应,一般都是反应速度缓慢的分子间的反应,往往需要加热或使用催化剂,而瞬间进行的离子反应很少。另外,分解或取代反应都是在分子中的某一部位发生,且在大多数情况下,反应分阶段进行。所以,往往有副产物生成或能够分离出多种反应中间产物。
二、有机化学与医学
在全部的医学课程中,有机化学是一门基础课,它为有关的后续课程奠定理论基础。研究医学的主要目的是为了防病、治病,研究的对象是组成成分复杂的人体。组成人体的物质除水和一些无机盐以外,绝大部分是有机物。例如构成人体组织的蛋白质,与体内代谢有密切关系的酶、激素和维生素,人体贮藏的养分——糖原、脂肪等。这些有机化合物在体内进行着一系列复杂的变化(也包括化学变化),以维持体内新陈代谢作用的平衡。为了防治疾病,除了研究病因以外,还要了解药物在体内的变化,它们的结构与药效、毒性的关系,这些都与有机化学密切相关。
有机化学作为医学课程的一门基础课,它为生物化学、生物学、免疫学、遗传学、卫生学以及临床诊断等提供必要的基础知识。有关生命的人工合成,遗传基因的控制,癌症、艾滋病等的治疗都是目前医学和生物学正在探索的重大课题。在这些领域中也离不开有机化学的密切配合。
有机化学与人类的生产和生活有着十分密切的关系。它涉及数目众多的天然物质和合成物质,这些物质直接关系到人类的衣、食、住、行。利用有机化学可以制造出无数种在生活和生产方面不可缺少的产品。我们身上穿的衣服,工业上使用的汽油、柴油、橡胶、塑料、油漆、染料以及杀虫剂、昆虫信息素等都是有机化合物。很难设想,在人类生活的哪一个方面是不受有机化学的影响的。这种密切的关系就明显地反映在这门内容丰富的课程中。
三、组成有机化合物的化学键——共价键
典型的有机化合物与典型的无机化合物的本质差别在于组成分子的化学键不同。如上所述,有机化合物都含有碳,碳原子位于元素周期表第二周期第四族,它有四个价电子,在形成分子时,它既不易失去也不易得到四个电子使其成为惰性元素的电子结构。因此,碳与其它原子结合时,是采取各自提供数目相等的电子,作为双方共有,并使每个原子达到稳定的八隅体结构。这种由共享电子对所形成的键叫做共价键。由一对共享电子形成的键称为单键。由两对或三对共享电子所形成的键分别叫做双键或三键。双键和三键也叫做重键。它们是有机化合物中最常见的共价键。例如:
在上述分子中,有的含有碳氢(C-H)、碳碳(C-C)单键,有的含有碳碳(C=C)、碳氧(C=O)双键及碳碳(C≡C)三键。
四、碳原子的sp3、sp2和sp杂化轨道
杂化轨道理论已在第四章 讨论过了。本节仅对碳原子的杂化轨道作一简单介绍。
甲烃分子中的碳原子是sp3杂化的,杂化后的四个sp3轨道构成109°28′的夹角[图10-1(a)]。在甲烷分子中,碳原子的四个sp3杂化轨道分别与四个氢原子1s轨道重叠形成键角为109°28′的正四面体分子[图10-1(b)]。
(a) (b)
图10-1 四个sp3杂化轨道和甲烷
成键情况
图10-2 由sp3-s和sp3-sp3形成的碳氢o键和碳碳o键
烷烃分子中的碳氢键和碳碳键是碳原子的一个sp3杂化轨道与氢原子的1s轨道或另一个碳原子的一个sp3杂化轨道重叠而成(图10-2)。这样形成的碳氢单键和碳碳单键,其电子云具有圆柱状的轴对称,叫做σ键。由于它是轴对称的,所以用单键相连的碳氢原子或碳碳原子可以围绕轴自由旋转。
乙烯分子中的碳原子与甲烷的碳原子不同,它是sp2杂化的。也就是说,碳原子的三个p轨道中的两个参与杂化,而另一个p轨道未参与杂化。杂化后生成了三个相同的sp2轨道。这三个轨道轴在同一个平面上,互成120°的角。另一个未参与杂化的p轨道的对称轴垂直于这个平面。
在乙烯分子中,碳原子的三个sp2杂化轨道中的两个同氢原子的1s轨道重叠形成碳氢σ键。未参与杂化的两个p轨道用侧面互相重叠形成一个π键(图10-3)。
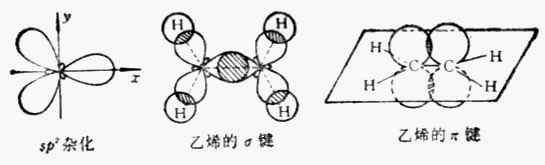
图10-3 sp杂化轨道及乙烯的o键和π键
所以,双键是由一个σ键和一个π键组成的。
碳原子的2s轨道同一个2p轨道杂化,形成两个相同的sp杂化轨道。它们对称地分布在碳原子的两侧,二者之间的夹角为180°。乙炔分子中的键就是由sp杂化轨道形成的。碳原子的一个sp杂化轨道同氢原子的1s轨道形成碳氢σ键,另一个sp杂化轨道与相邻的碳原子的sp杂化轨道形成碳碳σ键,组成直线结构的乙炔分子。没有参与杂化的两个p轨道与另一个碳的两个p轨道相互平行,且“肩并肩”地重叠,形成两个相互垂直的π键(图10-4)。
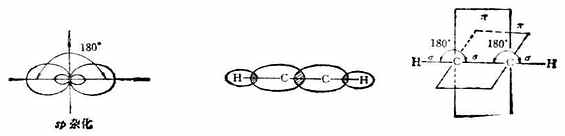
图10-4 sp杂化轨道及乙炔的o键和π键
五、有机化合物分子的结构
(一)分子式和构造式
分子式是以元素符号表示分子组成的式子。由于它不能表明分子的结构,因此在有机化学中应用甚少。分子结构的涵义包括:(1)分子中各原子的排列次序;(2)分子中各原子间相互结合的方式;(3)分子中各原子在空间的排布。只表示分子中各原子的排列次序及结合方式的式子叫做构造式。例如分子组成是C2H6O的化合物可以是构造不同的两个化合物。

构造式在有机化学中的应用最多,在推测和说明有机化合物的物理性质及化学性质时也极为重要。
(二)化合物的构型和构型式
构造式只是在平面上表示分子中各原子或原子团的排列次序和结合方式,是两维的。但是,分子结构是立体的,应当用三维表示法。例如最简单的甲烷分子,碳原子位于正四面体的中心,四个氢原子位于正四面体的四个顶点[图10-5(a)]。
为了形象地表明分子中各原子在空间的排布,往往借助分子模型表示。最常用的分子模型有两种,一是用各种颜色的圆球代表不同的原子,用木棍代表垢子间的键。这种用圆球和木棍做成的模型称为球棒模型[图10-5(b)]。另一种是根据实际测得的原子半径和键长按比例制成的模型,叫做比例模型[图10-5(c)]。它能更准确地表示分子中各原子间的相互关系。
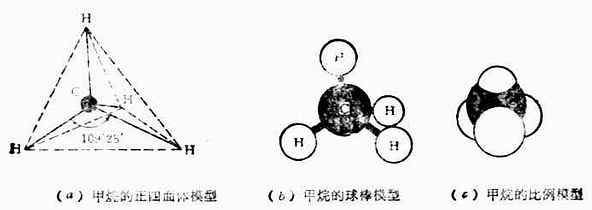
图10-5
在具有确定构造的分子中,各原子在空间的排布叫做分子的构型。为了在平面上表示有机化合物分子的立体结构,通常把两个在纸平面上的键用实线画出,把在纸平面前方的键用粗实线或楔形实线表示,在纸平面后方的键用虚线或楔形虚线表示(图10-6)。这种三维式就是构型式。
甲烷 正丁烷 丙酮
图10-6 甲烷、正丁烷和丙酮的三维表示法
但是,为了方便起见,在本书的大部分章节都用构造式。
六、共价键参数
第四章 中曾讨论过共价键的概念,这里再讨论一下共价键的性质。
键长、键角、键能及键的极性等参数可以表征有机分子中共价键的某些性质。它们对探讨有机化合物的结构和性质是十分重要的。
(一)键长
在正常的、未激发的分子中,各原子处于平衡的位置。这时两个成键原子核中心间的距离就是该键的键长,一般用纳米(nm)表示。键长取决于成键的两个原子的大小及原子轨道重叠的程度。成键原子及成键的类型不同,其键长也不相同。例如,C-C、C=C及C≡C的键长分别是0.154、0.133和0.121nm,即单键最长,双键次之,三键最短。
(二)键角
分子中某一原子与另外两个原子形成的两个共价键在空间中的夹角,叫做键角。它的大小与分子的空间构型有关。例如,烷烃的碳原子都是sp3杂化的,所以H-C-C或H-C-H的键角都接近于109°28′;烯烃是平面型分子,碳是sp2杂化的,H-C-H或H-C-C的键角接近于120°;炔烃是线型分子,碳的杂化方式是sp,所以H-C-C的夹角为180°。
键角的大小是影响化合物性质的因素之一。例如环丙烷的C-C-C键角比正常的C-C-C键角小,因此它不太稳定。
(三)键能和键离解能
在25℃和101.325kPa下,以共价键结合的A、B两个原子在气态时使键断裂,分解为A和B两个原子(气态)时所消耗的能量叫做键能。一个共价键断裂所消耗的能量又叫做共价键的离解能。对于双原子分子来说,键能就等于离解能。键的离解能反映了以共价键结合的两个原子相互结合的牢固程度:键的离解能愈大,键愈牢固。但对多原子分子来说,键能和键离解能是两个不同的概念。多原子分子的离解能是指断裂一个给定的键时所消耗的能量,而键能则是断裂同类型共价键中的一个键所需要的平均能量。
表10-1列举了一些化合物的键的离解能。一般地说,它对我们较为有用。
表10-1 一些化合物的键离解能
| 键 | D/kJ·mol-1 | 键 | D/kJ·mol-1 |
| H-H | 435 | n-C3H7-H | 410 |
| H-F | 444 | t-C3H7-H | 397 |
| H-CL | 431 | t-C4H9-H | 381 |
| H-Br | 368 | CH2=CH-H | 435 |
| H-I | 397 | CH2=CHCH2-H | 368 |
| F-F | 159 | CH3-CH3 | 368 |
| CL-CL | 243 | C2H5-CH3 | 356 |
| Br-Br | 192 | n-C3H7-CH3 | 356 |
| I-I | 151 | i-C3H7-CH3 | 351 |
| CH3-H | 435 | t-C3H7-CH3 | 335 |
| CH3-F | 452 | CH2=CH-CH3 | 385 |
| CH3-CL | 351 | CH2=CHCH2-CH3 | 301 |
| CH3-Br | 293 | n-C3H7-CL | 343 |
| CH3-I | 234 | i-C3H7-CL | 339 |
| C2H5-H | 410 | t-C4H9-CL | 331 |
| C2H5-F | 444 | CH2=CH-CL | 351 |
| C2H5-CL | 343 | CH2=CHCH2-CL | 251 |
| C2H5-Br | 289 | ||
| C2H5-I | 226 |
(四)键的极性
由两个相同的原子或两个电负性相同的原子组成的共价键,由于它们的共用电子对的电子云对称地分布于两个原子核之间,所以这种共价键是非极性的。如果组成共价键的两个原子的电负性不同,则形成极性共价键。它们的共用电子对的电子云不是平均地分布在两个原子核之间,而是靠近电负性较大的原子,使它带部分负电荷(用δ-表示);电负性较小的原子则带部分正电荷(用δ+表示)。例如,氯甲烷,![]() ,电负性较大的氯原子帯部分负电
,电负性较大的氯原子帯部分负电
荷,碳带部分正电荷。两个键合原子的电负性相差愈大,键的极性愈强。
键的极性能导致分子的极性。用极性键结合的双原子分子是极性分子;用极性键结合的多原子分子是否有极性,则与分子的几何形状有关。
键的极性能够影响物质的物理性质和化学性质。它不仅与物质的熔点、沸点和溶解度有关,而且还能决定在这个键上能否发生化学反应或发生什么类型的反应,并影响与它相连的键的反应活性。
七、共价键的断裂和反应类型
任何一个有机反应过程,都包括原有的化学键的断裂和新键的形成。共价键的断裂方式有两种:均裂和异裂。
(一)均裂
共价键断裂后,两个键合原子共享的一对电子由两个原子各保留一个。这种键的断裂方式叫均裂。
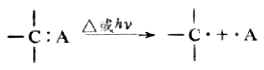
均裂往往借助于较高的温度或光的照射。
由均裂生成的带有未成对电子的原子或原子团叫自由基或游离基。有自由基参加的反应叫做自由基反应。这种反应往往被光、高温或过氧化物所引发。自由基反应是高分子化学中的一个重要的反应,它也参与许多生理或病理过程。
(二)异裂
共价键断裂后,其共用电子对只归属于原来生成共价键的两部分中的一部分。这种键的断裂方式叫做异裂。它往往被酸、碱或极性溶剂所催化,一般在极性溶剂中进行。
碳与其它原子间的σ键断裂时,可得到碳正离子或碳负离子:
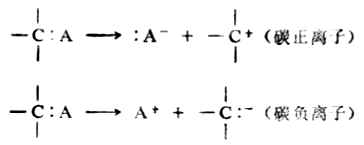
通过共价键的异裂而进行的反应叫做离子型反应,它有别于无机化合物瞬间完成的离子反应。它通常发生于极性分子之间,通过共价键的异裂而完成。
路易斯酸碱概念可以帮助我们对离子型反应的理解。按照路易斯的定义,接受电子对的物质为酸,提供电子对的物质为碱。
碳正离子和路易斯酸是亲电的,在反应中它们总是进攻反应中电子云密度较大的部位,所以是一种亲电试剂。碳负离子和路易斯碱是亲核的,在反应中它们往往寻求质子或进攻一个荷正电的中心以中和其负电荷,是亲核试剂。由亲电试剂的进攻而发生的反应叫亲电反应;由亲核试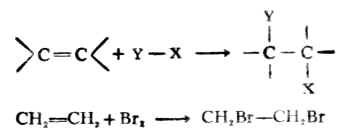
剂的进攻而发生的反应叫亲核反应。
有机化学反应还可根据产物与原料之间的关系分为取代反应、加成反应、消去反应、异构化反应和氧化还原等五种反应类型。
1.取代反应
连接在碳原子上的一个原子或官能团被另一个原子或官能团置换的反应叫取代。在反应中,该碳原子上有一个σ键断裂和一个新的σ键生成。
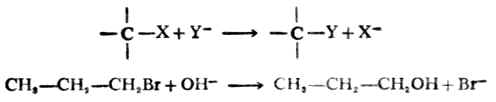
2.加成反应
两个原子加到一个π键上形成两个σ键的反应叫加成。
3.消去反应
一般地说,位于两个相邻碳原子上的两个σ键断裂,并在这两个原子之间形成一个π键的反应叫消去。
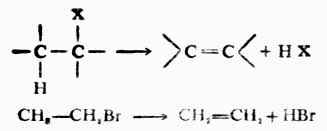
4.异构化反应
一个化合物通过原子或原子团的移动而转变为它的异构体的反应叫做异构化。
5.氧化还原反应
在有机化学中,氧化一般是指有机物得氧或脱氢的过程,还原是指有机物加氢或失氧的过程。因些,烃变成醇,醇变成酸都是氧化反应,它们各自的逆过程都是还原反应。
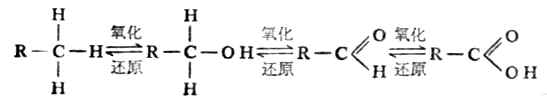
八、有机化合物的分类
按照形成有机分子构造骨架上的碳原子的结合方式,有机化合物可分类如下:

链状化合物之所以称为脂肪族化合物,是因为它们是最早从有长链结构的脂肪酸和脂肪中分离出来的,因此被认为是链状化合物的代表。芳香族化合物是具有苯环的一类化合物。在有机化学发展的初期,这类化合物是从树脂或香脂中得到的,而且它们大多数都具有芳香气味,所以称为芳香化合物。但是具有苯环的化合物不一定都有芳香气味,而有芳香气味的化合物也不一定含有苯环。所以,芳香族化合物中的“芳香”二字已失去其原有的涵义。
有机化合物的化学性质除了和它们的碳骨构造有关外,主要则决定于分子中某些特殊的原子或原子团。这些能决定化合物基本化学性质的原子或原子团叫官能团。由于含有相同官能团的化合物的化学性质基本相似,所以可以把官能团作为主要标准对有机化合物进行分类,以便于学习。
表10-2列举了一些有机化合物的类别及其官能团。
表10-2 有机化合物的分类及其官能团
| 官能团 | 名称 | 分类名 |
| >C=C< | 双键 | 烯烃 |
| -C≡C- | 三键 | 炔烃 |
| -OH | 羟基 | 醇(脂肪族)酚(芳香族) |
| -O- | 醚键 | 醚 |
| -CHO | 醛基 | 醛 |
| >C=O | 酮基 | 酮 |
| -COOH | 羧 基 | 羧酸 |
| -SO3H | 磺基 | 磺酸 |
| -NO2 | 硝基 | 硝基化合物 |
| -NH2 | 氨基 | 胺 |
| CN | 氰基 | 腈 |
| -X(F,CL,Br,I) | 卤素 | 卤代物 |
烷烃没有官能团,但各种含有官能团的化合物可以看作是它的氢原子被官能团取代而衍生出来的。
苯环不是官能团,但在芳香烃中,苯环具有官能团的性质。
第十一章 链烃
分子中只含有碳和氢两种元素的有机化合物叫碳氢化合物,简称烃。烃是有机化合物的母体,其它各类有机化合物可以看作是烃的衍生物。烃的种类很多,根据烃分子中碳原子互相连接的方式不同,可将烃分为两大类;开链烃和闭链烃。
开链烃简称链烃,它的构造特征是分子中碳原子互相连接成不闭合的链。链烃按分子中所含碳与氢的比例不同分为饱和链烃和不饱和链烃。饱和链烃又称烷烃。不饱和烃包括烯烃、二烯烃和炔烃等。
闭链烃分子中的碳原子连接成闭合的环,所以又叫环烃。环烃可分为脂环烃和芳香烃两类。
各类烃的分子构造特征和实例如下:
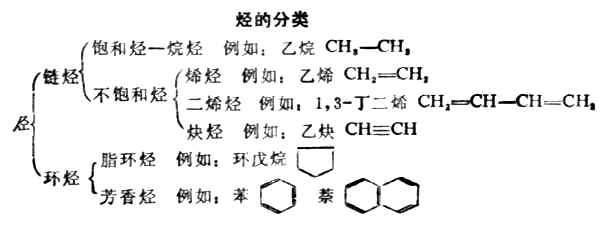
第一节 烷烃
一、烷烃的构造
烷烃的构造特点是其中的碳原子与碳原子都以单键相结合,其余价键都和氢原子相连接,含有一个、两个和三个碳原子的烷烃构造如下;
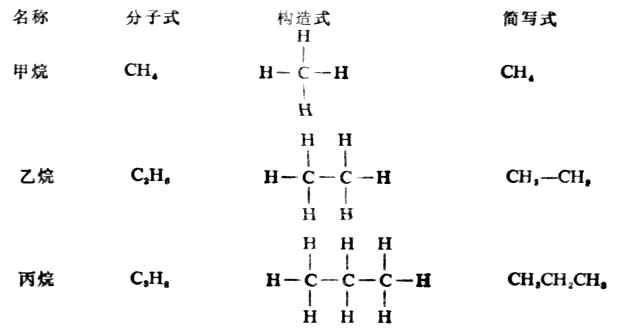
其它烷烃的构造与乙烷、丙烷相似。除甲烷外,烷烃分子中的各个碳原子上所连的四个原子或原子团不尽相同,所以其键角稍有变化,但仍接近于109°28′,因为这样的空间排布,能量最低,体系最稳定。这些分子中碳原子与碳原子连结成链状,其分子的形状是一系列共享一个顶点的四面体。如乙烷(图11-1)
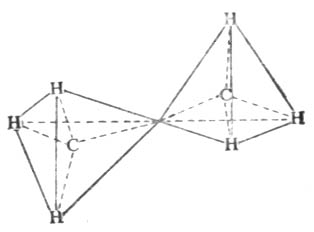
图11-1 乙烷的链状结构
二、烷烃的同系列和通式
根据烷烃的构造特点和它的原子组成可知,最简单的烷烃是含有一个碳原子的甲烷CH4,其次是含有两个碳的乙烷C2H6。按烷烃分子中碳与氢原子数可排列如表11-1。
表11-1 烷烃的同系列
| 碳原子数 | 分子式 | 同系列差 |
| 1 | CH4 | CH2 |
| 2 | C2H6 | |
| 3 | C3H8 | CH2 |
| 4 | C4H10 | CH2 |
| 5 | C5H12 | CH2 |
| … | … | |
| n-1 | CnH2(n-1)+2 | CH2 |
| n | CnH2(n+2) |
从表11-1可见,任何相邻的两个烷烃在分子组成上都相差CH2,这叫做同系列差。这样的一系列化合物叫做同系列。同系列中的化合物互称同系物。同系列在有机化学中的重要性在于同系物具有相似的化学性质,其物理性质一般随碳原子数目的增减表现出有规律的变化,对学习及研究有机化合物带来了很大方便。但是,如果碳原子数目相差过多,其性质也会表现出较大的差异。因此,在运用同系物的概念时,既要考虑到它们的共性,也要注意其个性。
从同系列中可以看出,烷烃分子中的碳和氢原子数间有一定的关系。如果碳原子数为n,则氢原子数即为2n+2。因此,烷烃的分子组成通式是CnH2n+2。
三、烷烃的同分异构现象和构象
(一)碳链异构
一种物质只能有一种特定的构造。因此,要了解有机物的特性和反应,常常要研究它们的构造。在研究烷烃的同系列时,发现随着碳原子数的逐渐增加,会出现同分异构现象。例如:分子式为C4H10的烷烃,碳原子的连结方式有两种可能,其构造式分别为:
分子式为C5H12的烷烃,碳原子的连结方式则有三种可能,其构造式分别为:
像这样具有相同的分子式,而有不同的构造的化合物互称同分异构体,简称异构体。若分子式相同,由于碳链构造的不同而产生的异构体叫做碳链异构体,例如,正丁烷和异丁烷;正戊烷、异戊烷和新戊烷。这种异构现象由于组成分子的原子或原子团连结次序不同引起的,所以属于构造异构。随着分子中碳原子数目的增加,同分异构体的数目会很快地增加,如表11-2。
表11-2 随着碳原子的增加异构体数目增长的情形
| 碳原子数 | 分子式 | 异构体数目 | |
| 1 | CH4 | ||
| 2 | C2H6 | ||
| 3 | C3H8 | ||
| 4 | C4H10 | 2 | |
| 5 | C5H12 | 3 | |
| 6 | C6H14 | 5 | |
| 7 | C7H16 | 9 | |
| 8 | C8H18 | 18 | |
| 9 | C9H20 | 35 | |
| 10 | C10H22 | 75 | |
| 15 | C15H32 | 4 347 | |
| 20 | C20H42 | 366 319 | |
| 40 | C40H82 | 62 491 178 805 831 | |
烷烃中碳链构造的不同主要是由碳原子之间的结合方式的不同引起的。在烷烃中碳原子与碳原子之间可能有四种结合方式,因此把碳原子分为伯(以1°表示)、仲(2°)、叔(3°)、季(4°)四类。 .
只与另外一个碳原子直接相连的碳原子,如上式中的C-1,5,6,7,8叫做伯碳原子;若碳原子与另外两个碳直接相连如-4,叫做仲碳原子;与另外三个碳原子直接相连的碳如C-3叫做叔碳原子;与另外四个碳原子直接相连的碳如C-2叫做季碳原子。
连在伯、仲和叔碳原子上的氢,分另称为伯、仲和叔氢原子。不同类型的氢原子的反应性不同。
(二)构象
有机物的分子中,以单键(σ键)相连结的两个碳原子,通过沿C-C单键的旋转,可使这两个碳原子上的原子或原子团在空间有不同的排布方式。每一种排布方式,都是有机物分子在空间的一种构象。具有一定构型的分子,仅由于围绕单键旋转,使分子中各原子在空间有不同的排布,称为构象。
1.乙烷的构象
乙烷是含有碳碳单键的最简单的化合物。当两个碳原子围绕C-C键旋转时,两个碳原子上的两组原子之间可以相对处于不同的位置,出现无数的空间排布方式,每一种空间排布方式就是一种构象。
不同的构象可用透视式或纽曼投影式表示。(Ⅰ)和(Ⅱ)是乙烷的两种典型构象。
纽曼投影式中,离观察者较远的碳原子用圆圈表示,它的三个C-H键用圆圈上的实线表示;离观察者较近的碳原子用圆心的点表示,它的三个C-H键则用与圆心相连的三条实线表示。
(Ⅰ)式中两组氢原子处于交叉的位置,这种构象叫做交叉式。式中两组氢原子彼此相距最远,相互斥力最小,能量最低,因而稳定性最大。这种构象是优势构象。(Ⅱ)式中,两组氢原子两两相对重叠,这种构象叫重叠式。在重叠式构象中,非键合氢原子间距离最近,排斥作用最大,这种构象具有较高的内能,是一种不稳定的构象。在室温时,乙烷分子是交叉式、重叠式以及介于它们两者之间的许多构象的平衡混合物,不易分离。
2.正丁烷的构象
正丁烷![]()
的构象要比乙烷复杂。当围绕正丁烷的C(2)-C
(3)键旋转时,可以有全重叠式,邻位交叉式、部分重叠式和对位交叉式等不同的典型构象。它们的透视式和纽曼投影工表示如下;
透视式 纽曼投影式
在正丁烷的构象中,对位交叉式的两个甲基相距最远,相互作用最弱,内能最低,是最稳定的现象。邻位交叉式的两个甲基相距较近些,所以稳定性稍差。部分重叠式的甲基和氢原子十分靠近,相互作用大,稳定性较邻位交叉式差。而在全重叠式中,由于两个甲基处于十分靠近的地位,相互作用最大,稳定性最差。因此这几种构象的内能高低次序为:全重叠式>部分重叠式>邻位交叉式>对位交叉式。
可见,正丁烷在一般情况下,对位交叉式是占优势的构象。
在链状化合物中,优势构象都是类似于正丁烷对位交叉式的构象。应该注意,分子主要以其优势构象存在,并不意味着其它的构象不存在,而是所占比例较小而已。
四、烷烃的命名
有机化合物的种类繁多,数目庞大,又有许多异构体。所以必须有一个合理的命名法,以便于识别。有机化合物的正确的名称不仅应表示分子的组成,而且要准确、简便地反映出分子的构造。因此命名法是有机化学的重要内容之一。烷烃的常用命名法有普通命名法和系统命名法。
(一)普通命名法
1.直链烷烃的命名
直链烷烃按碳原子数叫“正某烷”。十个及十个碳原子以下的烷烃分别用天干(甲、乙、丙、丁、戊、己、庚、辛、壬、癸)表示。例如,CH4四烷,C2H6乙烷,C3H8丙烷……C10H22癸烷。对含有十个碳原子以上的烷烃用汉语数字命名。例如,C11H24十一烷,C12H26十二烷,C20H42二十烷等。
2.含侧链烷烃的命名
![]()
且无其它支链的烷烃,则按碳原子总数叫做异某烷。例如,
(二)系统命名法
对构造比较复杂的化合物的命名可采用系统命名法。系统命名法可用于各种化合物的命名。
1.烷基
烃分子中去掉一个氢原子所剩下的原子团叫烃基。脂肪烃去掉一个氢原子所剩下的原子团叫做脂肪烃基,通常用R表示。烷烃的基叫做烷基,它的通式CnH2n+1烷基的命名根据烷烃而定。多于两个碳原子的烷烃,有可能衍生出多个不同的烷基。例如:
2.系统命名法
我国现用的系统命名法是根据IUPAC(International Union of Pure and Applied Chemistry)规定的原则,再结合我国汉语文字的特点而制定的。烷烃的系统命名法的主要之点是如何确定主链和处理取代基的位置。
(1)选择最长的连续的碳链为主链作为母体,叫某烷。较短的链为支链,作为取代基。
(2) 从靠近支链的一端开始,把母体烷烃的各个碳原子依次编号,以确定取代基的位次。取代基的位次号与名称之间用一短线相连,写在母体名称之前。例如:
(3)主链上连接几个不同的取代基时,则按“次序规则”(见本章第二节)将取代基的大小顺序列出,小者在前,“较优”者在后。
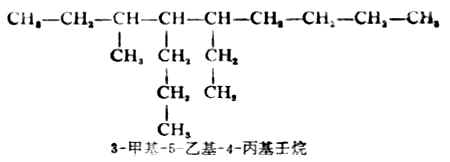
(4)若在主链上连有相同的取代基,则将取代基合并,用二、三……数字表示取代基的数目,写在取代基前面,各取代基的位次号仍须标出。例如:
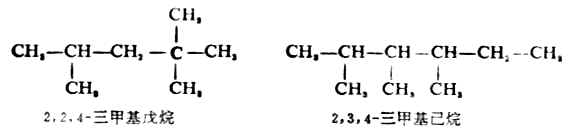
(5)若同时可能有几个等长的主链时,要选择含取代基最多的碳链为主链。例如:
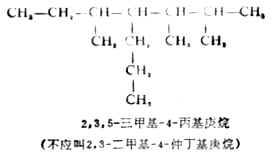
(6)若在主链的等距离两端同时遇到取代基且多于两个时,则要比较第二个取代基的位次大小,以取代基位次的代数和最小为原则。例如:
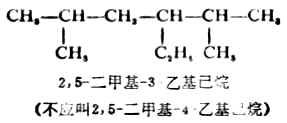
五、烷烃的物理性质
在有机化学中,物理性质通常是指化合物的聚集状态、气味、熔点(mp)、沸点(bp)、密度(ρ)、折射率(nΧD)、溶解度以及波谱数据等。
在室温和常压下,直链烷烃中从甲烷到丁烷都是气体;含5-15个碳原子的烷烃是液体;16及16个碳原子以上的是固体。不仅物态随着正烷烃同系物相对分子质量的增加而有明显的改变,其它一些物理性质如熔点、沸点、密度、折射率也呈现出规律性的变化。
从表11-3可以看出,正烷烃的熔点(前三个除外)和沸点基本上都是随着碳链的增长而变大。这是一个“量的变化会引起质的变化”的例证。
表11-3 正烷烃的物理常数
| 名称 | 熔点 | 沸点/℃ | 相对密度 | 折射率(n20D) |
| 甲烷 | -183 | -164 | 0.4661 | - |
| 乙烷 | -183 | -89 | 0.5462 | - |
| 丙烷 | -187 | -42 | 0.5853 | - |
| 正丁烷 | -138 | -0.5 | 0.5788 | - |
| 正戊烷 | -130 | 36 | 0.6262 | 1.3575 |
| 正己烷 | -95 | 69 | 0.6603 | 1.3751 |
| 正庚烷 | -91 | 98 | 0.6838 | 1.3878 |
| 正辛烷 | -57 | 126 | 0.7025 | 1.3974 |
| 正壬烷 | -51 | 151 | 0.7179 | 1.4054 |
| 正癸烷 | -30 | 174 | 0.7300 | 1.4102 |
| 正十一烷 | -26 | 196 | 0.7402 | 1.4172 |
| 正十二烷 | -10 | 216 | 0.7487 | 1.4216 |
| 正十三烷 | -6 | 235 | 0.7564 | 1.4256 |
| 正十四烷 | 6 | 254 | 0.7628 | 1.4290 |
| 正十五烷 | 10 | 271 | 0.7685 | 1.4315 |
| 正十六烷 | 18 | 287 | 0.7733 | 1.4345 |
| 正十七烷 | 22 | 302 | 0.7780 | (1.4369) |
| 正十八烷 | 28 | 316 | 0.7768 | (1.1390) |
| 正十九烷 | 32 | 330 | 0.7855 | (1.4529) |
烷烃的熔点变化没有沸点那样有规律,通常是随着分子的对称性增大而升高。分子越对称,它们在晶体中的排列越紧密,熔点就高。例如,正戊烷、异戊烷、新戊烷的熔点分别为-130℃、-160℃、-17℃。新戊烷的熔点最高。
烷烃的相对密度都小于1,且随着相对分子质量的变大而有所增加,最后接近于0.80左右。这也是由于分子间的作用力随着相对分子质量的增加而加大,使分子间的距离相对地减小,密度增大。
烷烃都不溶于水,但能溶于苯、氯仿、四氯化碳等有机溶剂。它们的溶解度随着相对分子质量的增加而减小。
六、烷烃的化学性质
烷烃的分子中没有官能团。除甲烷只有C-Hσ键外,所有烷烃分子中仅含C-C及C-Hσ键。
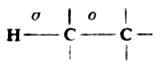
由于烷烃分子中的C-C键和C-H键都很强,需要较高的能量才能使之断裂(如断裂C-Cσ键需347.3kJ·mol-1,断裂C-Hσ键需380.7-435.1kJ·mol-1),所以一般情况下,烷烃具有极大的化学稳定性,与强酸、强碱及常用的氧化剂、还原剂都不发生化学反应。另外,碳原子和氢原子的电负性差别很小,分子中σ键的极性很弱,很难被极化,故烷烃的分子也不易和极性试剂发生共价键异裂的离子型反应。但是,在一定的条件下,例如使用高温、高压或催化剂,烷烃也能发生一些化学反应。
(一)卤化反应
烷烃和氯在黑暗中几乎不起反应。但是在日光照射、高温或催化剂的影响下它们能发生剧烈的反应,生成氯化氢和氯代烷烃。例如甲烷和氯气在强烈的日光或紫外光照射下反应猛烈,甚至发生爆炸。
![]()
在漫射的日光下则起一般的氯化反应,生成一氯甲烷、二氯甲烷、三氯甲烷(俗称氯仿)和四氯化碳。

烷烃的氯化过程是逐步的。每一步被取代出来的氢原子与另一个氯原子化合成为氯化氢。
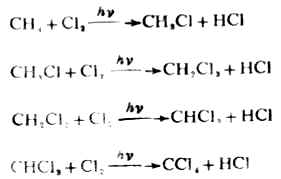
较高相对分子质量的烷烃氯化时,常生成复杂的混合物。
(二)氧化反应
烷烃在通常情况下是不被氧化的。但是它能在空气中燃烧(剧烈氧化)生成二氧化碳和水,同时放出大量的热能。因此烷烃可以用作燃料。
C2H6+3*1/2*O2→2CO2+3H2O △H=-1426kJ.mol-1
C6H14+9*1/2*O2→6CO2+7H2O △H=-4141kJ.mol-1
一些气态烃或极细微粒的液态烃与空气在一定比例范围内混合,点燃时会发生爆炸。煤矿井的瓦斯爆炸就是甲烷与空气混合物(体积比约为1:10左右)燃烧时造成的。
七、烷烃氯化的反应历程
化学反应历程是说明一个化学反应所经历的过程,也就是对每一个化学反应的各个中间步骤的详细描述。
已知烷烃的氯化反应是一种自由基反应。反应过程中,反应物的共价键发生均裂,生成自由基。一般地说自由基很不稳定,极易与其它化合物的分子发生反应,使自己变成稳定的分子,又使其它化合物的分子变为自由基,从而引起一连串反应(链反应)。例如,氯分子在光照下,均裂为氯自由基。
![]()
反应由此开始,所以这个步骤叫做链的引发。氯自由基很活泼,它夺取甲烷分子中的氢结合为氯化氢,产生甲基自由基。
Cl·+CH4→CHl+CH3·
CH3·和CL2反应,夺得一个氯原子,生成稳定的CH3CL,同时又有一个新的CL·产生。
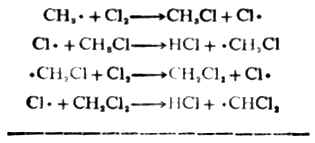
这个过程叫做链的增长。反应过程表明,只要在开始时有少量的氯原子(自由基),反应即会继续传递下去。
最后由于自由基相互结合形成稳定的化合物,反应便终止。如:
Cl·+Cl·→Cl2
CH3·+Cl·→CH2Cl CH3·+CH3·→CH3-CH3
上述过程叫做链的终止。
八、几种常用的烷烃混合物
常用的烷烃混合物,除了汽油、煤油和柴油外,还有以下几种产品。
(一)石油醚
石油醚是低级烷烃的混合物。沸点范围在30-60℃的是戊烷和己烷的混合物;沸点范围在90-120℃的是庚烷和辛烷的混合物。它们主要被用作有机溶剂。石油醚极易燃烧并具有毒性,使用及贮存时要特别注意安全。
(二)液体石蜡
液体石蜡主要成分是18-24个碳原子的液体烷烃的混合物,是呈透明液体。它不溶于水和醇,能溶于醚和氯仿中。液体石蜡性质稳定。精制的液体石蜡在医药上常用作肠道润滑的缓泻剂。
(三)凡士林
凡士林是液体石蜡和固体石蜡的混合物,呈软膏状半固体,不溶于水,溶于醚和石油醚。因为它不能被皮肤吸收,而且化学性质稳定,不易和软膏中的药物起变化,所以在医药上常用作软膏基质。
(四)石蜡
石蜡是C25-C34固体烃的混合物,医药上用作蜡疗、药丸包衣、封瓶、理疗等。
第二节 烯烃
一、烯烃的构造和通式
烯烃是指一类含有碳碳双键(![]()
烯烃分子中不是所有碳原子的价都饱和了,因
此它又称为不饱和烯。根据碳碳双键的数目,烯烃又可以分为单烯烃(含一个双键)、二烯烃(含两个双键)和多烯烃(含多个双键)。其中以单烯烃和共轭二烯烃最为重要。平时“烯烃”这个名字是代表单烯烃的意思,所以通常烯烃是指含有一个碳碳双键的不饱和烃而言。烯烃的通式是CnH2n。碳碳双键(![]() )是烯烃的官能团。
)是烯烃的官能团。
烯烃的碳碳双键(![]() )并不等于两个单键的加和,其中一个是O键一个是π键。π键是由碳碳双键的碳原子上未参与杂化的p轨道互相平行重叠形成的。
)并不等于两个单键的加和,其中一个是O键一个是π键。π键是由碳碳双键的碳原子上未参与杂化的p轨道互相平行重叠形成的。
二、烯烃的同分异构现象
(一)构造异构
由于存在双键,使烯烃的异构体数目比相应的烷烃多。如丁烷只有两种同分异构体,而分子式为C4H8的丁烯则有三种构造异构体。
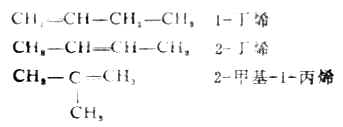
在烯烃的构造异构体中,有一种是碳链异构,即骨架不同的异构现象。如1-丁烯(或2-丁烯)与2-甲基-1-丙烯;另一种是由于双键的位置不同,如1-丁烯和2-丁烯。这种由于官能团位置的不同而产生的异构现象叫做位置异构。碳链异构与位置异构都属于构造异构。
(二)顺反异构
除上述两种异构现象外,由于以双键相连的两个碳原子不能绕σ键轴自由旋转,所以当两个碳原子上各连有两个不同的原子或基团时(如2-丁烯),双键上的四个基团在空间就可以有两种不同的排列方式,即两种构型。
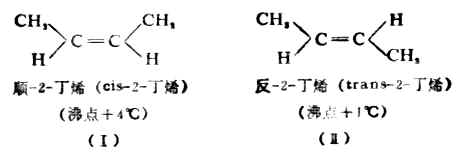
这两个异构体在原子或基团的连接顺序及官能团的位置上均无区别,即构造相同;它们的区别仅在于基团在空间的排列方式不同。在前一个化合物(Ⅰ)中,相同的基团(两个甲基或两个氢原子)在双键的同侧,叫做顺式异构体(词头cis-系拉丁字,意指在一边),而后者(Ⅱ)的两个甲基(或两个氢原子)则在双键的两侧,所以叫做反式异构体(词头trans-系拉丁字,意指交叉)。这种异构现象叫做顺反异构,是立体异构的一种,属于构型异构。立体异构是构造相同,但分子中的原子或原子团在空间排布不同的同分异构现象。构型异构是立体异构中的一种,是构造相同,构型不同的立体异构现象。
顺反异构体是两种不同的化合物。顺反异构体不仅在理化性质上不同,它们的生理活性也往往有差异,如具有降血脂作用的亚油酸,它的两个双键都是顺式构型。
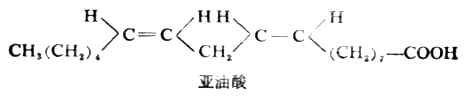
三、烯烃的命名法
烯烃的系统命名法的关键也是如何选择母体化合物和如何确定取代基的位置。
1.选择含有双键的最长碳链为主链作为母体。主链上的碳原子从靠近双键的一端开始编号,并把双键位置写在烯烃名称的前面。
![]()
2.把支链作为取代基,其位置、数目和名称按“次序规则”(见后)“较优”者后列出的顺序写在某烯之前。
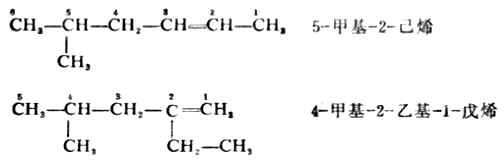
3.如双键在主链的中央,则编号从靠近取代基的一端开始。
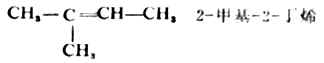
4.烯烃主链上的碳原子在十个以上时,烯字的前面应加一个“碳”字。
![]()
烯烃去掉一个氢原子生成一价基团,叫做烯基。碳链的编号应从含有自由键的碳原子开始。例如:

5.对于双键碳原子上连结有四个不同取代基的烯烃,其顺反异构体如用相同基团在双键的同侧或异侧的方法命名则遇到困难,例如:
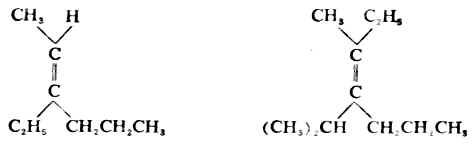
这时应根据Cahn-Ingold-Prelog的顺序规则对顺反异构体命名。次序规则是为了表达某些立体化学关系,须决定有关原子或原子团的排列次序时所用的方法。其主要内容如下:
(1) 将各种取代基的原子(与C=C的碳相连的原子)按原子序数大小排列,大者为“较优”基团。例如:I>Br>Cl>S>P>O>N>C>H(“>”表示“优于”)。
(CH3)2C->(CH3)2CH->CH3CH2->CH3-
假使第二个原子也相同时,则沿取代链逐次相比。例如:
![]()
此外应注意:一个原子序数大的原子要比两个或三个原子数小的原子优先,例如:
-CH2CL>-C(CH3)3
因此,此规则是比较原子序数的大小,而不是几个原子的原子序数之和。
(3)有双键或三键的基团:
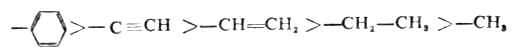
根据上述规则,一此常见的原子及原子团的优先顺序是:I>Br>Cl>-SO3H>F>
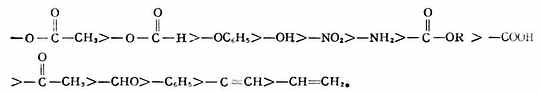
按次序规则决定双键上每个碳所连的两个原子或原子团的优先次序后,在下式中,如a>b,c>d,则当a与c在参考平面(π键所在平面,即与![]()
平面相垂直的平面)同侧
时,叫做Z型(Z取自德文Zusammen,在一起);当a与c在参考平面两侧时,叫做E型(E取自德文Entgegen,相反,相对)。Z,E写在括号里,放在化合物系统名称的前面。
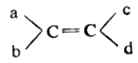
例1
例2
四、烯烃的物理性质
烯烃的物理性质如熔点、沸点、相对密度和溶解度等与相应的烷烃相似。常温时,C2~C4的烯烃是气体,C5~C18是液体,C18以上是固体。烯烃都难溶于水而易溶于有机溶剂。
表11-4 烯烃的物理常数
| 碳原子数 | 构造式 | 熔点/℃ | 沸点/℃ | 相对密度(d204) |
| 2 | H2C=CH2 | -169 | -102 | |
| 3 | CH3CH=CH2 | -185 | -48 | |
| 4 | CH3CH2CH=CH2 | -185 | -6.5 | 0.5946 |
| 5 | CH3(CH2)2CH=CH2 | -138 | 29 | 0.6411 |
| 6 | CH3(CH2)3CH=CH2 | -138 | 63 | 0.6734 |
| 8 | CH3(CH2)5CH=CH2 | -101 | 121 | 0.7149 |
| 10 | CH3(CH2)7CH=CH2 | -66 | 170 | 0.7408 |
| 12 | CH3(CH2)9CH=CH2 | -35 | 213 | 0.7584 |
| 14 | CH3(CH2)11CH=CH2 | -12 | 246 | 0.7852 |
| 18 | CH3(CH2)15CH=CH2 | 17 | 0.7891 | |
| 20 | CH3(CH2)17CH=CH2 | 28 | 341 | 0.7882 |
五、烯烃的化学性质
烯烃的官能团是![]() 。π电子云成块状分布于五个σ键所在平面的上下两侧,它
。π电子云成块状分布于五个σ键所在平面的上下两侧,它
与碳原子的结合不很牢固。由于烯烃具有易断裂和易极化的不稳定的π键,故使它具有不同于烷烃的特殊化学性质,如易发生加成、氧化、聚合等反应。
(一)加成反应
烯烃的加成反应是指在起反应时,烯烃分子中π键断裂,试剂中的两个原子或原子团分别加到双键的两个碳原子上的反应。双键加成的典型反应可表示为:
1.加氢
在普通情况下,烯烃与氢并不发生反应。如有适当的催化剂(Pt,Pd,Ni)存在,烯烃在液相或气相下能够氢化,变成相应的烷烃。例如:
![]()
这种在催化剂作用下的加氢反应,称为催化氢化。由于催化氢化反应可以定量地进行,所以可根据吸收量的计算来分析样品中双键的数目。
2.加卤素
烯烃与卤素(氯或溴)加成反应是亲电加成反应,这个反应在常温下就能很迅速地发生,例如:
如果用溴的四氯化碳溶液时,反应结束后溴的棕红色消失。常用这个方法来鉴定化合物是否含有碳碳双键。
3.加卤化氢
烯烃与卤化氢(HI,HBr,HCl)的加成反应也是亲电加成反应,生成卤代烷。例如:
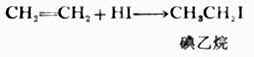
对HX一类试剂,加在双键上的两部分(H与X)不一样,所以叫做不对称试剂。乙烯是对称烯烃,它和不对称试剂加成产物只有一种。若不对称试剂和不对称烯烃发生加成反应时,加成方式就有两种可能,例如,丙烯与氯化氢加成时,产物可能是:
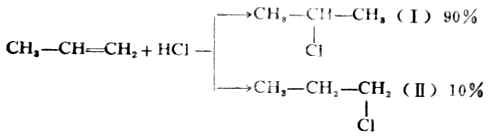
得到的产物主要是(Ⅰ)。也就是当不对称烯烃和卤化氢加成时,氢原子主要加在含氢较多的双键碳原子上。这个经验规律叫做马尔可夫规则(Markovnikov`s rule),简称马氏规则。
(二)氧化反应
烯烃很容易被氧化,主要发生在π键上。首先是π键断裂,条件强烈时σ键也可断裂。随着氧化剂及反应条件的不同,氧化产物也不同。常用的氧化剂是高锰酸钾溶液。
烯烃与中性或碱性高锰酸钾溶液作用时,被氧化为邻二醇。
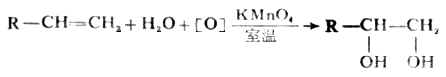
烯烃与酸性高锰酸钾溶液作用,碳链在双键处断裂,生成碳原子数较少的羧酸和酮等。例如:
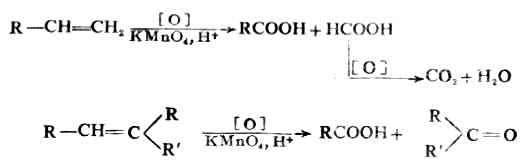
用高锰酸钾氧化烯烃,可用以检验双键的存在,亦可推断烯烃中双键的位置等。
(三)聚合反应
烯烃不仅能和其它化合物起加成反应,特别是低级的1-烯烃,在一定的条件(如高温、高压、催化剂)下还可在多个相同(可相似)分子间发生自身加成。例如:
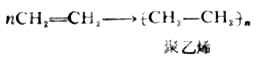
这种由低分子结合成更大分子的过程叫做聚合反应,生成的产物叫做聚合物或高聚物,进行聚合反应的原料烯烃称为单体。因为烯烃的聚合反应都是通过双键的断裂而使分子自相加成聚合起来,所以它又称加聚反应,简称加聚。
聚乙烯是白色或淡白色的固体物质,具有柔曲性、热塑性和弹性。聚乙烯的机械强度随制造方法而有所不同。高密度聚乙烯的韧性、抗张强度、耐热性以及对溶剂的抵抗能力均比低密度聚乙烯好。
聚乙烯塑料可作人工髋关节髋臼、输液容器、各种医用导管、整形材料和包装材料等。高聚物在医药上如人工材料等方面的应用,其意义也日渐增大。
六、烯烃的亲电加成反应历程
(一)烯烃与卤素的加成
乙烯和溴的加成是亲电加成,加成过程如下:非极性的溴分子由于受乙烯π电子或极性条件(如微量的水、玻璃容器的器壁等)的影响而极化变成了偶极分子
。加成反应分两步进行。第一步
中带正电荷的
Brσ+部分进攻乙烯分子,使C=C中的π键变弱,Br-Br中的σ键也变弱,生成一个带正电荷的σ络合物——环状溴鎓离子及Br-。
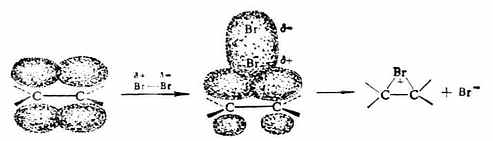
第二步Br-从溴鎓离子的背面进攻,得加成产物。
用实验方法可以证明是Brσ+而不是Brσ-首先与烯烃加成。
在乙烯与溴加成反应中,第一步进行得较慢,是决定反应速率的步骤。第二步是带相反电荷的两个离子间结合,所以反应较快。由于决定反应的一步是由亲电试剂发动进攻的,所以该反应是亲电反应。又由于整个反应是加成反应,故叫做亲电加成反应。
(二)烯烃与卤化氢的加成
烯烃与卤化氢(HCl,HBr,HI)或浓的氢卤酸的加成也是亲电加成。卤化氢是极性分子(![]()
),氢卤酸为H+X-。
加成反应的第一步是质子(H+)与烯烃生成碳正离子。这是决定反应速率的一步。
碳正离子中,带正电荷的碳是sp2杂化的,这个碳上有空的未参与杂化的p轨道。
第二步,X-与碳正离子结合,生成卤代烷
CH3CH2++X-→CH3CH3x
不对称烯烃(如丙烯)与HX的加成符合马氏规则。反应第一步生成的碳正离子有两种可能性:一种是(Ⅰ),即正电荷在中间一个碳原子(C-2)上;另一种是(Ⅱ),即正电荷在末端的碳原子(C-1)上。
实验表明,生成这两种碳正离子(Ⅰ及Ⅱ)所需的活化能不同,生成(Ⅰ)的活化能较小,生成(Ⅱ)的活化能较大;同时,(Ⅰ)与(Ⅱ)本身的能量大小也不一样,(Ⅰ)较小而(Ⅱ)较大。所以各种烷基碳正离子的稳定性次序为:3°>2°>1°>+CH3。2°碳正离子要比1°碳正离子更容易生成。也就是说异丙基碳正离子(Ⅰ)比丙基碳正离子(Ⅱ)更容易生成。因此,(Ⅰ)是丙烯与HX加成反应的主要中间体,即第二步反应的主产物是2-卤丙烷而不是1-卤丙烷。
七、诱导效应
有机化合物的性质,不仅决定于分子中原子的组成、连接顺序和方式,而且决定于分子中原子间的相互影响和空间排布。一般把原子间的相互影响归结为电子效应和空间效应。电子效应说明改变分子中电子云的分布对物质所产生的影响;空间效应说明分子中的空间结构对性质的影响。电子效应又可分为诱导效应和共轭效应。
在一个分子中引入一个原子或原子团以后,与这个原子或原子团相连的原子之间键的极性,将影响到分子中的其它部分,使分子的电子云密度分布发生一定程度的改变。这表现在分子中发生了σ电子的转移。这种转移是由成键原子的电负性不同引起的,并通过静电诱导作用沿着原子链中的σ键向某一方向传递下去,原子间的这种相互影响叫做诱导效应(I效应)。
诱导效应的方向以C-H键作为比较标准(I效应=0)。当其它原子或原子团(X或Y)取代C-H的氢原子后,成键的电子云密度分布不同于C-H键。如果X的电负性大于氢原子,则当X取代氢后,C-X键的电子偏向X,产生偶极:
箭头指的方向是电子偏移的方向。与氢相比,X具有吸电子性,我们把它们叫做吸电子基。由它们所引起的诱导效应叫做吸电子诱导效应或亲电诱导效应,一般用-I表示。如果Y的电负性小于氢原子,则当Y取代后,C-Y键的电子向碳偏移。与氢相比,Y具有斥电子性,我们把它们叫做斥电子基。由它们所引起的诱导效应叫做斥电子诱导效应,或叫供电诱导效应,用+I表示。
在多原子分子中,+I或-I诱导效应都可以沿着分子中原子的链(σ键)由近及远地传递下去。例如:
但是,诱导效应将随着传递距离的增加而迅速地减弱,一般经过3~4个键以后,影响已经很小了。
诱导效应只是使共价键中的电子云密度由于电负性的差异而引起的定向偏移,并不改变各原子的电子层结构,故只产生局部的正负电荷。
根据实验结果,一些原子或原子团电负性大小的次序如下:
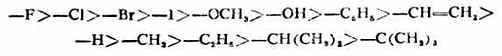
在H前面的原子或原子团是吸电子基,在H后面的是斥电子基。
上面所述的诱导效应是由分子内的静电作用产生的永久性的效应,由物质分子的结构所决定的,与外界条件无关,又叫做静态诱导效应。
马氏规则还可以用甲基的诱导效应来解释。丙烯是不对称烯烃,与乙烯不同。乙烯的双键的两个碳原子各连两个氢,其分子中π电子云的分布是均匀的。丙烯双键的两个碳原子中,有一个连两个氢,另一个连着氢和甲基。由于氢与甲基的电负性不同,氢的电负性大,甲基的电负性小,所以,丙烯分子中碳碳双键上的电子云密度比乙烯的大,同时π电子云的分布也不均匀:
式中的弯箭号“![]()
”表示一对π电子的转移方向,δ+及δ-表示双键两个碳原子上电荷的分布不均匀。因而,当亲电试剂H+向丙烯发动进攻时,其攻击部位是丙烯分子中带部分负电荷的碳。这样,生成的中间体是![]()
,加成的主要产物是
,符合马氏规则。
第三节 二烯烃
二烯烃是含有两个C=C双键的不饱和烯烃。它比含相同数目碳原子的烯烃少两个氢原子,分子组成的通式为CnH2n-2。
一、二烯烃的分类
二烯烃分子中的两 个C=C的位置和它们的性质有密切关系。根据两个C=C的相对位置,可将二烯烃分为三类,其中以共轭二烯烃最为重要。
1.累积二烯烃
两个双键与同一个碳原子相连,即含有![]() 构造体系的二烯
构造体系的二烯
烃。例如1,2-丁二烯CH2=C=CH-CH3。这类化合物数目不多。
2.孤立二烯烃
此类二烯烃的两个双键被两个以上的单键隔开,即含有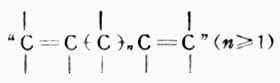 构造的二烯烃。例如:1,4-戊二烯CH2=CH-CH2-CH=CH2这类二烯烃的构造和性质与单烯烃相似。
构造的二烯烃。例如:1,4-戊二烯CH2=CH-CH2-CH=CH2这类二烯烃的构造和性质与单烯烃相似。
3.共轭二烯烃
两个C=C间有一个单键,即含![]()
结构体系(共轭体系
)的二烯烃。例如,1,3-丁二烯CH2=CH-CH=CH2。
二、共轭二烯烃的结构
在共轭二烯烃中,最简单、最重要的是1,3-丁二烯。
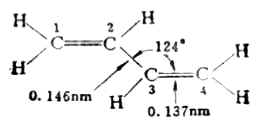
1,2-丁二烯
在1,3-丁二烯分子中,两个C=C的键长为0.137nm,比一般的烯烃分子中的C=C的键长(0.133nm)长,而C(2)-C(3)键长为0.146nm,它比一般的烷烃分子中的C-C的键长(0.154nm)短,这种现象叫做键长的平均化。
在1,3-丁二烯分子中,四个碳原子都是以sp2杂化轨道形成C-Cσ键。由于sp2杂化轨道的共平面性,所有的σ键都在同一平面内。此外,每个碳原子还留下一个未参与杂化的p 轨道,它们的对称轴都垂直于σ键所在的平面,因而它们彼此互相平行(图11-2)。1,3-丁二烯的C-2与C-3的p轨道也是重叠的,这种重叠虽然不象C-1和C-2或C-3和C-4轨道之间重叠程度那样大,但它已具有部分双键性质。在这种情况下,这四个p轨道相互平行重叠(图11-3),使四个p电子不是分别在原来的两个定域的π轨道中,而是分布在四个碳原子之间,即发生离域,形成了包括四个碳原子及四个π电子的体系。这种体系叫做共轭体系,这种键称为共轭π键。
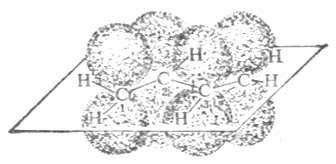
图11-2 1,3-丁二烯分子中p轨道的重叠
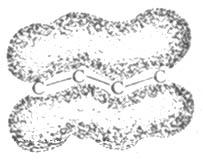
图11-3 1,3-丁二烯分子中共轭π键
像1,3-丁二烯这样的共轭体系是由两个π键组成,故称π-π共轭。由于共轭π键的形成,体系的能量降低,故共轭体系比相应的非共轭体系稳定。共轭体系有以下几个特点:(1)形成共轭体系的原子必须在同一个平面上;(2)必须有可以实现平行重叠的p轨道,还要有一定数量的供成键用的p电子;(3)键长的平均化;(4)共轭体系较稳定等等。
通过对1,3-丁二烯分子结构的分析,可知在共轭体系中,原子间的相互影响与诱导效应有本质上的不同。共轭体系中,由于π电子的运动范围遍及整个共轭体系。因此在受到极性试剂的进攻时,其影响可以通过π电子的运动迅速地传递到整个共轭体系。由于共轭体系的存在而引起的这种分子内原子间的相互影响叫做共轭效应。
三、二烯烃的命名
二烯烃系统命名法是以含有两个C=C的最长碳链为主链,作为母体二烯烃。从最靠近C=C的一端开始将主链上的碳原子编号,两个C=C的位次标明于母体二烯烃名称之前。取代基的位置随着主链上碳原子的编号位次而定。例如:
四、共轭二烯烃的化学性质
共轭二烯烃的化学性质和烯烃相似,可以发生加成、氧化、聚合等反应。但由于两个双键共轭的影响,显出一些特殊的性质。
共轭二烯烃可以与1或2mol卤素或卤化氢加成。例如:
1,4-二溴-2-丁烯
加第一分子溴的速率要比加第二分子溴快得多,反应常常终止在二溴代物阶段。而且生成的二溴代物也不是一种而是两种:3,4-二溴-1-丁烯和1,4-二溴-2-丁烯。3,4-二溴-1-丁烯是由溴和一个双键加成而生成的1,2-加成产物。1,4-二溴-2-丁烯是溴加在共轭双键两端而生成的1,4-加成产物。
1,3-丁二烯与1molHX加成时,也得到1,2-及1,4-加成产物。
共轭二烯烃的1,2-与1,4-加成产生的比例决定于反应条件。通常在较低温度及非极性溶剂中,有利于1,2-加成,在较高温度及极性溶剂中,有利于1,4-加成。例如,用己烷为溶剂时,在-15℃进行反应,1,3-丁二烯与溴 的1,2-加成产物占54%,1,4-加成产物占46%;如在60℃时反应,则1,4-加成产物占70%。
第四节 炔烃
炔烃是含有碳碳三键(-C≡C-)的链烃。
![]()
R-C≡CH或R`-C≡C-R”可代表它们的构造式,碳碳三键(-C≡C-)是炔烃的官能团。
炔烃也是不饱和烃,通式是CnH2n-2,与二烯烃或环烯烃相同。
一、炔烃的同分异构现象和命名法
炔烃由于碳链构造和三键位置的不同,也具有同分异构现象。不过因为三键支链的位置的限制,其异构体的数目要比碳原子数相同的烯烃为少。例如,含有五个碳原子的炔烃,只有三种同分异构体:
炔烃的命名法和烯烃相似。例如:
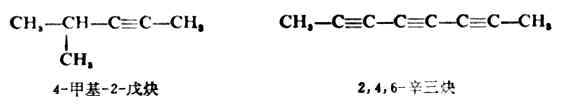
二、炔烃的物理性质
在正炔烃的同系列中,C2~C4的炔烃是气体,C5~C15的是液体,C15以上的是固体。炔烃的熔点和沸点也随着碳原子数目的增加而增高(表11-5)。
表11-5炔烃的物理常数
| 名称 | 构造式 | 熔点/℃ | 沸点/℃ | 相对密度(d204) |
| 乙炔 | HC≡CH | -81.8 | -83.6 | - |
| 丙炔 | CH3C≡CH | -101.51 | -23.2 | - |
| 1-丁炔 | CH3CH2C≡CH | -122.5 | 8.1 | - |
| 2-丁炔 | CH3C≡CCH3 | -32.3 | 27 | 0.691 |
| 1-戊炔 | CH3(CH2)C≡CH | -90 | 29.3 | 0.695 |
| 2-戊炔 | CH3CH2C≡CH | -101 | 55.5 | 0.714 |
| 1-己炔 | CH3(CH2)3C≡CH | -132 | 71 | 0.715 |
| 2-己炔 | CH3(CH2)2C≡CH | -88 | 84 | 0.730 |
| 3-己炔 | CH3CH2C≡CCH3 | -51 | 81.8 | 0.724 |
| 1-庚炔 | CH3(CH2)4C≡CH | -81 | 100 | 0.734 |
| 2-庚炔 | CH3(CH2)3C≡CCH3 | - | 112 | 0.748 |
| 3-庚炔 | CH3(CH2)2C≡CCH3 | - | 105 | 0.752 |
| 1-辛炔 | CH3(CH2)5C≡CH | -80 | 125.2 | 0.746 |
| 2-辛炔 | CH3(CH2)4C≡CCH3 | -60.2 | 137.2 | 0.759 |
| 3-辛炔 | CH3(CH2)C≡CCH2CH3 | -105 | 133 | 0.752 |
| 4-辛炔 | CH3 (CH2) 2C≡C(CH2)2CH3 | -102 | 131 | 0.751 |
| 1-壬炔 | CH3(CH2)6C≡CH | -65 | 160.7 | 0.760 |
| 2-壬炔 | CH3(CH2)5C≡CCH3 | - | 155747 | 0.769 |
| 3-壬炔 | CH3(CH2)4C≡CCH2CH3 | - | 154745 | 0.762 |
| 4-壬炔 | CH3(CH2)3C≡C(CH2)2CH3 | - | 152752 | 0.757 |
| 1-癸炔 | CH3(CH2)7C≡CH | -44 | 0.765 | |
| 3-癸炔 | CH3(CH2)5C≡CCH2CH3 | - | 0.765 |
三、炔烃的化学性质
炔烃的官能团是-C≡C-,它有两个π键,有较弱的亲核性(Lewis碱),其化学性质与烯烃有不少相似之处,例如能发生加成、氧化和聚和反应等。另外,-C≡C-H的C-Hσ键具有与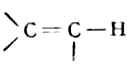
或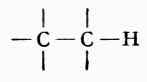
σ键不同的性质,即弱酸性很。
(一)加成反应
1.加氢
在催化剂(Pt,Pd或Ni)的作用下,炔烃与氢加成可生成烯烃,最后生成烷烃。
![]()
2.加卤素
炔烃能与氯或溴加成。反应分两步进行,第一次加1mol试剂,生成烯烃的二卤衍生物;第二次再加1mol试剂,生成四卤代烷。例如:
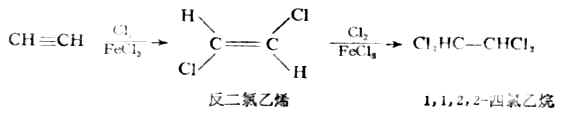
3.加卤化氢
炔烃和卤化氢的加成反应也是分两步进行的。
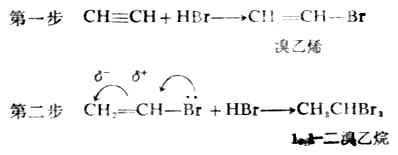
1,1-二溴乙烷
在生成的溴乙烯分子中,溴原子的未共用电子对与π键形成共轭体系(p-π共轭),这里共轭效应起了主要作用,而溴原子的诱导效应仅居次要地位。因此,当与第二个溴化氢分子加成时,溴原子继续加在已有一个溴的碳原子上,生成CH3CHBr2。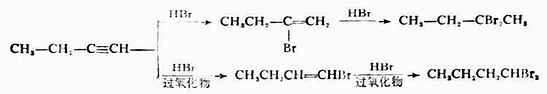
不对称炔烃与HX加成时遵从马氏规则。在有过氧化物存在下,不对称炔烃与HBr的加成反应则是反马氏规则的。
(二)氧化反应
炔烃氧化时,碳链在三键处断裂。例如,乙炔用高锰酸钾氧化时,生成二氧化碳。
![]()
其它炔烃用高锰酸钾氧化,生成羧酸。
![]()
从反应结果可以看到高锰酸钾的紫色消失,所以也可利用此反应检查碳碳三键。
(三)聚合反应
乙炔在不同的催化剂和反应条件下,发生各种不同的聚合反应,生成链状或环状的化合物。如乙炔若发生二分子聚合反应时,生成乙烯基乙炔CH2=CH-C≡CH;若在适当的催化剂存在下,三个分子的乙炔聚合成苯。

(四)炔化物的生成
连接在C≡C碳原子上的氢原子相当活泼,这是因为三键C是sp杂化,s成分占1/2,电负性比较强,使得Csp-H1sσ键的电子云更靠近碳原子,增强了C-H键极性,使氢原子容易离解,显示酸性。乙炔基阴离子能量低,体系稳定,所以乙炔分子CH≡CH中氢原子容易被金属取代,生成的炔烃金属衍生物叫做炔化物。例如,将乙炔通入硝酸银氨溶液或氯化亚铜氨溶液中,分别生成白色的乙炔银和砖红色的乙炔亚铜沉淀。
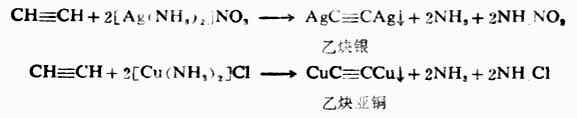
上述反应极为灵敏,常用来鉴定具有-C≡CH构造特征的炔烃,并可利用这一反应从混合物中把这种炔烃分离出来。而R`-C≡C-R型的炔烃不发生这两个反应。乙炔银和乙炔亚铜在湿润时比较稳定,在干燥时能因撞击或升高温度发生爆炸,所以实验完毕后,应立即加硝酸把它分解掉。
第十二章 环烃
环烃又称闭链烃。它们是具有环状构造的碳氢化合物。根据这类化合物的构造和性质又分为脂环烃和芳香烃。
第一节 脂环烃
脂环烃是具有链烃性质的环烃。脂环烃及其衍生物广泛存在于自然界中,例如有些地区所产的石油中含多量的环烷烃;一些植物中含有的挥发油(精油),其成分大多是环烯烃及其含氧衍生物。挥发油是中草药中重要的有效成分,有的可作香料。在自然界广泛存在甾族化合物都是脂环烃的衍生物,在人体中起重要作用。
一、脂环烃的分类和命名
脂环烃分为饱和环烃和不饱和脂环烃。饱和脂环烃称为环烷烃;不饱脂环烃又分为环烯烃和环炔烃。环烷烃和环烯烃较多见,环炔烃则较少见。依环数多少又可把脂环烃分为单环脂烃和多环脂烃。
环烷烃中只有一个碳环的称为单环烷烃,它的通式为CnH2n,与单烯烃互为同分异构体。单环烷烃可分为大环(环上的碳原子数≥12)、中环(8~11个碳)、普通环(5~7个碳)和小环(3~4个碳)。到目前为止,已知的大环有三十碳环,最常见的是五碳环(环戊烷)和六碳环(环己烷)。
单环烷烃的命名是根据组成环的碳原子数为环某烷。例如:
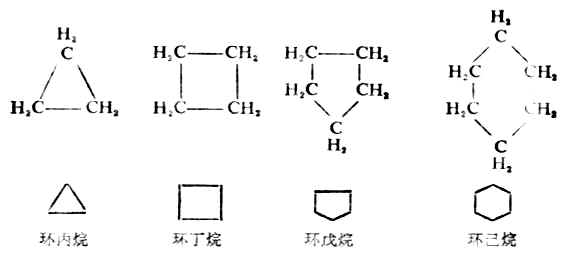
环上如有取代基时,取代基的位次尽可能采用最小数标出;若有不同取代基时,则以含碳最少的取代基作为1位。例如:
单环烯烃的命名,称为环某烯。标明双键位置以最小的数为原则。若有取代基时,取代基的位置数则以双键为准依次排列。例如:
脂环烃中具有几个环(常见的为双环)且共用一个、两个或两个以上碳原子的叫做多环脂烃。
二、环烷烃的结构
环烷烃中的碳原子也是sp3杂化的,它们的杂化轨道之间的夹角应为109°28′。但环丙烷的三个碳原子在一个平面上,C-C间的sp3杂化轨道没有在两原子核连线的方向上重叠,也就是没有达到最大程度的重叠,如图12-1。所以分子内存在一种达到最大重叠的倾向,这种倾向就叫做“张力”。因此内能较高,环不稳定。环丁烷的情况与环丙烷相似,分子中也存在着张力,但比环丙烷要稳定得多。
图13-1 环丙烷中sp3杂化轨道重叠示意图
五个碳以上的环烷烃环上的碳的碳原子并不都在同一平面上,C-C键角为109°28′左右。例如环戊烷的组成环的五个碳中只有四个是处在同一个平面上,另一个碳在平面外。这样的结构在不断地翻动着,处于平面外的碳沿着环迅速地变换。因而环戊烷是一个有一只角向上的近平面结构。

环戊烷
环己烷有四个碳原子在一个平面上,其它两个碳一个在此平面的上方,另一个在这个平面的下方(椅型);或者两个都在此平面的上方(船型)。
椅式 船式
环己烷的六个成环碳原子不共平面,C-C-C键角保持正常键角109°28′。通过键的扭动可 以得到椅型和船型两种不同的排列方式。
从不己烷的椅型构象和船型构象可以清楚地看出,椅型环己烷中所有相邻两个碳原子的碳氢键都处于正丁烷的邻位交叉式,非键合的C-1和C-3上的氢原子相距0.25nm,属于正常的原子间距。而船型环己烷的构象中,有两对碳原子(C-2与C-3;C-5与C-6)的键相互处于重叠式;同时又由于船头及船尾(C-1与C-4)的两个碳氢键是向内伸展的,相距较近,约0.183nm,比正常的非键合原子的间距小,故斥力较大,能量较高。实验证明,船型比椅型的能量高29.7kJ·mol-1左右。在常温下,环己烷是两种构象混合物,其中主要以椅型环己烷相聚在,船型只约占0.1%.
(纽曼投影式) (透视式) (透视式) (纽曼投影式)
椅型 (船型)
在椅型环己烷中,六个碳原子在空间分布于两个平面上,C-1、C-3、C-5在同一平面上,C-2、C-4、C-6在另一平面上。这样,环己烷中的十二个碳氢键可以分为两种类型,其中六个是垂直于平面而与对称轴平行的,叫直立键或a键,三个向上,三个向下,交替排列。另六个大致与环平面平行,实际与对称轴成±19.5°角,叫平伏键或e键(如图12-3).
在室温下,环己烷的一种椅型构象,可以通过C-C键的扭动很快地转变为另一种椅型构象.这时原来的a键就变成了e键,原来的e键变成了a,但对应平面上下关系不变(图12-4)。

图12-4 两种椅型构象的转变
对环己烷来说,这两种构象可以相互转变,但环上有取代基时情况不同。
一元取代的环己烷,其取代基可以a键,也可以连在e键上,形成两种不同的构象。一般以e键取代的构象能量较低,比较稳定。这是因为e键上的取代基与环上同侧的两个a键上的氢原子距离较远,斥力较小,较为稳定。例如,甲基环烷在室温时,当取代基在a键上时,则与环上同侧的两个a键上氢的距离较近,斥力较大,故不稳定。甲基环烷在室温时,当取代基在a键 上时,则与环上同侧的两个a键上的氢的距离较近,斥力较大,故不稳定。甲基以e键连结的分子约占95%,而以a键连结的分子仅占5%,且存在如下的动态平衡:
95%5%
当取代基越大时,这种以e键取代的构为主的趋势越大。
二元取代的环己烷可以有1-2-,1-3-和1.4-三种位置异构体,在每一种构体中,又有顺式与反式异构体。以1,2-二甲基环己烷为例,顺式异构体中两个甲基位于环平面的同侧,其相应的构象式为:
这两个构象式实际上是相同的,都是一个甲基连于e键,另一个甲基连于a键,能量相同,稳定性相同。
反式异构体中,两个甲基位于环的异侧,两个甲基可以都连在两个e键上(ee型),或都连于两个a键上(aa型)。显然ee型比较稳定。所以,反式1,2-二甲基环己烷主要以ee型的构象存在。
当两个取代基不相同时,如顺-1-甲基-4-叔丁基在e键,甲基在a键的构象为优势构象。

所以环己烷和取代环己烷的构象稳定性有如下规律:
①椅型构象比船型构象稳定。
②环己烷的一元取代物中,以e键取代物稳定;多元取代物中,以e-取代多的构象较稳定。
③环上有不同的取代基时,大的取代基结合在e键上的构象最稳定。
三、脂环烃的性质
(一)物理物质
脂环烃的物理性质与链烃相似。环丙烷和环丁烷在常温下是气体,环戊烷是液体,高级环烷烃是固体,如环三十烷的熔点为56℃。环烷烃的熔点、沸点和相对密度都比含同数碳原子的烷烃为高(表12-1)。
表12-1 一些环烷烃及烷烃的物理常数比较
| 化合物 | 熔点/℃ | 沸点/℃ | 相对密度(d204) |
| 环丙烷 | -127.6 | -32.9 | 0.720(-79℃) |
| 丙烷 | -187.69 | -42.07 | 0.5005(7℃) |
| 环丁烷 | -90 | 12.5 | 0.703(0℃) |
| 丁烷 | -138.45 | -0.5 | 0.5788 |
| 环戊烷 | -93.9 | 49.3 | 0.7454 |
| 戊烷 | -129.72 | 36.07 | 0.6262 |
| 环己烷 | 6.6 | 80.7 | 0.7786 |
| 己烷 | -95 | 68.95 | 0.6603 |
1.加氢
环烷烃可进行催化氢化反应,氢化时环被打开,两端碳原子与氢原子结合而生成链状的烷烃。在氢化过程中,由于环烷烃环的大小不同,反应的难易程度也不一样。
(二)化学性质
从化学键的角度来分析,环烷烃与烷烃相似;环烯烃和环炔烃分别与烯烃和炔烃相似。但是,由于脂环烃具有环状构造,小环烃出现的一些特殊的化学性质。主要表现在环的稳定性上,小环较不稳定,大环则较稳定。
1.加氢
环烷烃可进行催化氢化反应,氢化时环被打开,两端碳原子与氢原子结合而生成链状的烷烃。在氢化过程中,由于环烷烃环的大小不同,反应的难易程度也不一样。
2.加卤素
环丙烷在常温下,环丁烷在加热时分别与氯或溴发生加成反应,开环得1,3-或1,4-二卤代烷。
环戊烷及更高级的环烷烃与卤素不发生加成反应,而是进行自由基取代。例如:
3.加氢卤酸
环丙烷在常温时与氢卤酸发生加成反应得卤丙烷。环上有烷基取代的环丙烷衍生物与氢卤酸的加成符合马氏规则。碳环打开,氢原子加在连氢较多的碳原子上,而卤原子则加在连氢较少的碳上。
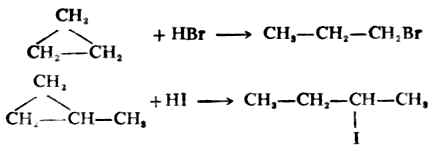
常温时,环丁烷、环戊烷及更高级的环烷烃与氢卤酸不起反应。
另外,若以强氧化剂在加热条件下与环烷烃作用时,则环断裂,生成二元羧酸。例如:
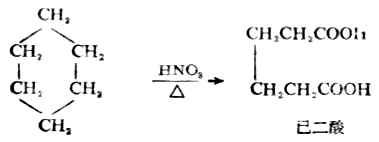
第二节 芳香烃
芳香烃科称芳烃,它是芳香族化合物的母体。这里所讲的芳香烃是指分子中含有苯环的烃类。苯是最简单最重要的芳香烃。
在芳香烃中,根据所含苯环数目的多少和连接方式,又可分为单环芳香烃和多环芳香烃两类。
单环芳香烃:
这类芳香烃分子中只含有一个苯环,如苯,甲苯、二甲苯等。
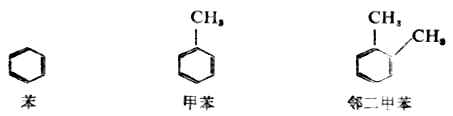
多环芳香烃:
分子中含有两个或两个以上的苯环,根据苯环的连接方式不同,又可分为三类:
多苯代脂烃这类芳香烃可看作是脂肪烃中两个或两个以上氢原子被苯取代的化合物,如二苯甲烷、三苯甲烷等。

联苯和联多苯分子中两个或两个以上的苯环直接互相连接,如联苯、多联苯等。

稠环芳香烃苯环通过共用相邻的碳原子相互稠合而成的芳香烃称为稠环芳香烃。如萘、蒽、菲等。
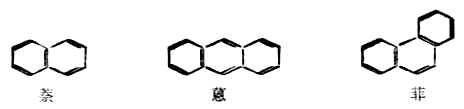
芳香烃是合成芳香族化合物的重要原料,而芳香族化合物又是医学、染料及国防等工业的重要物质。芳香烃主要来自石油C5-C8馏分的芳构化,即从石油加工中制取。
一、苯的结构
根据元素分析和相对分子质量的测定,证明苯的分子式C6H6。由苯的分子式可见,碳氢比和乙炔相同,都是1:1,它应具有不饱和性,但是事实并非如此。苯极为稳定,不易氧化,难起加成反应,但在催化剂的作用下,易发生取代反应。由此证明,苯的性质与不饱和烃大有区别。苯的这种性质来自苯的特殊结构。
1865年凯库勒首先提出了苯的环状结构,即六个碳原子彼此连结成环,每个碳原子上都结合着一个氢原子。为了满足碳的四价,凯库勒提出如下的构造式:
凯库勒的这种环状构造式在一定程度上反映了客观事实,如苯在一定条件下,催化加氢生成环己烷。这说明了苯分子的六个碳原子结合成环状结构。但凯库勒式还不能解释分子中虽含有三个双键,为什么不出现与烯烃相类似的加成反应。另外,苯的邻位二元取代物只有一种,而凯库勒的构造式却能有两种。

为了解释这种情况,凯库勒认为分子中的单、双键不是固定的,它们可以相互转变。
多年来,人们对于苯提出了多种构造式,但还没有一种能比较完善地表示它的结构。
经过现代物理方法的研究,证明苯分子中的六个碳原子都是sp3杂化的。每个碳原子各以两个sp2杂化轨道分别与另外两个碳原子形成C-Cσ键。这样六个碳原子构成了一个正六边形的环状结构。每个碳原子上的另一个sp2轨道,其电子云的对称轴在正六边形的平面上,这个sp2杂化轨道与氢原子的1s轨道,其电子云的对称轴在正六边形的平面上,这个sp2杂化轨道与氢原子的1s轨道形成C-Hσ。因此苯人子中的所有原子都在一个平面上,键角都是120°[图12-(a)],每个碳原子还有一个未参与杂化的pz杂化轨道[图12-(b)],它的对称轴垂直于此平面,能与相邻的两个碳原子上的pz轨道分别从侧面平行重叠,形成了一个闭合的共轭体系[图12-5(c)],在这个体系中,环上有六个碳原子和六个π电子,离域的π电子云完全平均化,体系能量低,比较稳定。π电子云成两个轮胎状[图12-5(d)],均匀分布在苯环平面的上下两侧。苯分子中的碳-碳键长也完全平均化,都是0.1393nm。这种具有6π电子闭合共轭体系,使得苯环具有高度的对称性和特殊的稳定性。由于形成了闭合共轭体系,无单、双键之分,故苯的邻位二元取代物只能有一种。
目前国内、外多采用凯库勒式![]() ,但不要理解为苯分子中存在单键和双键,另一种表示方法是用正六边形碳环中画一圆圈
,但不要理解为苯分子中存在单键和双键,另一种表示方法是用正六边形碳环中画一圆圈![]() (代表环状共轭π
(代表环状共轭π
键)的式子表示。
二、苯的同系物的异构现象和命名
苯的同系物是指苯分子中氢原子被烃基取代的衍生物。当苯环上只有一个取代基时,可以苯环为母体命名,烷基作取代基。若侧链为不饱和烃基(如烯基或炔基)等,则以不饱和烃为母体命名,苯环(苯基)作为取代基。例如:
当苯环上有两个取代基时,则有三种位置异构体。两个取代基的相对位置,可用邻(o)、对(p)和间(m)或数字表示。
当苯环上有三个或三个以上取代基时,它们的位置用数字表示。
芳香烃分子中的一个氢原子被去掉后,所余下的原子团称为芳基,常用Ar表示。例如:

三、苯及其同系物的性质
(一)物理性质
苯和它的常见同系物一般为无色的液体,不溶于水,易溶于有机溶剂。相对密度0.8-0.9。芳香烃一般都有毒性。液体芳香烃常用作有机溶剂。苯及其同系物的物理常数见表12-2。
表12-2 苯的同系物
| 名称 | 熔点℃ | 沸点℃ | 相对密度(d204) |
| 苯 | 5.5 | 80.1 | 0.8765 |
| 甲苯 | -95 | 110.6 | 0.8669 |
| 邻二甲苯 | -25.2 | 144.4 | 0.8802 |
| 间二甲苯 | -47.9 | 139.1 | 0.8641 |
| 对二甲苯 | -13.2 | 138.4 | 0.8610 |
| 乙苯 | -93.9 | 136.2 | 0.8667 |
| 连三甲苯 | <-15 | 176.1 | 0.8943 |
| 偏三甲苯 | -57.4 | 169.4 | 0.8758 |
| 均三甲苯 | -52.7 | 164.7 | 0.8651 |
| 正丙苯 | -101.6 | 159.2 | 0.8620 |
| 异丙苯 | -96.9 | 152.4 | 0.8617 |
(二)化学性质
由于苯及同系物分子中都含有苯环,故它们的化学性质与饱和烃具有明显的不同,具有特殊的“芳香性”。主要表现在取代、加成和氧化反应上,其中以取代反应为重要。
1.取代反应
在一定条件下,苯环上的氢原子易被其它的原子或原子团取代。
(1)卤代反应:在铁粉或卤化铁的催化下,氯或溴原子可取代苯环上的氢,主要生成氯苯或溴苯。
在同样的催化剂存在时,苯的同系物与卤素的反应比苯容易。一烷基苯与卤素反应主要是卤素取代烷基的邻位或对位上的氢原子。
如果不用催化剂,而是在日光或加热的条件下甲苯与氯气反应,则取代不是发生在苯环上,而是发生在侧链上,即甲基上的氢逐个地被氧化(自由基取代)。
每步反应都有氯化氢身生成。如果控制氯气的量,可以使反应停止在生成氯化芐的阶段。
在光照下,乙苯与氯的反应得到一个混合物。一般说来,在进行自由基卤代时,α-H比β-H容易被取代。乙苯与溴在日光下反应时,α-溴乙苯几乎是唯一产物,表明了自由基溴代时,溴对不同氢原子取代的选择性。
(2)硝化反应苯与浓硝酸及浓硫酸的混合物(混热)共热后,苯环上的氢原子被硝基(-NO2)取代,生成硝基苯。
在有机化合物分子中引入硝基的反应叫做硝化反应。
硝基苯不易继续硝化。如果用发烟硝酸和浓硫酸在95℃时,硝基苯可转变为间二硝基苯。
所以当苯环上带有硝基时,再引入第二个硝基到苯环上就比较困难;或者说,硝基苯进行硝化反应比苯要难。此外,第二个硝基主要是进入苯环上原有硝基的间位。
苯的同系物发生硝化反应时比苯要容易。硝基主要进入烷基的邻位及对位。
如果反应温度为50℃时,邻及对硝基甲苯继续硝化,主要得2,4-二硝基甲苯,后者在100℃时进一步反应,生成2,4,6-三硝基甲苯(INT),它是一种重要的炸药。
(3)磺化反应 苯与浓硫酸在75-80℃或发烟硫酸(SO3+浓H2SO4)在40℃时反应。苯环上的氢原子被磺酸基(-SO3H)取代,生成苯磺酸。
在有机化合物分子中引入磺酸基的反应叫做磺化反应。
苯磺酸继续磺化时,需要用发烟硫酸及较高温度,产生主要为间苯二磺酸。可见,苯环上已有了磺基后,再引入第二个磺基时比苯要难,而且第二个磺基主要进入原来磺基的间位。
苯的同系物的磺化反应比苯容易进行。例如,甲苯与浓硫酸在常温下即可发发生碘化反应,主要产生是邻及对苯磺酸。如在100-120℃时反应,则对甲苯酸为主要产生。
碘酸是有机强酸,易溶于水,其酸性可与无机强酸相比。
(4)傅-克反应:芳香烃在无水ALCL3作用下,环上的氢原子也能被烷基和酰基所取代。这是一个制备烷基烃和芳香酮的方法,称为傅瑞德尔-克拉夫慈反应,简称傅-克反应。
① 烷基化反应

② 酰化反应:

常用的酰基化试剂是酰卤,此外还可以用酸酐。
2.氧化反应
苯环本身很稳定,在一般情况下难以氧化。苯的同系物则能与一些氧化剂(如重铬酸钾的酸性溶液、高锰酸钾溶液)反应。这时,苯环的侧链被氧化,只要侧链上有α-H,无论侧链烷基长短如何,都被氧化为与苯相连的羧基。
叔丁基苯不含α-H,在上述条件下不被氧化。
在剧烈的条件下和催化剂存在时,苯环才被破坏。例如:
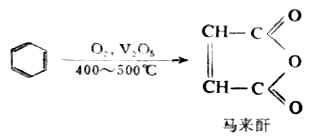
3.加成反应
环苯在一般条件下不容易发生加成反应。当在催化剂、高温或光的影响下,也可加成。
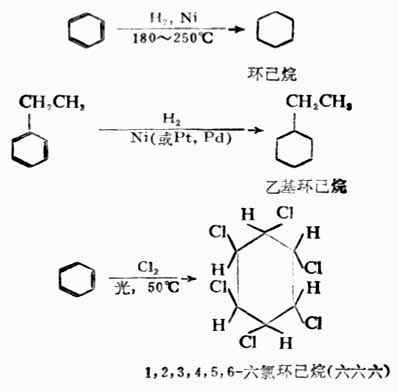
溴与苯可进行类似反应。
苯的同系物与卤素在日光下,不发生加成反应,而是在侧链上取代。
四、苯环上亲电取代反应的历程
苯及其同系物在苯环上的取代反应,包括卤化、硝化、磺化、烷基化及酰化等,是一个带正电荷的原子或原子团(E+)首先进攻苯环而进行的反应,故是一个亲电取代。它的整个过程用下式表示。
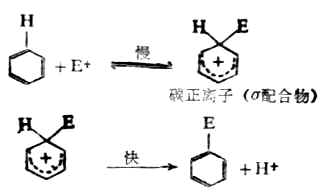
(一)卤化
苯与卤素在催化剂(例如FeCL3)存在下的卤化,是由亲电试剂发动进攻的。这个反应的亲电试剂与卤化铁生成的配合物。
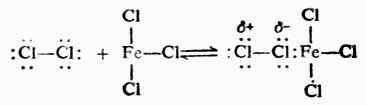
取代反应分两步进行。
第一步,亲电试剂进攻苯环的π电子与CL+生成C-CL键被亲电试剂进攻的碳原子变为sp3杂化,而破坏了原来的环状共轭体系。环上其余的五个sp2杂化的碳原子组成了一个共轭体系,这个体系包括五个碳和四个π电子,它带一个正电荷,连同环上的一个sp3碳原子构成σ配合物。
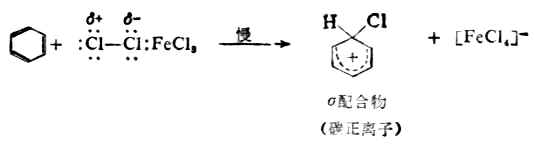
第二步,中间体碳正离子脱去一个质子,生成取代产物。
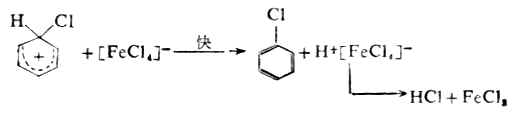
第一步是决定反应速率的一步,它是由亲电试剂对底物进攻,与烯烃的亲电加成的第一步相似。但在这里整个反应是取代,所以叫做亲电取代。第二步不同于烯烃的是从碳正离子脱去质子,而不是碳正离子与阴离子的结合,这是由于苯环比较稳定的缘故。
催化剂氯化铁促进氯分子极化,并与带负电荷的部分配合,使氯的亲电性加强。如果苯环上有强的活化基团,如羧基,卤化反应可不需加卤化铁。
(二)硝化
苯及同系物硝化反应的亲电试剂是硝金翁离子(![]()
)。在混酸中,它
是由浓硝酸与浓硫酸作用生成的。
![]()
硝金翁离子O=→O是很强的亲电试剂。
在有些情况下,硝化反应不用混酸而用硝酸。这时的硝金翁离子是通过下式生成的:
![]()
(三)磺化
苯及同系物磺化时,进攻试剂是亲电的三氧化硫。
![]()
三氧化硫是电中性的分子,但它发生极化:
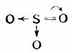
磺化反应可能分三步进行。
第一步,亲电试剂SO3的进攻,与苯生成σ配合物。这个σ配合物作为一个整体不带电荷,但环中的五个sp2碳及-SO-3两部分分别带一个正电荷信一个负电荷。
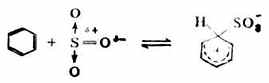
第二步和第三步转变为苯磺酸。
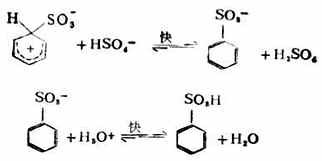
(四)傅-克反应
傅-克反应历程和硝化反应历程相似。
1.烷基化
亲电试剂是碳正离子R+,它是由以下过程生成的。
R-X+AlCl3→R++[AlCl3X]-
烷基化由以下两步进行:
第一步:
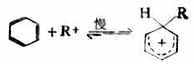
第二步:
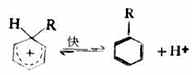
2.酰基化:
亲电试剂是正离子![]()
,它是由以下过程生成的。
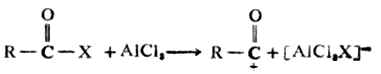
酰基化由以下两步进行:
第一步:
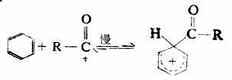
第二步:
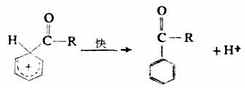
五、苯环上亲电取代的定位规律
实验证明当苯环上已经有一个取代基存在,再引入第二个取代基时,则第二个取代基进入的位置和难易程度主要决定于原有取代基的性质,而与进入的取代基关系较少。这应是苯环亲电取代的定位规律。因此,把苯环上已有的取代基叫做定位取代基。根据许多实验事实,可以把定位取代基分为两类。
(一)、邻、对位定取代基
当苯环上已带有这类定位取代基时,再引入的其它基团主要进入它的邻位或对位,而且第二个取代基的进入一般比没有这个取代基(即苯)时容易,或者说这取代基使苯环活化。下面是常见的邻、对位定位取代基。它们的定位取代效应按下列次序而渐减。
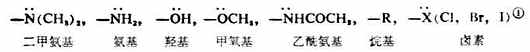
这类定位取代基的特征是,取代基中直接与苯环相连的原子大多数是未共用电子对或不含饱和键(但有例外,如-CH=CHCO2是邻、对位定位取代基)。
(二)间位定位取代基
当苯环上已存在这类定位取代基时,再引入的其它基团主要进入它的间位,而且第二个取代基的进入比苯要难,或者说这个取代基使苯环钝化。下面是常见的间位定位取代基,它们的定位效应按下列次序而渐减。
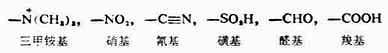
这类定位取代基的特征是,取代基中直接与苯环相连的原子一般都含有不饱和键或带有正电荷。
苯环的取代规律在实际应用上很有意义,因为掌握了这个规律,就可以预知取代反应中的主要产物。
取代定位规律并不是绝对的。实际上在生成邻位及对位产物的同时,也有少量间产物生成;在生成间位产物的同时,也有少量的邻位和对位产物生成。例如当甲苯在0℃下磺化时,除生成52.5%的对甲基磺酸和42.7%的邻甲基苯磺酸外,还生成3.8%的间甲基苯磺酸。
(三)二取代苯的取代定位规律
如果苯环上已经有了两个取代基,当引入第三个取代基时,影响第三个取代基进入的位置的因素较多。定性地说,两个取代基对反应活性的影响有加和性。人们从实际工作中得出了以下的经验规律:
1.苯环上已有两个邻对位定位取代基或两个间位定位取代基,当这两上定位取代基的定位方向有矛盾时,第三个取代基进入的位置,主要由定位作用较强的一个来决定。如果两上定位取代基的作用强度相近,将得到数量相近的异构体。例如,下列化合物进行亲电取代反应时,第三个取代基主要进入的位置用“→”表示。
2.苯环上已有一个邻对位定位取代基和一个间位定位取代基,且二者的定位方向相反,这时主要由邻对位定位取代基来决定第三个取代基进入的位置。例如:
3.两个定位取代基在苯环的1位和3位时,由于空间位阻的关系,第三个取代基在2位发生取代反应的比例较小。例如:
六、苯及其主要同系物
(一)苯
苯为无色液体,具有特殊气味,易燃烧。熔点5.5℃,沸点80℃。不溶于水,易溶于有机溶剂。苯有毒性,可致癌。
苯是重要的化工原料,也是优良的有机溶剂。
(二)甲苯
甲苯为无色液体,易燃烧,挥发性强。甲苯主要用以合成硝基甲苯、TNT、苯甲酸、苯甲醛等。甲苯也用作溶剂。
(三)二甲苯
二甲苯有三种异构体(邻、间、对位)。三种异构体的混合物为无色液体,易燃。不溶于水,易溶于有机溶剂。二甲苯在医学上制作组织切片标本时,用于脱醇、脱脂、二甲苯也是一种重要的有机合成原料。
第三节 多环芳香烃
多环芳香烃可按照分子中苯环互相连续的方式为联苯、联多苯、多苯化脂烃和稠环芳香烃等几类。其中以稠环芳香烃为最重要。
一、萘
萘是煤焦油中含量最多的成分,可达10%左右。
(一)萘的构造
萘的分子式为C10H8。通过X射线测定萘分子的结构,证明萘分子具有平面结构。两个苯环共享两个碳原子互相稠合在一起,碳碳键的键长既不同于典型的单键和双键,届不同于苯分子中的碳碳键。萘的构造式及各键的键长如下:
苯分子中C-1,4,5,8为α位;C-2,3,6,7为β位。
(二)萘的物理性质
萘为白色片状晶体,易升华,熔点80℃,沸点218℃。不溶于水,而能溶于乙醇,、乙醚和苯等有机溶剂中。
(三)萘的化学性质
1.取代反应
萘可发生与苯类似的亲电反应,一般在α-C上进行。例如,卤代和硝化反应。磺化则根据温度不同。例如:
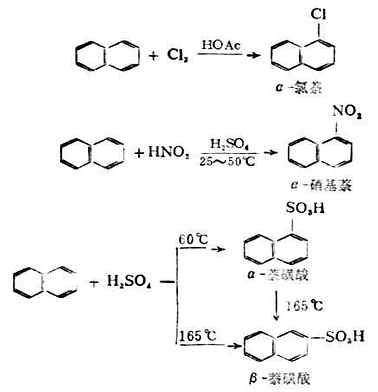
2.加成反应
萘比苯易加成,在不同条件下生成不同的加氢产物。
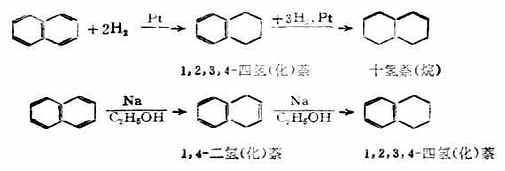
3.氧化
萘比苯易被氧化。用V2O5作催化剂时,萘的蒸气可被空气氧化,生成邻苯二甲酸酐。
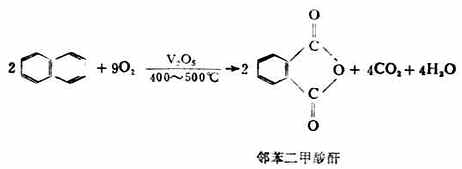
苯环上有取代基时,则根据取代基的不同,氧化时有一个环可能被破坏。若环上连接有间位定位取代基时,这个环比葳难氧化,而连有邻、对位定位取代基的环比苯易氧化。例如:
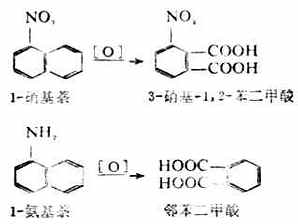
二、蒽和菲
蒽和菲都存在于煤焦油中。蒽为无色片状晶体,熔点216℃,沸点340℃;菲为具有光泽的无色晶体,熔点101℃,沸点340℃。
蒽和菲的分子式都是C14H10,二者互为同分异构体。它们在结构上都同萘相似。蒽和菲的构造式如下:
1,4,5,8位置相同,称为α位;2,3,6,7位置相同,称为β位;9和10位置相同,称为γ位。蒽和菲具有一定的不饱和性,在一定的条件下也可被氧化。
菲的构造式很重要。完全氢化的菲在C-7和C-8处与环戊烷稠合的化合物叫做环戊烷多氢菲,环戊烷多氢本身不存在于自然界中,但它的衍生物却广泛存在于动植物体内,且具有重要的生理作用。例如胆甾醇、维生素D、胆酸、性激素等。环戊烷多氢菲的构造式及各碳原子的位次编号如下:
三、致癌烃
致癌烃是能引起恶性肿瘤的一类多环稠苯芳香烃。这一灯化合物都含四个或更多的苯环。它们存在于煤焦油和沥青中。皮肤长期接触其蒸气,可能引起皮肤癌。因此,为了保证人民健康,我们必须防止多环稠苯芳香烃对环境的污染,常见的致癌烃有3,4-苯并芘,1,2,5,6-二苯并蒽和1,2,3,4-二苯并菲等。
第十三章 卤代烃
卤代烃是烃分子中的一个或几个氢原子被卤素原子取代后生成的化合物。含一个卤原子的卤代烃可用R-X表示,卤原子是卤代烃的官能团。常见的卤代烃是烃的氯、溴和碘的取代物。由于氟代烃的制法和性质都比较特殊,和其他三种卤代烃不同,不在本书中讨论。
一、卤代烃的分类和命名
(一)分类
在卤代烃中,按照卤素的不同,可分为氟代烃、氯代烃、溴代烃和碘代烃。又可根据分子中卤原子的数目不同分为一卤代烃和多卤代烃。此外,根据烃基的不同,还可以分为卤代烷烃、卤代烯烃和卤代芳烃。在卤代烷中又可根据卤原子所连接的碳原子不同,分为伯卤代烷、仲卤代烷和叔卤代烷。
(二)命名
卤代烃因种类不同,命名方法也不同。
简单的卤代烃,用普通命名法命名,以相应的烃称为卤某烃。
复杂的卤代烃,可用系统命名法命名,把卤代烃看作烃的衍生物,按照烃的命名法编号,然后把支链、卤素的位置按“次序规则“写在某烃的名称之 前。
卤代烷烃的命名法与烷烃相似。
卤代烯烃的命名,双键的位次仍用较小的编号标出。
卤代芳香烃的命名有两种情况:当卤原子在芳环上时,则以芳烃为母体,卤原子为取代基;卤原子在侧链上时,则以相应的链烃为母体。
有此卤代烃也采用俗名,如三氯甲烷(CHCL3),三碘甲烷(CHI3)叫碘仿。
二、卤代烃的性质
(一)物理性质
室温下除低级卤代烃如CH3CL,CH3Br,C2H5CL及CH2=CHCL为气体外,其余的是液体或固体。
它们的沸点也有规律性。烃基相同时,氯代物的沸点最低,密度最小;碘代物沸点最高,密度最大。卤素相同时,其沸点随烃基的增大而增高,密度则减小。
除某些氯代烷外,卤代烃一般都比小重,特别是多氯代物、溴代物和碘代物。
(二)化学性质
卤代烃的化学性质除主要与卤原子有关外,烃基部分也有影响,特别是直接与卤原子相连的碳原子是饱和的还是不饱和的,对卤原子的化学活泼性有很大的关系。

1.取代反应
在卤代烷和卤原子连在苯环侧链上的卤代烃中,与卤原子直接相连的碳原子是饱和的。由于卤原子的电负性比碳原子大,碳-卤键就成为极性共价键,碳原子一端带部分正电荷δ+,卤原子一端带部分负是荷δ-。

卤代烃分子中的上述情况,使试剂中带负电的原子团(如OH-,CN-)容易攻击带δ+碳原子而与之结合,带δ-的卤原子容易成为卤离子而离开。所以当卤代物与氢氧化钠或氰化钠作用时,羧基(-OH)或氰基(-CN)可取代卤原子而生成醇或腈类。这种反应称为取代反应。
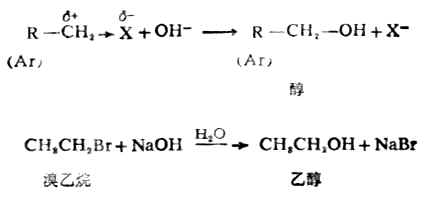
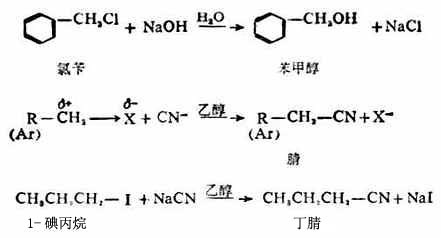
在上述反应中,都是由试剂的阴离子部分(如-OH或-CN)进攻卤代烃中电子云密度较小的显正性的碳原子而发生作用的。这些阴离子都具有亲核的性质。因此,把-OH、-CN等叫亲核试剂。由亲核试剂进攻而引起的取代反应称为亲核取代反应。
卤原子连在双键碳原子上的卤代烃,如氯乙烯、氯苯等,就不易起取代作用。这是由于卤原子中的未共用p电子对,可与π键形成p-π共轭体系,使电子云向碳原子方向移动,使碳-卤键的极性降低,即卤原子与碳原子结合得比较牢固,使卤原子的活泼性减小。所以氯乙烯和氯苯不易起取代作用。氯苯只在高温和高压下才能使氯原子被羧基取代生成苯酚。
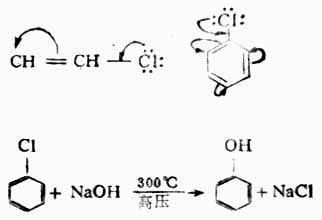
卤原子不直接连在双键碳原子上的卤代物,由于双键与卤原子距离较远,不发生p-共轭作用,因而它们的性质与卤代烷相似。如果卤素连接在双键的邻位碳上,则卤代物易起取代反应。如3-氯丙烯很很容易与OH-起亲核 作用生成烯丙醇。
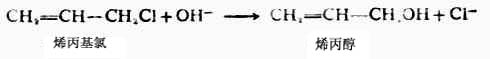
以上所述是烃基结构不同对取代活泼性的影响。当烃基相同而卤原子不同时,卤代烃的取代活泼性也不同,其顺序为碘代物>溴代物>氯代物。
2.消除反应
一卤代烷与浓氢氧化钾或氢氧化钠的乙醇溶液共热时,分子内脱去一分子卤代氢生成烯烃。这种反应叫做消除反应。
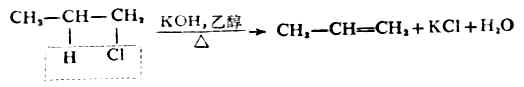
消除反应可从一个人女孩子中脱去简单分子(如H2O、HX、NH3等)生成不饱和化合物。
在卤代烷中,脱去卤化氢的反应以叔卤代烷最易进行,其次为仲卤代烷、伯卤代烷较难。仲或叔卤代灶发生消除反应时,可能得到不同的产物。
例如:
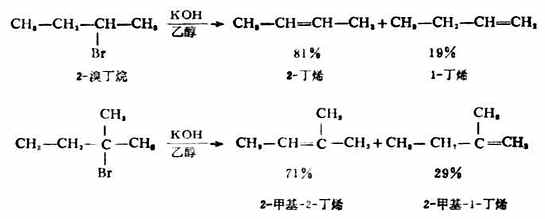
从上述实验结果可知,消除反应的主要产物是在双键碳上连有较多烷基的烯烃,也就是说,脱卤化氢如有两个不同的βH可以脱去,则消除的氢原子主要来自含氢原子较少的碳原子上。这个规律叫做札依采夫规律。
三、重要的卤化烃
(一)氯乙烷
氯乙烷是带有甜味的气体,沸点是12.2℃,低温时可液化为液体。工业上用作冷却剂,在有机合成上用以进行乙基化反应。施行小型外科手术时,用作局部麻醉剂,将氯乙烷喷洒在要施行手术的部位,因氯乙烷沸点低,很快蒸发,吸收热量,温度急剧下降,局部暂时失去知觉。
(二)三氯甲烷
三氯甲烷俗名氯仿,为无色具有甜味的液体,沸点61℃,不能燃烧,也不溶于水。工业上用作溶剂,在医药上也曾用作全身麻醉剂,因毒性较大,现已很少使用。
(三)二氟二氯甲烷
二氟二氯甲烷CH2CL2俗名氟利昂,为无色气体,加压可液化,沸点-29.8℃,不能燃烧,无腐蚀和刺激作用,高浓度时有乙醚气味,但遇火焰或高温金属表面时,放出有毒物质。氟利昂可用作冷冻剂。
(四)四氟乙烯
四氟乙烯CF2=CF2为无色气体,沸点-76℃,四氟乙烯聚合得到聚四氟乙烯:
![]()
聚四氟乙烯有耐热性,化学性能非常稳定,有“塑料王”之称。
第十四章 醇、酚、醚
醇、酚和醚都是烃含氧衍生物。
醇一般可看作是烃分子中的氢原子被羟基(-OH)取代的化合物。羟基是醇的官能团。但芳香烃苯环上的氢原子羟基取代的化合物不属于醇而属于酚。酚的官能团也是羟基。
R-h 烃R-OH 醇
Ar-H 芳香烃Ar-OH 酚
醇和酚分子中虽然都含有相同的官能团,但酚中的羟基仅限于直接连在芳香烃上,所以这种构造上的特点使酚的性质与醇不完全相同。一般把醇类的羟基称为醇式羟基,酚类的羟基称为酚式羟基。
醚是醇或酚的衍生物。它可看作是醇或酚羟基上的氢被烃基(-R‘、Ar’)取代的化合物。
R-OH 醇
Ar-OH 酚R-O-R‘醚
(Ar)(Ar`)
醇、酚和醚是重要的有机化合物。有的在医药上可用作消毒剂、麻醉剂、溶剂,有的是有机合成的常用原料。
第一节 醇
一、醇的分类
醇可根据烃基的不同、羟基所连碳原子的类型、羟基数目等三种方法进行分类。
1.

2.
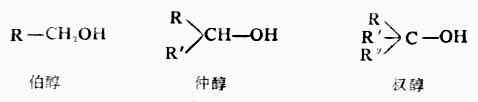
3.例如:
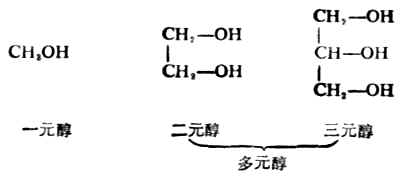
二、醇的命名
(一)普通命名法
简单的一元醇多用普通命名法命名。通常是在醇字前面加上烃基的名称,“基”字一般可以省略。例如:
(二)系统命名法
选择连有羟基碳原子在内的最长碳链为主链,从靠近羟基的一端开始编号,根据主链碳原子数称某醇。羟基位次用阿拉伯数字表明。支链或其它取代基按“次序规则”列出。
不饱和醇的命名,应选择连有羟基同时含有双键或三键碳原子在内的碳链作业主链,编号时应以羟基位次为最小。例如:
芳香醇也是按照上面的命名原则,把芳香烃当作取代基。例如:

多元醇的命名是选择包括连有尽可能我的羟基的碳链作主链,依次基数称某二醇、某三醇等。因为羟基是连在不同碳原子上的,所以当羟基数与主链碳原子数相同时可以不必标明羟基位次。例如:
三、醇的性质
(一)物理性质
低级饱和一元醇是易挥发的液体,较高级的醇为粘稠的液体,C11及C11以上的醇为蜡状固体。由于羟基的存在,醇分子间可以形成氢键,故醇随着羟基的增多,形成氢键数目增多,所以多元醇具有更高的沸点。
低级的醇如甲醇、乙醇、丙醇等均能以任何比例与水混溶,这是因为醇羟基也可与水形成氢键,结果使醇有可能在水分子间取得位置而溶入水中。当醇中的烃基链增长时,由醇的烃基部分引起的分子之间的吸引力(即范德华力)就会超过醇羟基和水间的氢键引起的吸引力。结果醇在水中的溶解度就很快随着降低。例如:在25℃的100g水中,正丁醇的溶解度为7.9g、正己醇为0.6g、正辛醇为0.5g,而癸醇则不溶于水,不溶于非极性溶剂。表14-1是饱和一元醇的物理常数。
表14-1 一些饱和一元醇的物理常数
| 名称 | 构造式 | 熔点/℃ | 沸点/℃ | 相对密度20℃ | 溶解度g·(100水)-1,,25℃ |
| 甲醇 | CH3OH | -97.8 | 64.5 | 0.792 | ∞ |
| 乙醇 | CH3CH2OH | -117.3 | 78.5 | 0.789 | ∞ |
| 正丙醇 | CH3CH2CH2OH | -127 | 97.8 | 0.804 | ∞ |
| 异丙醇 | (CH3)2CHOH | -86 | 82.5 | 0.789 | ∞ |
| 正丁醇 | CH3(CH2)2CH2OH | -89.8 | 117.7 | 0.810 | 7.9 |
| 异丁醇 | (CH3)2CHCH2OH | -108 | 108 | 0.802 | 10.0 |
| 正戊醇 | CH3(CH2)3CH2OH | -78.5 | 137.9 | 0.817 | 2.3 |
| 正己醇 | CH3(CH2)4CH2OH | -52 | 156.5 | 0.819 | 0.6 |
| 正辛醇 | CH3(CH2)6CH2OH | -15 | 195 | 0.827 | 0.05 |
| 正癸醇 | CH3(CH2)8CH2OH | 6 | 228 | 0.829 | |
| 正十二醇 | CH3(CH2)10CH2OH | 24 | 259 | 0.831 | |
| 苯甲醇 | C6H5CH2OH | -15 | 205 | 1.046 | |
| 2-苯基乙醇 | C6H5CH2CH2OH | -26 | 219 | 1.013 | 4 |
| 环己醇 |  |
25 | 161 | 0.962 | 5.7 |
(二)化学性质
醇的官能团是羟基,它由氢氧两原子组成。氧原子的电负性较大,吸电子的能力较强,所以醇分子中的C-O键和O-H键都有明显的极性。键的极性有利于异裂反应的发生,所以C-O键和O-H键都比较活泼,多数反应都发生在这两个部位。另外,由于诱导效应,与羟基邻近的碳原子上的氢也参与某些反应。
1.与碱金属的反应
醇与水相似,羟基里的氢可被活泼金属取代生成醇化物和氢氢气。例如:
2ROH+2Na→2RONa+H2↑
醇钠
2CH3-CH2OH+2Na→2CH2CH2ONa+H2↑
乙醇钠
醇与金属钠的反应不如水与金属反应时那样剧烈。这是由于烃基的斥电子作用,使羟基中氧原子上的电子云密度增加,减低了氧原子吸引氢氧间电子对的能力,降低了氢氧键的极性。
H-O:h
R→O:h
由于上述诱导效应的存在,使得醇羟基中的氢不如水中的氢那样活泼,不易成为离子,所以反应也较缓和。由此可见,烃基的斥电子能力愈强,醇羟基中氢原子的活泼性愈低,与金属钠的反应就愈缓慢。故伯、仲、叔醇中,伯醇与钠反应速率最快,叔醇最慢。
醇钠是白色固体,遇水即水解,生成醇和氢氧化钠,因此醇钠的水溶液具有强碱性。
RONa+H2O→ROH+NaOh
除金属钠外,醇也可与锂、钾等其它活泼金属起类似的反应,生成相应醇的金属化合物,统称醇化物。
2.氧化反应
醇分子中的α碳原子上若有氢原子时,该氢原子受羟基的影响,比较活泼易于被氧化。用高锰酸钾或重铬酸钾加硫酸等氢氧化剂氧化为相应的醛或酮。例如,伯醇氧化生成醛,醛继续氧化生成羧酸;仲醇氧化生成酮。叔醇在同样条件下不易被氧化。
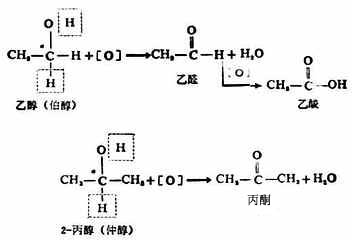
醇的氧化实质上是脱去两个氢原子,一个是羟基上的氢、一个是α碳(即与-OH相连的C)上的氢。因叔醇α碳上不连氢,所以在一般条件下不起氧化反应。但在反应条件剧烈时,则可发生分子断裂,产生含碳较少的产物。
用催化脱氢的方法也可将醇氧化。在Cu 、Ag等金属催化下,醇经高温可失去两个氢原子而生成相应的醛和酮,此法可用于工业生产。
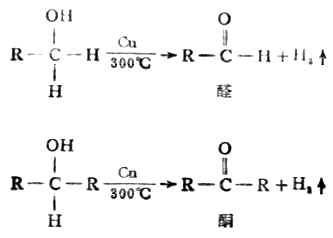
3.与氢卤酸的反应
醇与氢卤酸作用时,醇中的羟基可被卤素取代,生成卤代烃和水。
![]()
上述反应是可逆的,如其中一种反应物过量或移去产物水,可使平衡右移,提高卤代烃的收率。这个反应的速率与氢卤酸和醇的类型有关。当同一种醇与不同的氢卤酸作用时,反应速率是:HI>HBr>HCL。同一种氢卤酸与不同的醇作用时,反应速率是:叔醇>仲醇>伯醇。如用无水氯化锌作催化剂,浓盐酸可与叔醇立即反应,生成的卤代烃因不溶于反应试剂而呈混浊;如与仲醇反应,需几分钟才呈混浊;如与伯醇反应,则几小时也不见混浊。因此利用上述不同的反应速率,可作为区别伯、仲、叔醇的一种化学方法。这种由浓盐酸和无水氯化锌所配成的试剂又称为卢卡斯试剂。
4.脱水反应
醇与浓硫酸共热发生脱水反应,产物随反应条件及醇的类型而异在较高温度下,主要发生分子内的脱水(消除反应)生成烯烃;而在稍低温度下,则发生分子间脱水生成醚。
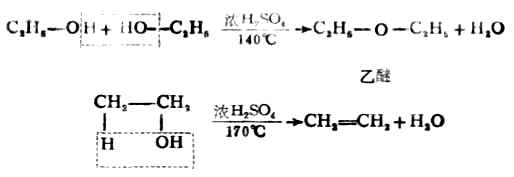
有些仲醇及叔醇的脱水可能生成两种烯烃。
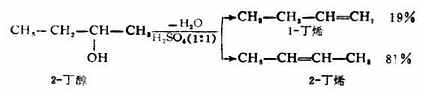
实验证明,醇脱水生成烯的反应主要产物是碳碳双键上连烃基最多的烯烃。即遵从扎依采夫规律。
5.与无机酸反应
醇可与无机含氧酸如硝酸、亚硝酸β硫酸和磷酸等作用,失去一分子水而生成无机酸酯。例如:
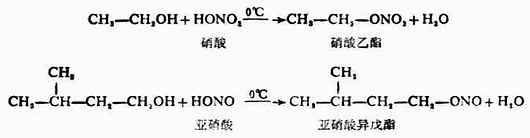
硫酸是二元酸,除可与一分子乙醇作用生成酸性酯外,尚可与两分子乙醇生成中性酯。
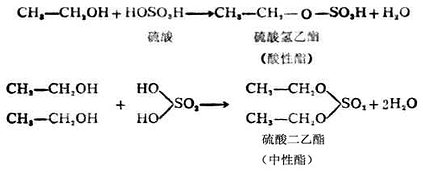
磷酸是一个三元酸,它可以形成三种类型的磷酸酯。即:
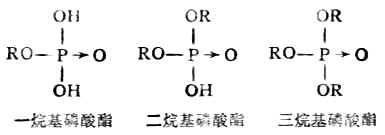
醇的无机酸具有多方面的作途。高级醇(含碳原子8-18个)的酸性硫酸酯的钠ROSO2Ona具有去垢作用,可用作洗涤剂;亚硝酸异戊酯是缓解心绞痛的药物;常用的杀虫药敌敌畏是具有磷酸酯结构的化合物。
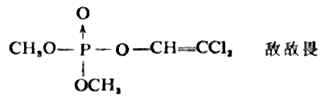
含有无机酸酯的物质也广泛存在于人体内。如存在于软骨中的硫酸软骨质就是具有硫酸酯结构;组成细胞的重要万分核酸及磷脂中都含有磷酸酯的结构;体内某些代谢过程也往往通过形成磷酸酯作为中间产物。
醇与羧酸作用生成羧酸酯的反应将在第十六章中讨论。
6.多元醇的特性
多元醇的化学性质与饱和一元醇类似,也能起酯化、氧化等反应。但由于多元醇所含的羟基比一元醇多,因此又存在着不同于一元醇的某些性质。例如多元醇除了能与碱金属反应外,还可与重多属的氢氧化物反应。如把丙三醇(甘油)加到氢氧化铜沉淀中去就可看到沉淀消失,产生一种深蓝色的甘油铜溶液,此反应可用来鉴定具有两个相邻羟基的多元醇。
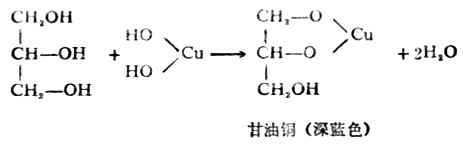
此外,对多元醇分子来讲,由于一种反应可在不同位置的羟基上进行,也可在几个羟基上同时进行,所以往往可得到多种没的产物。如丙三醇氧化就会生成各种氧化产物的混合物,例如:
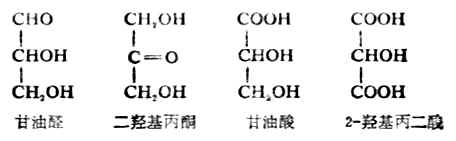
甘油的某些氧化产物的磷酸酯是人体内物质代谢的中间产物。
四、重要的醇
(一)甲醇
甲醇最初由木材干馏制得,故俗名木精。甲醇为无色透明液体,沸点64.5℃,能与水及多数有机溶剂混溶。甲醇有毒,误服少量(10ml)能使双目失明,30ml能中毒致死。甲醇可作溶剂,也是一种重要的化工原料。
(二)乙醇
乙醇是酒的主要成分,故俗名酒精。乙醇为墙角色液体,沸点78.5℃,用途广泛,是一种重要的有机合成原料和溶剂。我国药典规定乙醇浓度在20℃时不得小于94.58%(ml/ml),临床使用的是70%-75%乙醇水溶液作外用消毒剂,因它能使细菌蛋白质脱水变性。长期卧床病人用50%乙醇溶液涂擦皮肤,有收敛作用,并能促进血液循环,可预防褥疮。在医药上常用乙醇配制酊剂,如碘酊,俗称碘酒,就是碘和碘化钾的乙醇溶液。
(三)丙三醇
丙三醇俗名甘油,为无色、吸湿性强、有甜味的粘稠液体,沸点290℃,能与水或乙醇混溶。甘油有润肤作用,但它的吸湿性很强,会对皮肤产生刺激,所以在使用时须先用适量水稀释。在医药上甘油可用作溶剂,如酚甘油、碘甘油等。对便秘患者,常用甘油栓剂或50%甘油溶液灌肠,它既有润滑作用,又能产生高渗压,可引起排便反射。甘油三硝酸酯(俗称硝酸甘油)是缓解心绞痛药物。它受到震动或撞击能猛烈分解引起爆炸,故可用作炸药。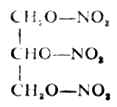
(四)山梨醇和甘露醇
山梨醇和甘露醇都是六元醇,二者是异构体,其构型式为:
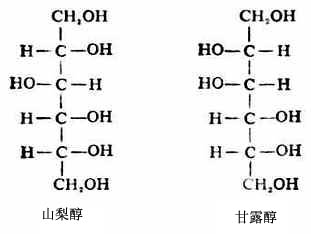
它们都是白色结晶粉末,味甜,广泛存在于植物中,如许多水果及蔬菜中均含有。
山梨醇和甘露醇均易溶于水。它们的20%或25%的溶液,在临床上用作渗透性利尿药,能将周围组织及脑组织的水分吸入血中随尿排出,从而降低颅内压,消除水肿,对治疗脑水肿与循环衰竭有效。
(五)苯甲醇
苯甲醇又名芐醇,常以酯的形式存在于植物香精油中。它是无色液体,有芳香味,沸点205℃,微溶于水,可与乙醇、乙醚混溶。
苯甲醇具有微弱的麻醉作用和防腐作用,也可作为局部止痒剂。
(六)龙脑
龙脑又名冰片或2-莰烷醇。它是透明或半透明片状结晶,熔点204℃,通过蒸馏艾纳香的新鲜叶子而得,药用的冰片是用化学方法合成的。有特异香气。它具有止痛消肿的作用。是人丹、冰硼散等中成药的成分之一。
第二节 酚
一、酚的分类和命名
酚的官能团是酚式羟基。
酚可以根据分子中所含羟基数目的不同分为一元酚、二元酚、三元酚等,二元酚以上的酚叫多元酚。
酚的命名是在酚字前加上芳环名称,以此作母体标以取代基的位次、数目和名称。例如:
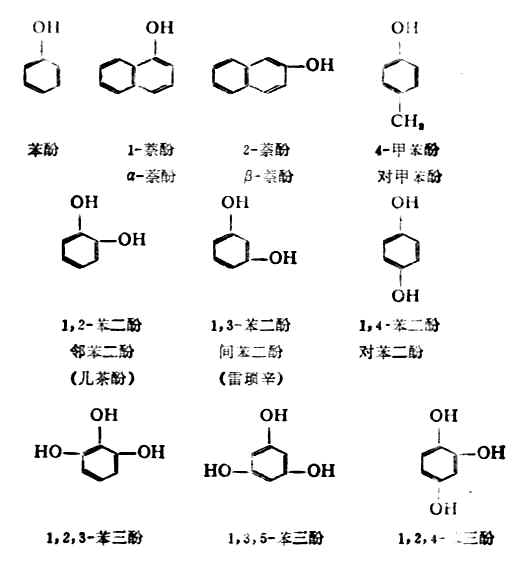
二、酚的化学性质
酚的羟基直接与苯环的sp2杂化的碳原子相连,这与脂肪族化合物中的烯醇很相似。另外,由于 酚的羟基氧原子的未共享电子对与苯环的共轭作用,不但使苯酚成稳定化合物,而且也有利苯酚的离解。
(一)弱酸性
酚比醇的酸性强,是由于酚式羟基的O-H键易断裂,生成的苯氧基负离子比较稳定,使苯酚的离解平衡趋向右侧,而表现弱酸性。酚式羟基的氢除能被金属取代外,还能与强碱溶液生成盐(如酚钠)和水。
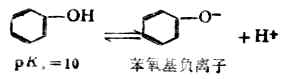
2C6H5OH+Na→2C6H5ONa+H2↑
C6H5OH+NaOH→C6H5ONa+H2O
若在苯酚钠的水溶液中通入二氧化碳,即有游离苯酚析出。这是因为苯酚酸性比碳酸弱,所以酚盐能被碳酸所分解。
C6H5OHa+CO2+H2O→C6H5OH+NaHCO3
由于酚的酸性弱于碳酸,所以酚只能溶于氢氧化钠而不溶于碳酸氢钠。实验室里常根据酚的这一特性,而与既溶于氢氧化钠又能溶于碳酸氢钠的羧酸相区别。此方法也可用于中草药中酚类成分与羧酸类成分的分离。
(二)与氯化铁的反应
大多数的酚能与氯化铁的稀水溶液发生显色反应。不同的酚与氯化铁反应呈显不同的颜色。例如,苯酚、间苯二酚、1,3,5-苯三酚与氯化铁溶液作用,均显紫色;甲苯酚呈蓝色;邻苯二酚、对苯二酚呈绿色;1,2,3-苯三酚呈红色,α-萘酚为紫色沉淀,β-萘酚则为绿色沉淀等。此显色反应常用以鉴别酚类的存在。
具有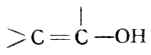
构造的烯醇型化合物也能与氯化铁溶液发生颜色反应。
一般的醇式羟基无此反应,故也可用来区别醇与烯醇。
(三)苯环上氢原子的取代反应
苯环连有羟基后,环的活泼性就增加,易起取代反应,取代基一般都进入羟基的邻对位及对位。例如苯的卤化反应一般较难进行,需要加热及催化剂,但苯酚的卤化就容易得多。在室温下加溴水于苯酚中,立即生成2,4,6-三溴苯酚的白色沉淀,此反应较灵敏,少量的苯酚也能检出。
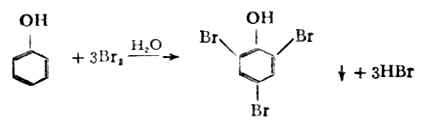
苯酚也易硝化,使用稀硝酸即可生成邻硝基苯酚和对硝基苯酚的混合物。如使用浓硝酸和浓硫酸的混合物作硝化剂则可生成二硝基苯酚或三硝基苯酚。2,4,6-三硝基苯酚俗称苦味酸,酸性比苯酚强得多。
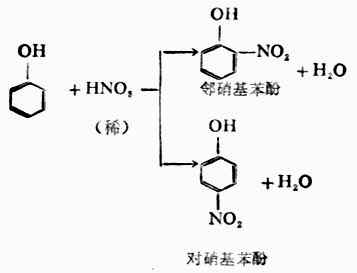
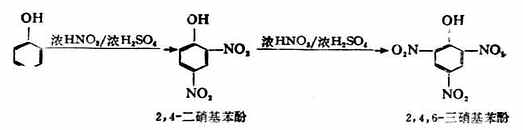
浓硫酸容易使酚磺化。室温下,产物为邻羟基苯磺酸,在100℃时主产物是对羟基苯磺酸。
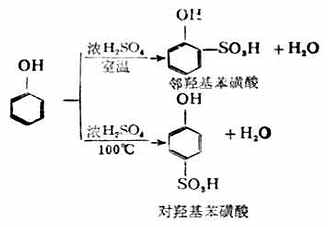
(四)氧化反应
酚类易被氧化,但产物复杂。纯苯酚系无色结晶,在空气中放置后,就能逐渐氧化变为粉红色、红色或暗红色。苯酚如用酸性重铬酸钾强烈氧化,则生成对苯醌。
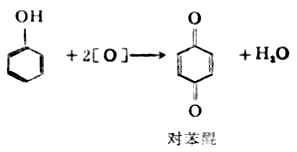
邻苯二酚和对苯二酚比苯酚更容易被氧化成相应的醌,但间苯二酚不能被氧化为相应的醌。醌是一般都具有颜色。
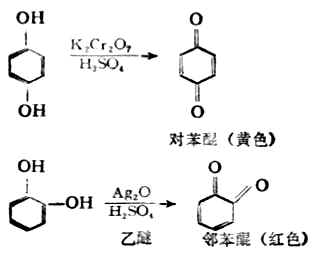
三、重要的酚
(一)苯酚
苯酚最初从煤焦油中得到,也称石炭酸。它是无色结晶,有特殊气味。熔点43℃,沸点182℃,能溶于水,25℃时100g水中可溶解发6.7g,68℃以上可完全溶解。此外,还易溶于乙醇、乙醚、苯等有机溶剂。苯酚能凝固蛋白质,有杀菌能力,医药上用作消毒剂。它的3%-5%溶液用于消毒手术器具,1%溶液外用于皮肤止痒,但苯酚浓溶液对皮肤具有腐蚀性。苯酚易被氧化,故应避光存于棕色瓶内。苯酚又是制造塑料、染料及药物的重要原料。
(二)甲苯酚
甲苯酚可由煤焦油得到,有邻、间、对三种异构体。它们都有苯酚气味,杀菌力比苯酚强。医药上常用的消毒剂煤酚皂液就是含47%-53%的三种甲苯酚混合物的肥皂水溶液,又称来苏尔。它的稀溶液常用于消毒。
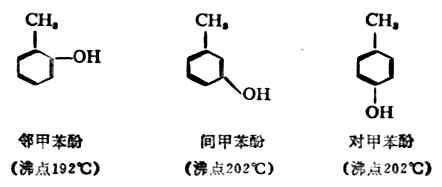
由于三者的沸点相近,不易分离,实际上常使用它们的混合物。
(三)苯二酚
苯二酚有三种异构体:
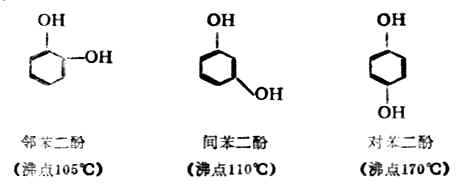
它们都是无色结晶。邻苯二酚和间苯二酚易用溶于水,对苯二酚在水中的溶解度小。
间苯二酚是具有抗细菌和真菌的作用,强度仅为苯酚的1/3。刺激性小,可用于治疗皮肤病如湿疹和癣症等。
对苯二酚常用作显影剂。
(四)萘酚
萘酚有α-和β-两种异构体。

α-萘酚为黄色结晶,熔点96℃,能与FeCL3作用生成紫色沉淀。β-萘酚为无色结晶,熔点122℃和FeCL3作用生成绿色沉淀。这两种化合物都是合成染料的原料。β-萘酚还具有抗细菌、霉菌和寄生虫的作用。
第三节 醚
一、醚的分类和命名
醚的官能团是醚键(C-O-C),醚键的氧连接两个烃基。如果两个烃基相同时称为单醚,通式为R-O-R。两个烃基不同时称为混醚,通式为R-O-R‘。烃基可以是脂肪烃基、脂环烃基或芳香烃基。
简单的醚。采用与氧原子相连的两上烃基的名称来命名。单醚就先写出烃基的名称,省略“二”字,然后加上“醚”字即可。混合醚的名称中,较小的烃基名称放在前面;如果有一个烃基是链状的,另一个是芳香烃基时,则把芳香烃基名称放在前面。例如:
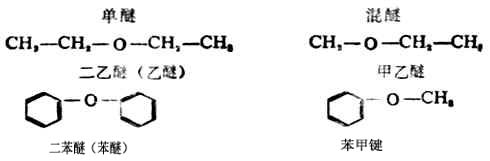
构造比较复杂的醚可用系统命名法命名。链状醚是选择包括连有氧原子的碳在内的最长碳链为主链,当作母体,把烃氧基(RO-或ArO-)作为取代基。
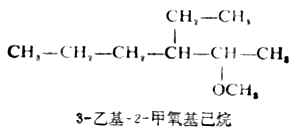
二、醚的性质
多数醚是易挥发、易燃的液体。由于醚分子间不能形成氢键,所以醚的沸点比同相对分子质量的醇的沸点低得多,如甲醚的沸点为-24.9℃,而乙醇的沸点则为78.5℃。一般醚都很难溶于水。
醚的化学性质与醇或酚有很大的不同。醚是比较稳定的化合物。醚与金属钠无反应,对碱及还原剂相当稳定。因此,常用一些醚作为有机反应中的溶剂。
(一)金羊盐的生成
醚键上的氧原子具有未共享电子对,作为刘易斯碱能接受强酸的H+,形成金羊盐。因此,醚能溶于强酸如浓HCL、浓H2SO4中。
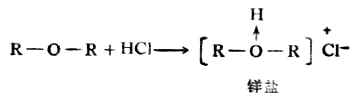
(二)烷基醚的氧化
含有α-氢的烷基醚由于受烃氧基的影响,在空气中放置时会被氧气氧化,生成过氧化物。过氧化物性质不稳定,温度较高时能迅速分解而发生爆炸。因此,在使用醚类时,应尽量避免将它们暴露在空气中。贮存时,宜放入棕色瓶中,并可加入少量阻氧化剂(如对苯二酚)以防止过氧化物的生成。用蒸馏法纯制醚类时,应检验有无过氧化物存在。其方法是,用FeSO4与KCNS的混合溶液与醚一起振摇。如醚中有过氧化物存在,则将Fe2+氧化为Fe3+而生成红色的[Fe(CNS)3-6。也可用酸性碘化钾溶液检验,若有过氧化物存在,则会游离出碘。
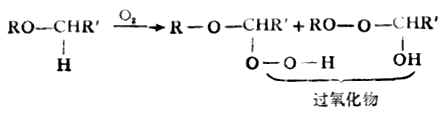
三、乙醚在医学上的应用
乙醚为无色液体,沸点34.5℃,极易挥发、燃烧,故使用时要特别小心,防止接近明火。
乙醚是一种应用很广泛的有机溶剂
■[此处缺少一些内容]■
第四节 硫醇和硫醚
■[此处缺少一些内容]■
第十五章 醛、酮、醌
醛、酮和醌的分子构造中都含有相同的官能团—羰基![]() ,因而统称为羰基化合物。它们在性质上有很多相似的地方。许多醛和酮是重要的工业原料,有些是香料或重要药物。
,因而统称为羰基化合物。它们在性质上有很多相似的地方。许多醛和酮是重要的工业原料,有些是香料或重要药物。
第一节 醛和酮
一、醛和酮的构造
羰基与一个氢原子和一个烃基相连的化合物叫做醛(甲醛例外,它的,羰基与两个氢原子相连),可用通式表示![]()
。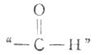 ”称为醛基,是醛的官能团,可简写为-CHO,它位于碳链的一端。
”称为醛基,是醛的官能团,可简写为-CHO,它位于碳链的一端。
羰基与两个烃基相连的化合物叫做酮,可用通式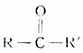 表示。酮的官能团
表示。酮的官能团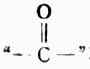
称为酮基,位于碳链中间。在一元酮中,两个烃基相同的叫单酮,两个烃基不同的叫做混酮。
羰基中的碳原子为sp2杂化,其中一个sp2杂化轨道与氧原子的一个p轨道按轴向重叠形成σ键;碳原子未参与杂化的p轨道与氧原子的另一个p轨道平行重叠形成π键。因此,羰基碳氧双键是由一个σ键和一个π键组成的。
由于氧原子的电负性比碳原子大,因此羰基中π电了云偏向于氧原子一边,使羰基碳原子带有部分正电荷,而氧原子则带有部分负电荷。羰基的极化情况可表示如下:
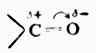
二、醛和酮的命名
(一)普通命名法
简单的脂肪醛按分子中的碳原子的数目,称为某醛。例如:
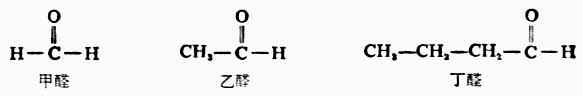
简单的酮可按羰基所连接的两上烃基命名。例如:
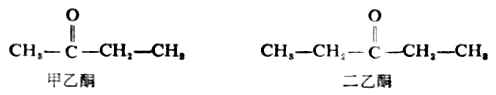
(二)系统命名法
对构造比较复杂的醛、酮则用系统命名法命名。命名时先选择包括羰基碳原子在内的最长碳链作主链,称为某醛或某酮。从醛基一端或从靠近酮基一端开始把主链中碳原子编号。由于醛基一定在碳链的链端,故不必用数字标明其位置,但酮基的位置必须标明,写在酮名的前面。主链上如有支链或取代基,应标明位次,把它的位次(按次序规则)、数目、名称写在某醛、某酮的前面。主链中碳原子的编号也可以用希腊字母表示,即把与羰基碳直接相连的碳原子用α表示,其它碳原子依次为β,γ…
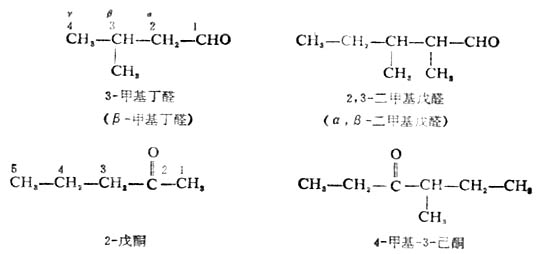
命名不饱和醛、酮则需标出不饱和键和羰基的位置。
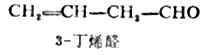
多元醛、酮命名时,同样选择包括羰基碳原子在内的最长碳链作为主链,编号时使羰基位置数字最小,同时加上用汉字数字表示的羰基数目。
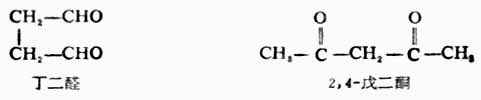
芳香醛、酮的命名,是以脂肪醛、酮为母体,芳香烃基作为取代基。
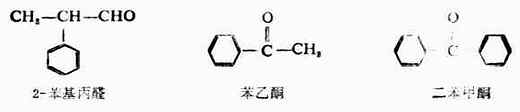
三、醛、酮的物理性质
在常温下,除甲醛是气体外,12个碳原子以下的脂肪醛、酮都是液体,高级脂肪醛、酮和芳香酮多为固体。
由于醛或酮分子之间不能形成氢键,没有缔合现象,故它们的沸点比相对分子质量相近的醇低。但由于羰基的极性,增加了分子间的引力,因此沸点较相应的烷烃高。如表15-1所示。
表15-1 相对分子质量相近的烷、醇、醛、酮的沸点
| 名称 | 正戊烷 | 正丁醇 | 丁醛 | 丁酮 |
| 相对分子质量 | 72 | 74 | 72 | 72 |
| 沸点/℃ | 36.1 | 117.7 | 74.7 | 79.6 |
醛、酮羰基上的氧可以与水分子中的氢形成氢键,因而低级醛、酮(如甲醛、乙醛、丙酮等)易溶于水,但随着分子中碳原子数目的增加,它们的溶解度则迅速减小。醛和酮易溶于有机溶剂。一些醛、酮的物理常数见表15-2。
表15-2一些醛、酮的物理常数
| 名称 | 构造式 | 熔点/℃ | 沸点/℃ | 相对密度 | 溶解度g·(100H2O)-1 |
| 甲醛 | HCHO | -92 | -19.5 | 0.815 | 55 |
| 乙醛 | CH3CHO | -123 | 20.8 | 0.781 | 溶 |
| 丙醛 | CH3CH2CHO | -81 | 48.8 | 0.807 | 20 |
| 丁醛 | CH3CH2CH2CHO | -97 | 74.7 | 0.817 | 4 |
| 乙二醛 | 15 | 50.4 | 1.14 | 溶 | |
| 丙烯醛 | CH2=CHCHO | -87.7 | 53 | 0.841 | 溶 |
| 苯甲醛 | -26 | 179 | 1.046 | 0.33 | |
| 丙酮 | CH3COCH3 | -95 | 56 | 0.792 | 溶 |
| 丁酮 | CH3COCH2CH3 | -86 | 79.6 | 0.805 | 35.3 |
| 2-戊酮 | CH3COCH2CH2CH3 | -77.8 | 102 | 0.812 | 几乎不溶 |
| 3-戊酮 | CH3CH2COCH2CH3 | -42 | 102 | 0.814 | 4.7 |
| 环己酮 | -16.4 | 156 | 0.942 | 微溶 | |
| 4-甲基-3-戊烯-2-酮 | (CH3)2C=CHCOCH3 | -59 | 130 | 0.865 | 溶 |
| 丁二酮 | 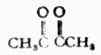 |
-2.4 | 88 | 0.980 | 25 |
| 2,4-戊二酮 | 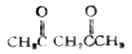 |
-23 | 138 | 0.792 | 溶 |
| 苯乙酮 | 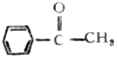 |
19.7 | 202 | 1.026 | 微溶 |
| 二苯甲酮 | 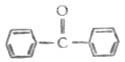 |
48 | 306 | 1.098 | 不溶 |
四、醛、酮的化学性质
醛、酮的化学性质主要决定于羰基。由于构造上的共同特点,使这两类化合物具有许多相似的化学性质。但是醛与酮的构造并不完全相同,使它们在反应性能上也表现出一些差异。一般说来,醛比酮活泼,有些反应醛可以发生,而酮则不能。
(一)羰基的加成
同碳碳双键一样,羰基中的碳氧双键也是由一个σ键和一个π键所组成,所以醛、酮都易发生加成反应。但和烯烃的亲电加成不同,羰基的加成属于亲核加成。由于氧原子的电负性大于碳原子,使羰基发生极化,氧原子带有部分负电荷,碳原了带有部分正电荷。一般说来,带负电荷的氧比带正电荷的碳较为稳定。所以,当羰基化合物发生加成反应时,首先是试剂中带负电荷的部分加到羰基的碳原子上,形成氧带负电荷的中间体,然后试剂中带正荷部分加到带负虵荷的氧上。这种由亲核试剂(能提供电子对的试剂)进攻而引起蝗加成反应叫做亲核加成反应。这类加反应可用于下式表示:
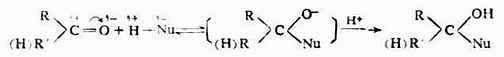
醛和酮可以与氢氰酸、亚梳酸氢钠、醇、氨的衍生物(如羟胺、肼等)试剂起加成反应。在反应产物中都是试剂中的氢与羰基上的氧相连接,其余部分与羰基的碳相连。
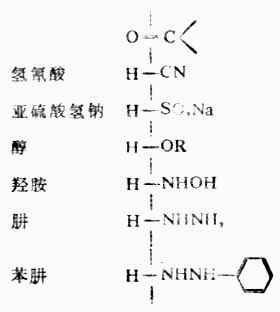
1.加氢氰酸
醛及脂肪族甲基酮与氢氰酸作用,生成α-α羰基腈。
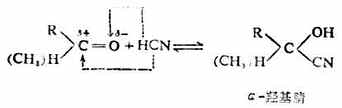
从上面的反应式或以看出,生成物比反应物增加了一个碳原子,因此这个反应可用来增长化合物的碳链。羟基腈在酸性水溶液中水解,即可得到羟基酸。
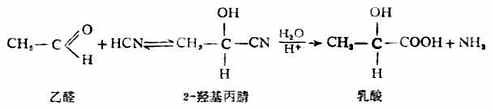
如果在醛、酮与氢氰酸反应中加入少量碱时,则反应速率明显加快;但如果加入酸,则抑制反应的进行。其原因是氢氰酸是一个弱酸,其离解过程为:
![]()
在上述平衡体系中加入酸, 能HCN的离解,加入碱则促进HCN的离解,使CN-浓度增大。碱能加速羰基与氢氰酸的加成反应表明,氢氰 酸不是以分子,而是以CN-及H+参加反应的。又因碱的加入,能增加CN-的浓度,所以首先向羰基进攻的是CN-。这是亲核加成反应历程的实验基础。
对于同一种亲核试剂,亲核加成的难易取决于羰基碳原子所带正电荷的强弱及位阻效应的大小。所谓位阻效应是指分子中相邻的原子或原子团,在空间所占的体积和位置而产生的影响。羰基碳原子所带正电荷越多,反应越容易进行;羰基上连接的烃基越大则位阻效应越大,亲核试剂就越不容易靠近,反应也就越不容易进行。酮的羰基和两个烃基相连,由于烷基的斥电子作用,降低了羰基碳原子的正电荷;另一方面酮的两上烃基增大了位阻效应,所以在许多亲核加成反应中,酮一般不如醛活泼。醛、酮亲核加成反应活泼性顺序排列如下:
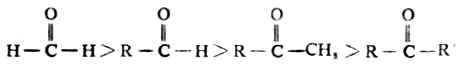
2.加亚硫酸氢钠
醛、脂肪族甲基酮和低级环酮(成环的碳原子在8个以下)都能与过量的饱和亚硫酸氢钠溶液发生加成反应,生成稳定的亚硫酸氢盐中成物。
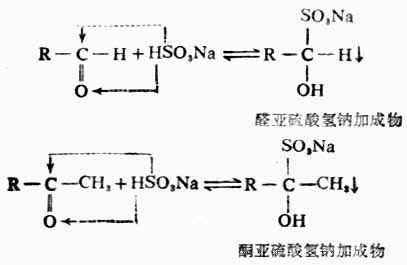
上述反应是可逆的。为使反应完全,常加入过量的饱和亚硫酸氢钠溶液,促使反应向右移动。由于这些加成物能被稀酸或稀碱分解成原来的醛或甲基酮,故常用这个反应来分离、精制醛或甲基酮。
其它脂肪酮或芳香酮(包括芳香族甲基酮)由于受位阻效应的影响难以进行这种加成反应。
3.加醇
醛与醇在干燥氯化氢的催化下,发生加成反应,生成半缩醛。
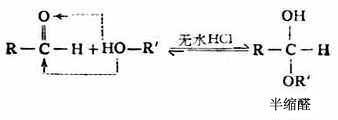
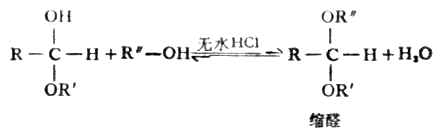
开链半缩醛是一类不稳定的化合物,能继续与另一分子醇作用,失去一分子水生成缩醛。缩醛是具有水果香味的液体,性质与醚相近。缩醛对氧化剂和还原剂都很稳定,在碱性溶液中也相当稳定,但在酸性溶液中则可以水解生成原来的醛和醇。在有机合成中,常先将含有醛基的化合物转变成缩醛,然后再进行别的化学反应,最后使缩醛变为原来的醛,这样可以避免活泼的醛基在反应中被破坏,即利用缩醛的生成来保护醛基。
酮在同样情况下不易生成缩酮。但是环状的缩酮比较容易形成。例如:
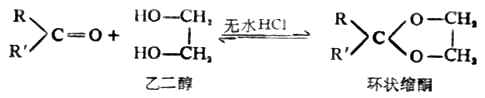
若在同一分子中既含有羰基又含有羟基,则有可能在分子内生成环状半缩醛(酮)。半缩醛(酮)、缩醛(酮)比较重要,因为它是学习糖类化学的基础,以后还要讨论。
4.与氨的衍生物的反应
醛、酮与氨的衍生物如羟胺、肼、2,4-二硝基苯肼等试剂作用,则生成相应的含碳氨双键的化合物,其名称及构造分别为:
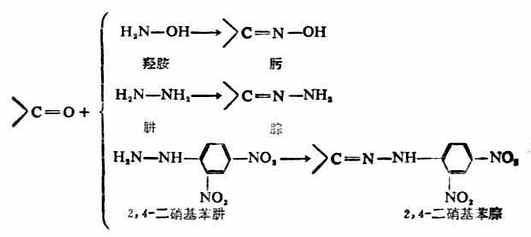
这此反应首先是N-H键断裂和与羰基加成,然后再脱去一分子水生成肟或腙。例如:
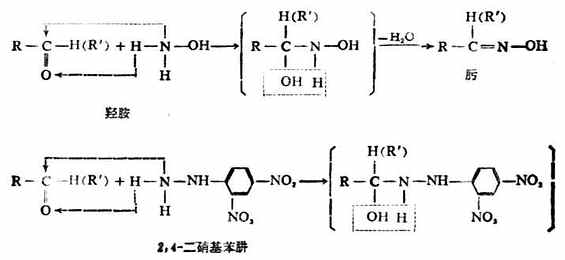
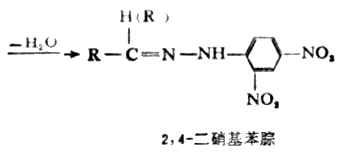
醛、酮与2,4-二硝基苯肼作用生成的2,4-二硝基苯腙是黄色结晶,具有一定的熔点,反应也很明显,便于观察,所以常被用来鉴别醛、酮。其它反应的产物肟、腙大都也是具有一定熔点的晶体,亦可用来鉴别醛、酮。因此,把这些氨的衍生物称为羰基试剂(即检验羰基的试剂)。
肟、腙等在稀酸作用下,可水解为原来的醛、酮,故可利用这些反应来分离和精制醛、酮。
(二)α碳原子上氢的反应
醛、酮分子中的α碳原子上的氢比较活泼,容易发生反应,故称为α活泼氢原子。若α碳原子上连接三个氢原子,则称其为活泼甲基。
醛、酮α碳原子上的氢因受羰基的影响具有活泼性,这是由于羰基的极化使α碳原子上C-H键的极性增强,氢原子有成为质子离去的趋向,很容易发生反应。
醛或酮的α氢原子易被卤素取代,生成α-卤代醛或酮。例如:
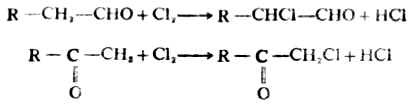
卤化反应继续进行时,也可生成α,α-二卤代物和α,α,α-三卤代物。
卤代醛或卤代酮都具有特殊的刺激性气味。三氯乙醛的水合物CCL3CH(OH)2,又称水合氯醛,具有催眠作用;溴丙酮具有催泪作用;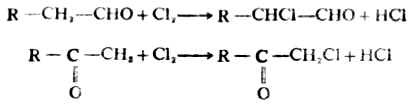
-溴苯乙酮的催泪作用更强,可用作泪瓦斯。
含有活泼甲基的醛或酮与卤素的碱溶液作用,三个α氢原子都被卤素取代,但生成的α,α,α三卤代物在碱性溶液中不稳定,立即分解成三卤甲烷(卤仿)和羧酸盐。
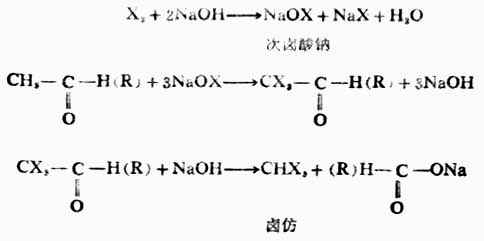
因为这个反应生成卤仿,所以称为卤仿反应。如用碘的碱溶液,则生成碘仿(称为碘仿反应)。碘仿为黄色晶体,难溶于水,并具有特殊的气味,容易识别,可用来鉴别是否含有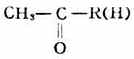
构造的羰基化合物。
次卤酸盐是一种氧化剂,可以使醇类氧成相应的醛、酮。因此,凡具有
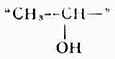
构造的醇会先被氧化成乙醛或甲基酮,再进行卤仿反应。所以碘仿
反应也能鉴别具有上述构造的醇类。如乙醇、异丙醇等。
2.羟醛缩合
含有氢原子的醛在稀碱的作用下,一分子醛的α氢原子加到另一分子醛的羰基氧原子上,其余部分加到羰基的碳原子上,生成既含有羟基又含有醛基的β-羟基醛(醇醛),这个反应称为羟醛缩合或醇醛缩合。例如:
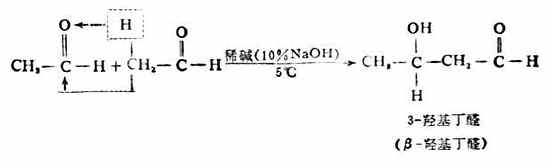
在碱或酸性溶液中加热时,β-羟 基醛易脱水生成α,β-不饱和醛。例如:
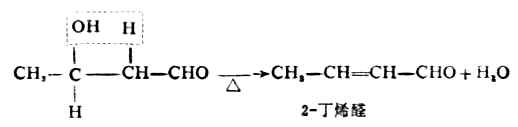
含有α氢原子的酮也可以发生类似的反应,生成β-羟 基酮,脱水后生成α,β-不饱和酮。
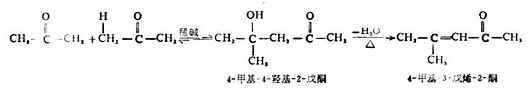
(三)还原反应
醛或酮经催化氢化可分别被还原为伯醇或仲醇。
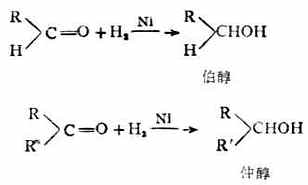
醛、酮与氢化铝锂(LiALH4)、硼氢化钠(NaBH4)或异丙醇铝(AL[OCH(CH3)2]3)作用,也都还原生成相应的醇。这些还原剂具有较高的选择性,只能还原羰基,而不影响分子中的碳碳双键等其它可被催化氢化的基团。例如,巴豆醛若用镍催化氢化则得到正丁醇,而用LiALH4还原可以得到巴豆醇。 >
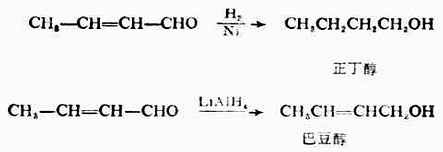
(四)醛的特殊反应
醛的羰基碳原子上连有氢原子,因此容易被氧化,不仅强氧化剂,即使氧化剂也可以使它氧化。醛氧化时生成同碳数的羧酸。酮则不易被氧化。
一些弱氧化剂只能使醛氧化而不能使酮氧化,说明醛具有还原性而酮一般没有还原性。因此,可以利用弱氧化剂来区别醛和酮。常用的弱氧化剂有土伦试剂、费林试剂和本尼迪特。
1.与土伦试剂反应
土伦试剂是由硝酸银碱溶液与氨水制得的银氨配合物的无色溶液。它与醛共热时,醛被氧化成羧酸,试剂中的一价银离子被还原成金属银析出。由于析出的银附着在容器壁上形成银镜,因此这个反应叫做银镜反应。
氧化剂也可以使它氧化。醛氧化时生成同碳数的羧酸。酮则不易被氧化。
一些弱氧化剂只能使醛氧化而不能使酮氧化,说明醛具有还原性而酮一般没有还原性。因此,可以利用弱氧化剂来区别醛和酮。常用的弱氧化剂有土伦试剂、费林试剂和本尼迪特。
1.与土伦试剂反应
土伦试剂是由硝酸银碱溶液与氨水制得的银氨配合物的无色溶液。它与醛共热时,醛被氧化成羧酸,试剂中的一价银离子被还原成金属银析出。由于析出的银附着在容器壁上形成银镜,因此这个反应叫做银镜反应。
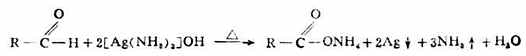
此反应可简单表示如下:
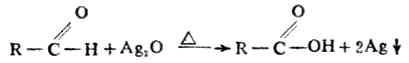
2.与费林试剂反应
费林试剂包括甲、乙两种溶液,甲液是硫酸铜溶液,乙液是酒石钾钠和氢氧化钠溶液。使用时,取等体积的甲、乙两液混合,开始有氢氧化铜沉淀产生,摇匀后氢氢化铜即与酒石酸钾钠形成深蓝色的可溶性配合物。
费林试剂能氧化脂肪醛,但不能氧化芳香醛,可用来区别脂肪醛和芳香醛。费林试剂与脂肪醛共热时,醛被氧化成羧酸,而二价铜离子则被还原为砖红色的氧化亚铜沉淀。
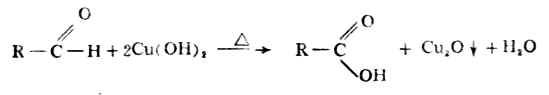
本尼迪特试剂也能把醛氧化成羧酸。它是由硫酸铜、碳酸钠和柠檬酸钠组成的溶液。它与醛的作用原理和费林试剂相似。临床上常用它来检查尿液中的葡萄糖。
(五)聚合反应
甲醛、乙醛等低级醛可以发生聚合反应,生成链状或环状化合物。例如:
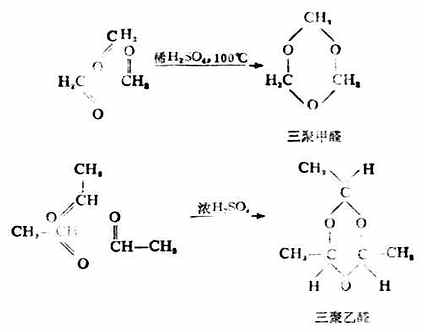
甲醛溶液长期放置后,生成多聚甲醛的白色固体。一般认为甲醛在水溶液中是以水合物形式存在的,这些水合物失去缩合即生成链状的多聚甲醛。
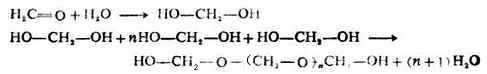
n一般最多可达100。多聚甲醛对热不稳定,在100℃时迅速地分解成甲醛。
高级的醛酮较难聚合。
五、个别醛和酮
(一)甲醛
甲醛又叫蚁醛,是具有强烈刺激臭味的无色气体,沸点-21℃。易溶于水,其40%的水溶液叫“福尔马林“,用作消毒剂和防腐剂。甲醛溶液能够消毒防腐的原因是因为甲醛具有使蛋白质凝固的性能。
(二)丙酮
丙酮是最简单的酮类化合物,它是无色液体,沸点56.5℃.丙酮极易溶于水,几乎能与一切有机溶剂混溶,也能溶解油脂、蜡、树脂和塑料等,故广泛用作溶剂。
患糖尿病的人,由于新陈代谢紊乱的缘故,体内常有过量丙酮产生,从尿中排出。尿中是否含有丙酮可用碘仿反应检验。在临床上,用亚硝酰铁氰化钠[Na2Fe(CN)5NO]溶液的呈色反应来检查:在尿液中滴加亚硝酰铁氰化钠和氨水溶液,如果有丙酮存在,溶液就呈现鲜红色。
(三)樟脑
樟脑是一类脂环状的酮类化合物,学名为2-莰酮,构造式为:
樟脑是无色半透明晶体,具有穿透性的特异芳香,味略苦而辛,有清凉感,熔点176-177℃,易升华。不溶于水,能溶于醇等。樟脑是我国的特产,台湾省的产量约占世界总产量的70%,居世界第一位,其它如福建、广东、江西等省也有出产。樟脑在医学上用途很广,如作呼吸循环兴奋药的樟脑油注射剂(10%樟脑的植物油溶液)和樟脑磺酸钠注射剂(10%樟脑磺酸钠的水溶液);用作治疗冻疮、局部炎症的樟脑醑(10%樟脑酒精溶液);成药清凉油、十滴水和消炎镇痛膏等均含有樟脑。樟脑也可用于驱虫防柱。
(四)麝香酮
麝香酮为油状液体,具有麝香香味,是麝香的主要香气成分。沸点328℃,微溶于水,能与乙醇互溶。麝香酮的构造为一个含15个碳原子的大环,环上有一个甲基和一个羰基,属脂环酮。
香料中加入极少量的麝香酮可增强香味,因此许多贵重香料常用它作为定香剂。人工合成的麝香广泛应用于制药工业。
第二节 醌
一、醌的构造和命名
醌是对含有环己二烯二酮构造的一类化合物的总称。如对苯醌![]() 、邻苯醌
、邻苯醌 等。
等。![]() 或
或![]()
叫做醌型构造。
具有醌型构造的化合物通常具有颜色。对位的醌多呈现黄色,邻位的醌多呈现红色或橙色,所以它是许多染料和指示剂的母体。
醌类化合物是以苯醌、萘醌等作为母体来命名的。两个羰基的位置可用阿拉伯数字标明写在醌名字前。也可用邻、对、远或α、β等表明两上羰基的相对位置。母体上如有取代基,可将取代基的位置、数目、名称写在前面。例如:
二、醌的化学性质
从醌的构造来看。其分子中既有羰基,又有碳碳双键和共轭双键,因此可以发生羰基加成、碳碳双键加成以及共轭双键的1,4-加成。
(一)羰基的加成
苯醌同醛、酮一样,可与羰基试剂发生加成反应。如以苯醌与羟胺反应,先生成对苯醌一肟,再生成对苯醌二肟。
(二)碳碳双键的加成
对苯醌和溴发生加成反应,可生成二溴化物或四溴 化物。
(三)共轭双键的1,4-加成
醌分子中含有共轭双键,可发生1,4-加成。如维生素K3与亚硫酸氢钠的加成。
三、重要的醌类化合物
(一)对苯醌
对苯醌是黄色晶体,熔点115.7℃,能随水蒸气蒸出,具有刺激性臭味,有毒,能腐蚀皮肤,能溶于醇和醚中。对苯醌很容易被还原成对苯二酚。
如将对苯醌的乙醇溶液和无色的对苯二酚的乙醇溶液混合,溶液颜色变为棕色,并有深绿色的晶体析出。这是一分子对苯醌和一分子对苯二酚结合而成的分子配合物,叫做醌氢醌,它的构造式表示如下:
在醌氢醌溶液中插入一铂片,即组成醌氢醌电极,这个电极的电位与溶液中的氢离子浓度有关,可用于测定溶液的氢离子浓度。
(二)α-萘醌和维生素K
α-萘醌又叫1,4-萘醌,是黄色晶体,熔点125℃,可升华,微溶于水,溶于酒精和醚中,具有刺鼻气味。
许多天然产物的色素含α-萘醌构造,例如维生素K1和K2。
维生素K1和K2的差别只在于侧链有所不同,维生素K1为黄色油状液体,维生素K2为黄色晶体。维生素K1和K2广泛存在于自然界中,绿色植物(如苜蓿、菠菜等)、蛋黄、肝脏等含量丰富。维生素K1和K2的主要作用是能促进血液的凝固,所以可用作止血剂。
在研究维生素K1和K2及其衍生物的化学构造与凝血作用的关系时,发现2-甲基-1,4-萘醌具有更强的凝血能力,称之不维生素K3,可由合成方法制得。
维生素K3为黄色晶体,熔点105-107℃,难溶于水,可溶于植物油或其它有机溶剂。由于维生素K3是油溶性维生素,故医药上用的是它的可溶于水的亚硫酸氢钠加成物。
第十六章 羧酸及其衍生物
羧酸(RCOOH)是最重要的一类有机酸。它可以看作是烃分子中的氢原子被羧基(
或写为-COOH)取代后生成的化合物,羧基是羧酸的官能团。羧酸能发生许多化学反应。当羧基中的羟基被其它原子团取代时,则形成羧酸衍生物,主要有羧酸酯、酰卤,酸酐和酰胺。
第一节 羧酸
羧酸在自然界中常以游离状态或以盐或酯的形式广泛存在于动植物体中,是与医药关系十分密切的一类化合物。
一、羧酸的分类及命名
按照烃基构造的不同,羧酸可分为脂肪族羧酸(饱和及不饱和的)、脂环族羧酸和芳香族羧酸。根据羧酸分子中所含羧基的数目,又可分为一元酸及多元酸。链状的一元羧酸(包括饱和的及不饱和的)通称为脂肪酸。羧酸的分类见表16-1。
表16-1 羧酸的分类
| 脂肪族羧酸 | 饱和羧酸 | 一元羧酸 | 二元羧酸 |
| CH2COOH | HOOC-COOH | ||
| 乙酸(醋酸) | 乙二酸(草酸) | ||
| 不饱合羧酸 | CH2=CH-COOH | HOOCCH=CHCOOH | |
| 丙烯酸 | 丁烯二酸 | ||
| 脂 环 族 羧 酸 | |||
| 环已烷羧酸 | 1,2-环戊烷二羧酸 | ||
| 芳香族羧酸 | |||
| 苯甲酸 | 邻苯二甲酸 | ||
许多羧酸可以从天然产物中获得,因此它们常根据最初的来源而有俗名,如蚁酸、醋酸、草酸等。羧酸的系统命名法与醛相似。饱和脂肪酸命名是以包括羧基碳原子在内的最长碳链作为主链,根据主链碳原子数称为某酸,从羧基碳原子开始编号。例如:

不饱和脂肪酸命名时,主链应是包括羧基碳原子和各碳碳重键的碳原子都在内的最长碳链,从羧基碳原子开始编号,并注明重键的位置。例如:
二元酸的命名是以包括两个羧基碳原子在内的最长碳链作为主链,按主链的碳原子数称为“某二酸”。例如;
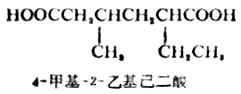
羧基直接连在脂环上的羧酸命名时,可在脂环烃的名称后加上“羧酸或二羧酸”等词尾;羧基在脂环上的羧酸命名是将脂环烃的名称与脂肪酸的名称连接起来。另外,不论羧基直接连在脂环上还是连在脂环侧链上,均可把脂环作为取代基来命名。例如;
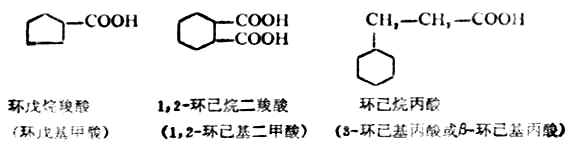
芳香酸可将其作为脂肪酸的芳香基取代物来命名。例如:
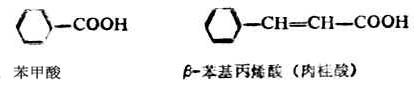
二、羧酸的物理性质
低级饱和脂肪酸(甲酸、乙酸、丙酸)是具有强烈刺激性气味的液体;中级的(C4-C9)羧酸是带有不愉快气味的油状液体;C10及C10以上的羧酸为无味的油状固体,挥发性很低,脂肪族二元羧酸和芳香族羧酸都是固体。
低级脂肪酸易溶于水,但随着相对分子质量的增加,在水中的溶解度减小,以至难溶或不溶于水,而溶于有机溶剂。
羧酸的沸点比相对分子质量相近的醇还要高。例如,甲酸和乙醇的相对分子质量相同,但乙醇的沸点为78.5℃,而甲酸为100.5℃。这是因为羧酸分子间能以氢键缔合成二聚体,羧酸分子间的这种氢键比醇分子间的更稳定。例如,乙醇分子间的氢键键能为25.94kJ·mol-1,而甲酸分子间的氢键键能则是30.12kJ·mol-1。低级羧酸即使在气态也是以二缔合体的形式存在。
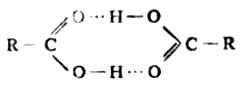
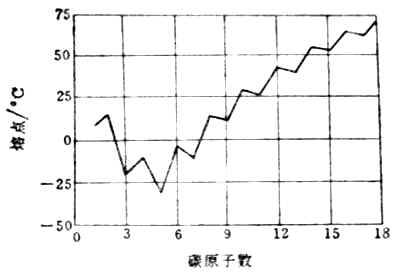
饱和脂肪酸熔点随着分子中碳原子数的增加呈锯齿形变化(图16-1)。含偶数碳原子的羧酸其熔点比其相邻的两个含奇数碳原子羧酸分子的熔点高。这可能是由于偶数碳原子羧酸分子较为对称,在晶体中排列更紧密的缘故。一些羧酸的物理常数和pKa值见表16-2。
表16-2 一些羧酸的物理常数和pKa
| 名称 | 构造式 | 熔点/℃ | 沸点/℃ | 溶解度g·(100g水)-1 | PKa (25℃)pKa1 ,pKa2 |
| 甲酸 | HCOOH | 8.4 | 100.5 | ∞ | 3.77 |
| 乙酸 | CH3COOH | 16.6 | 118 | ∞ | 4.76 |
| 丙酸 | CH3CH2COOH | -22 | 141 | ∞ | 4.88 |
| 正丁酸 | CH3CH2CH2COOH | -4.7 | 162.5 | ∞ | 4.82 |
| 正戊酸 | CH3(CH2)3COOH | -35 | 187 | 3.7 | 4.81 |
| 正己酸 | CH3(CH2)4COOH | -1.5 | 205 | 0.4 | 4.84 |
| 正庚酸 | CH3(CH2)5COOH | -11 | 223.5 | 0.24 | 4.89 |
| 正辛酸 | CH3(CH2)6COOH | 16.5 | 237 | 0.25 | 4.85 |
| 壬酸 | CH3(CH2)7COOH | 12.5 | 254 | 4.96 | |
| 癸酸 | CH3(CH2)8COOH | 31.5 | 268 | ||
| 软脂酸 | CH3(CH2)14COOH | 62.9 | 269(13Pa) | ||
| 硬脂酸 | CH3(CH2)10COOH | 69.6 | 287(13Pa) | ||
| 丙烯酸 | CH2=CHCOOH | 13 | 141 | 4.26 | |
| 乙二酸 | HOOC-COOH | 189 | 8.6 | 1.46 4.40 | |
| 己二酸 | HOOC(CH2)4COOH | 151 | 276 | 1.5 | 4.43 5.52 |
| 顺丁烯二酸 | 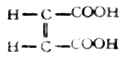 |
131 | 易溶 | 1.92 6.59 | |
| 反丁烯二酸 | 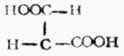 |
287 | 0.7 | 3.03 4.54 | |
| 苯甲 酸 | C6H5COOH | 122 | 249 | 0.34 | 4.19 |
| 苯乙酸 | C6H5CH2COOH | 78 | 265 | 1.66 | 4.28 |
| 萘乙酸 | 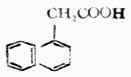 |
131 | 0.04 |
三、羧酸的化学性质
羧酸是由羧基和烃基组成的,羧基包括羰基和羟基两个部分,因而不同程度地反映了羰基和羟基的某些性质。但羧基的性质并非两个基团的简单加和,由于羰基和羟基的相互影响表现出许多新的性质。
用物理方法测定甲酸中C=O键长为0.1245nm,比普通羰基的键长(0.122nm)略长一点;C-OH键中的碳氧键长为0.131nm,比醇中的键长(0.143nm)短得多。这表明羧酸中羰基与羟基间发生了相互影响。
在羧酸分子中,羰基碳原子的三个sp2杂化轨道一个与氧成键,一个与羟基氧成键,另一个与氢或烃基成键,这三个轨道在一个平面上,键角约120°;碳原子上的一个未参与杂化的p轨道与氧原子的p轨道构成了π键。但羧基中-OH氧上有一对未共用的电子,可与π键形成p-π共轭体系。
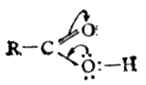
这样一来,一方面使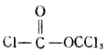
原子团失去了典型的羰基性质,另一方面-OH氧原子的电子云向羰基移动,氧的电子云密度降低,有利于氢的离解,故羧酸的酸性强于醇。
经X射对甲酸根离子的测定表明,它的两个碳氧键的键长都是0.127 nm 。这说明氢以质子形式脱离羧基后,p-π共轭作用更完全,发生了键的平均化。这样,-COO-上的负电荷不再集中于一个氧原子,而是平均分配在两个氧上,所以羧酸根离子更稳定.
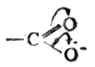
根据羧酸的构造,它可以发生如下反应。
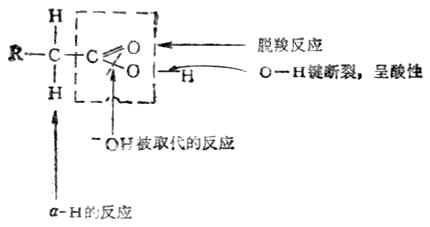
(一)酸性
羧酸在水中可离解出质子而显酸性,其pKa值一般为4-5,属于弱酸。
![]()
羧酸的酸性虽比盐酸,硫酸等无机酸弱得多,但比碳酸(pKa=6.35)和一般的酚类(pKa-10)强。故羧酸能分解碳酸盐和碳酸氢盐,放出二氧化碳。
2RCOOH+Na2CO3→2RCOONa+CO2↑+H2o
RCOOH+NaHCO3→RCOONa+CO2↑+H2o
利用羧酸与碳酸氢钠的反应可将羧酸与酚类相区别。因羧酸可溶于碳酸氢钠溶液并放出二氧化碳,而一般酚类与碳酸氢钠不起作用。
低级和中级羧酸的钾盐、钠盐及铵盐溶于水,故一些含羧基的的药物制成羧酸盐以增加其在水中的溶解度,便于做成水剂或注射剂使用,。
在羧酸(RCOOH)分子中,与羧基直接或间接直连的原子团对羧酸的酸性有不同程度的影响(表16-3)。
表16-3 一些羧酸的电离常数
| 化合物 | 构造式 | PKa |
| 1.甲酸 | HCOOH | 3.77 |
| 2.乙酸 | CH3COOH | 4.76 |
| 3.氯乙酸 | ClCH2COOH | 2.86 |
| 4.二氯乙酸 | Cl2CHCOOH | 1.29 |
| 5.三氯乙酸 | Cl3CCOOH | 0.65 |
| 6.溴乙酸 | BrCH2COOH | 2.90 |
| 7.碘乙酸 | ICH2COOH | 3.18 |
| 8.氟乙酸 | FCH2COOH | 2.66 |
| 9.三氟乙酸 | F3CCOOH | 强酸 |
| 10.丁酸 | CH3CH2CH2COOH | 4.82 |
| 11.α-氯丁酸 | 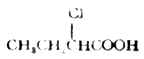 |
2.84 |
| 12.β-氯丁酸 | 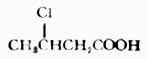 |
4.06 |
| 13.γ-氯丁酸 | CLCH2CH2CH2COOH | 4.52 |
和脂肪酸中,与羧基相连的烷基具有供电诱导效应(+I),使羧基上的氢较难离解,酸性较甲酸弱(表16-3中的1,2)。当卤素取代羧酸分子中烃基上的氢后,由于卤原子的吸电子诱导效应(-I),酸性增强(表16-3中的3,6,7,8)。烃基某个碳上引入的卤原子的数目越多,酸性越强(表16-3中的3,4,5及8,9)当卤原子相同时,卤原子距羧基越近,酸性越强(表16-3中的11,12,13)。当卤原子的种类不同时,它们对酸性的影响是F>CL>Br>I。所以氟乙酸的酸性>氯乙酸>溴乙酸>碘乙酸(表16-3中的3,6,7,8)。
(二)羟基被取代的反应
羧酸中的羟基可以被其它原子或原子团取代,生成羧酸衍生物。例如:
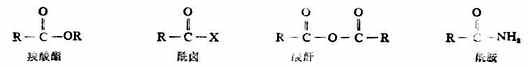
羧酸分子中去掉羧基上的羟 基后,余下的原子团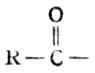
叫做酰基。
1.酯化反应
酸与醇脱水生成酯的反应叫做酯 化。
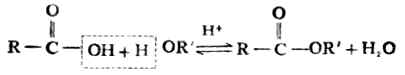
羧酸与醇的酯化反应是可逆的,而且反应速率很慢,需用酸作催化剂。例如:
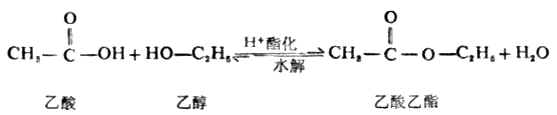
2.酰卤的生成
羧酸(除甲酸外)能与三卤化磷、五卤化磷或亚硫酰氯(SOCL2)反应,羧基中的羟基被卤素取代生成相应的酰卤。
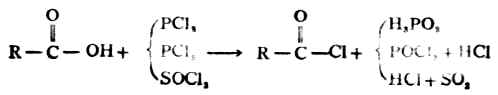
例如:
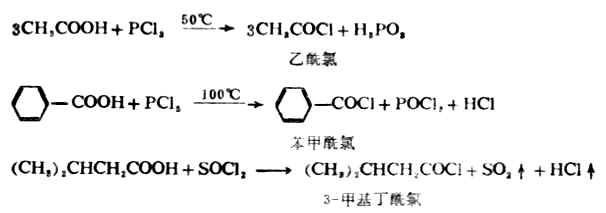
应用SOCL2制备酰卤时,副产物都是气体,便于处理及提纯。
3.酸酐的生成
除甲酸外,一元羧酸与脱水剂共热时,两分子羧酸可脱去一分子水,生成酸酐。
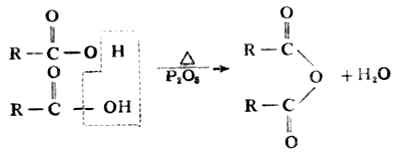
4.酰胺的生成
在羧酸中通入氨气或加入碳酸铵,可以得到羧酸的铵盐。将固体的羧酸铵加热,分子内失去一分子水生成酰胺。
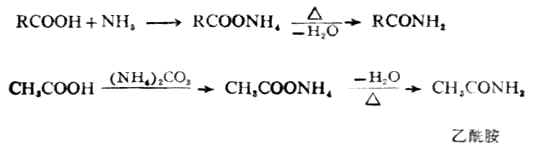
(三)脱羧反应和二元羧酸的受热反应
羧酸脱去羧基的反应叫做脱羧。这个反应的结果是从羧基脱去CO2。
![]()
除甲酸外,一元羧酸较稳定,直接加热时难以脱羧,只有在特殊条件下才可发生,生成少一个碳的烃。例如:
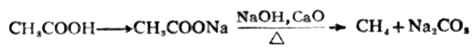
生物体内发生的许多重要的脱羧反应是在脱羧酶的作用下进行的。
有些二元酸对热不稳定,在加热或与脱水剂共热的条件下,随两个羧基间距不同而发生脱羧反应或脱水反应,这是二元羧酸的特性。
1.乙二酸和丙二酸
乙二酸或丙二酸加热脱羧生成一元羧酸。
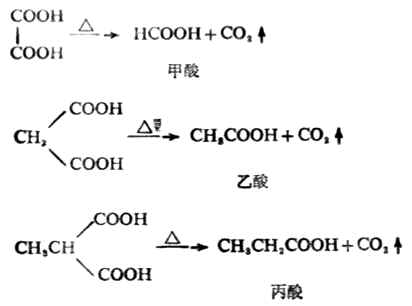
2.丁二酸、戊二酸及邻苯二甲酸
这三种酸与脱水剂共热时失水,生成环状酸酐。
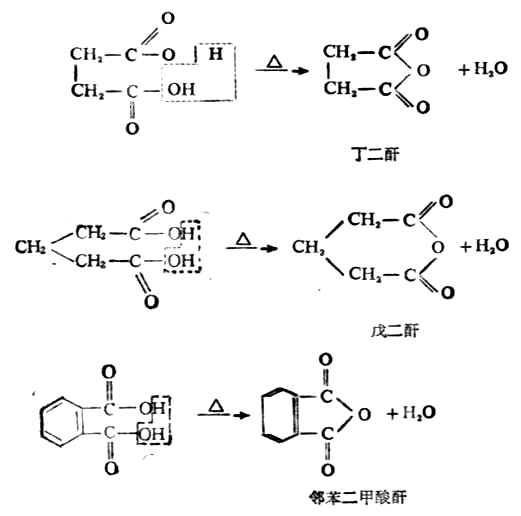
3.己二酸,庚二酸
己二酸、庚二酸与氢氧化钡共热时,既失水又脱羧 ,生成环酮。
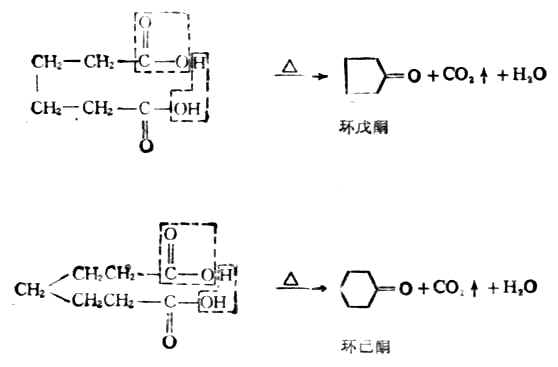
(四)α-H的卤代作用
与羰基相似,羧基也能活化α-H,但其致活作用比羰基小得多。因此,羧酸中的α-H被卤素取代的反应较慢,需加入红磷、硫或碘等作催化剂或在光照下才易进行。
![]()
四、重要的羧酸
(一)甲酸
甲酸最初是从红蚂蚁体内发现的,所以俗称蚁酸。它是无色有刺激性的液体,沸点100.5℃,易溶于水。甲酸的腐蚀性很强,能使皮肤起泡。
甲酸的构造比较特殊,分子中的羧基与氢原子相连,既具有羧基的结构又有醛基的结构,因而既有酸性又有还原性,能发生银镜反应或使高锰酸钾溶液褪色。
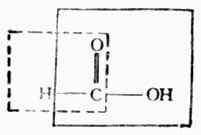
(二)乙酸
乙酸俗名醋酸,是食醋的主要万分。乙酸为无色有刺激气味的液体,熔点16.6℃,沸点118℃。由于乙酸在16.6℃以下能凝结成冰状固体,所以常把无水乙酸称为冰醋酸。乙酸易溶于水,也能溶于许多有机物。乙酸还是重要的工业原料。
(三)乙二酸
乙二酸![]()
俗名草酸,在大部分植物尤其是草本植物中常以盐的形式存在。草酸是无色晶体。常见的草酸含有两分子结晶水。无水草酸的熔点189℃,加热到150℃以上时就开始分解生成甲酸及二氧化碳,甲酸再分解为一氧化碳和水。
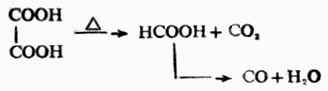
草酸具有还原性,在分析化学中常用来标定KMnO4溶液的浓度。
(四)苯甲酸
苯甲酸![]()
俗名安息香酸。它与芐醇形成的酯存在于天然树脂与
安息香胶内。苯甲酸是白色固体,熔点121℃,微溶于水,受热易升华。苯甲酸有抑菌,防腐作用。可作防腐剂,也可外用。
第二节 羧酸衍生物
一、酰卤、酸酐、酯的构造和命名
羧酸衍生物是指羧酸分子中,羧基中的羟基被其它原子或原子团取代后生成的化合物。
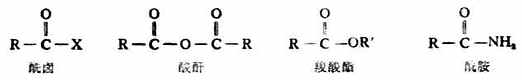
羧酸衍生物在构造上的共同之处是分子中均含有酰基![]() 。
。
最常见的酰卤是酰氯和酰溴,他们可根据相应的酰基来命名。例如:
羧酸酯常根据相应的羧酸和醇来命名。一元醇的羧酸酯叫做“某酸某酯”。例如:

多元醇的羧酸酯命名时,通常是醇的名称在前,羧酸的名称在后,叫“某醇某酸酯”。例如:
酸酐是按照相应的羧酸的名称叫做某(酸)酐。例如:
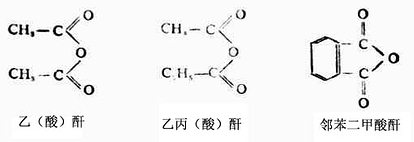
二、酰卤、酸酐、酯的物理性质
低级的酰卤与酸酐都是具有强烈刺激性气味的液体,遇水即分解。高级的酰卤和酸酐为固体,不溶于水。
低级的羧酸酯是具有香味的液体,微溶于水,高级羧酸酯为蜡状固体,羧酸酯均溶于有机溶剂,许多有机物也能溶于羧酸酯中,故有些羧酸酯也可作为溶剂。
酰卤、酸酐和羧酸酯由于分子间不存在氢键,它们的沸点比相对分子质量相近的羧酸的沸点低得多。
三、酰卤、酸酐、酯的化学性质
酰卤、酸酐和羧酸酯在分子构造上有相似之处,故它们的化学性质相似,都能与水、醇和氨作用而发生水解、醇解和氨解反应。但它们的反应活性不同,以酰卤最活泼,酸酐次之,羧酸酯较不活泼。
(一)水解
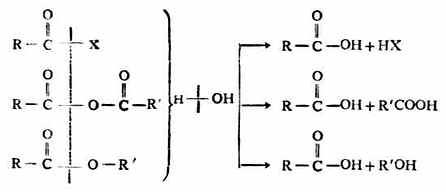
酰卤、酸酐和羧酸酯水解的共同产物是羧酸;与此同时,酰卤生成卤化氢,酸酐生成另一分子羧酸,羧酸酯则得到醇。羧酸酯的水解是酯化的逆反应,必须在酸或碱存在下加热才能较快地进行。在酸催化下的水解反应可较快地达到平衡。在碱的催化下,由于反应生成的羧酸被碱中和生成羧酸盐,使平衡右移,水解反应能进行到底。
(二)醇解
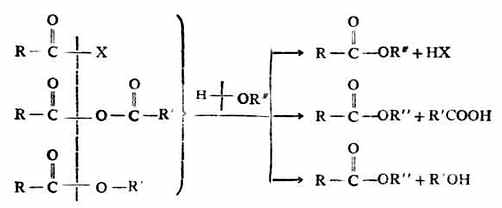
酰卤,酸酐和羧酸酯与醇反应均有羧酸酯生成,其中,羧酸酯的醇解是可逆反应,须在催化剂存在下进行。这个反应是从一种羧酸酯转变成另一种羧酸酯。因此又叫酯交换。例如:
![]()
(三)氨解
酰卤、酸酐和羧酸与氨(或胺)发生氨解时的相同产物是酰胺(或N-取代酰胺)。
羧酸衍生物水解时都产生羧酸;醇解时都生成羧酸酯;氨解时都生成酰胺。因此,它们的水解、醇解和氨解又是水,醇,氨(或胺)分子中的一个氢(醇是羟基上的氢,胺是氮上的氢)被酰基取代的反应。这类在分子中引入酰基的反应称为酰化。酰卤、酸酐的反应活性大,易进行酰化反应,因此常作为酰化剂。
酰化反应在药物合成中具有重要意义。在某些药物中引入一个酰基,常可增加药物的脂溶性,改善体内吸收,降低毒性,提高或延长药效。例如:
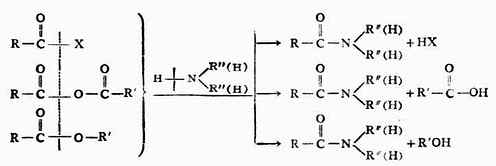
四、重要的羧酸衍生物
(一)乙酐
乙酐又称醋酐,是常用的酰化剂,它是无色有刺激气味的液体,沸点140℃,工业上,醋酐用于合成醋酸纤维,染料,药物和香料等。
(二)邻苯二甲酐
邻苯二甲酐![]() 是无色针状晶体,熔点128℃,是一种常用的
是无色针状晶体,熔点128℃,是一种常用的
酰化剂。它与某些酚类反应,能生成一些显色的化合物,例如,酚酞,荧光素等。
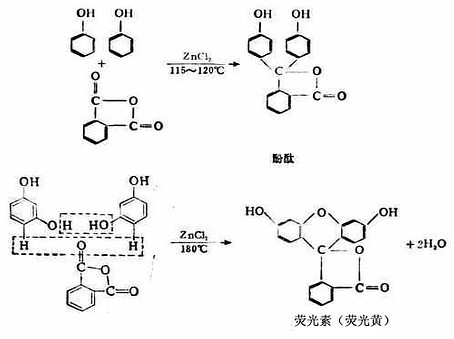
酚酞为无色固体,熔点261℃,难溶于水而溶于乙醇,在医药上用作轻泻剂。由于酚酞在碱性溶液中呈紫红色。在酸性溶液中无色,故常作为酸碱滴定指示剂。
荧光素在碱性溶液中呈橙色,并有绿色荧光。当两个溴原子取代荧光素的氢原子后,再引进一个HgOH原子团,生成的化合物叫汞溴红(红汞),其水溶液为鲜红色,常用作杀菌消毒剂。
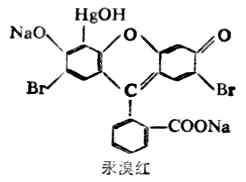
(三)光气和双光气
光气(COCL2)是碳酸的二酰氯,常温下为无色气体,能压缩成液体,沸点8.3℃,易溶于苯,甲苯。光气是一种窒息性毒剂。它和酰氯一样,性质活泼,能与水、醇、氨作用而分解,温度升高时,分解速率加快。
双光气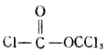
氯甲酸三氯甲酯)可从光气经部分醇解再氯代而成。
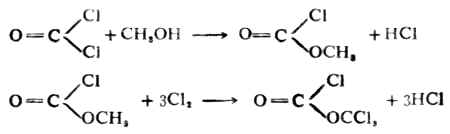
双光气分子中的各原子数是光气的两倍,能分解生成两分子的光气,故叫双光气。纯净的双光气是无色透明液体,沸点127℃,含有杂质时常呈黄色。它难溶于水,易溶于苯,四氯化碳及其他有机溶剂中。双光气的性质与光气相似,但比光气稳定。
第十七章 取代羧酸和对映异构
取代羧酸可以看成是羧酸分子中烃基上的氢原子被其他官能团取代后的生成物。最常见的是氢原子分别被卤素、羟基、氧原子或氨基取代,生成卤代酸、羟基酸、氧代酸或氨基酸。例如:
卤代酸
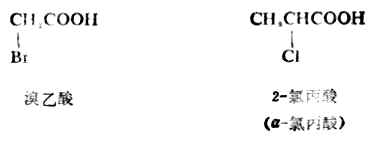
羟基酸

氧代酸

氨基酸
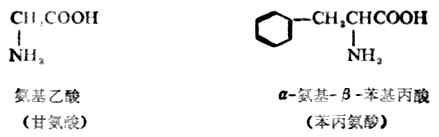
本章主要讨论羟基酸和氧化酸。
第一节 羟基酸
一、羟基酸的构造及分类
羟基酸是分子中同时具有羟基和羧基两种官能团的化合物,又可分为醇酸和酚酸两类。
醇酸:
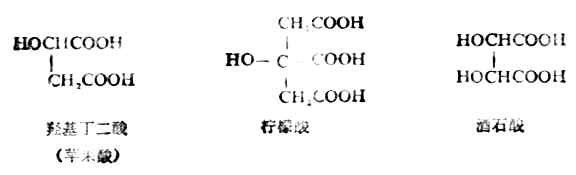
酚酸:
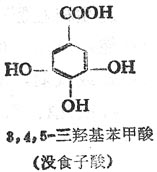
醇酸还可以根据羟基与羧基的相对位置,分为α-,β-,γ-,δ-…羟基酸。
二、羟基酸的命名
羟基酸以及其他含两种或几种官能团的化合物用系统命名法命名时,在这些官能团中选择一种作为主官能团,并以相应的化合物为母体,其他的官能团都看作是取代基。
选择主官能团的优先顺序依次为:
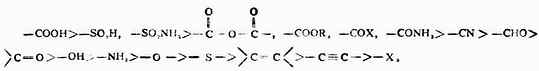
因此,只要是分子中含有羧基,该化合物一般即以相应的羧酸为母体,其他官能团作为取代基来命名。例如:
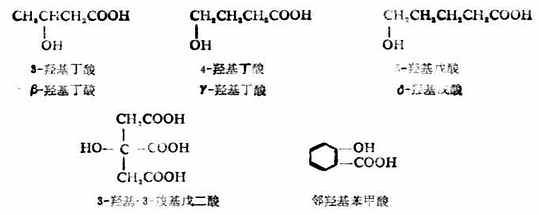
许多羟基酸还有俗名,其应用往往比系统名称更为广泛。因此,对于与医学有关的重要取代羧酸的俗名及其构造式都须记住。
三、羟基酸的物理性质
醇酸一般是粘稠的液体或晶体,易溶于水,其溶解度通常都大于相应的脂肪酸。这是由于分子中同时含有羟基和羧基两个极性基团,它们都能与水形成氢键的缘故。醇酸不易挥发,在常压下蒸馏时会发生分解。
酚酸大多为晶体,其熔点比相应的芳香酸高。有些酚酸易溶于水,如没食子酸;有的微溶于水,如水杨酸。
四、羟基酸的化学性质
含有两种或两种以上官能团的化合物,在一般情况下,具有各官能团的基本化学性质。但由于两种官能团存在于同一分子中,就有可能发生相互影响。因此,在分析各化合物的分子构造以推测其性质时,除注意哪些性质是各个官能团所固有的以外,还须注意:(1)某一个官能团受另一个官能团的影响,例如,活性的增强或减弱,新性质的出现以及不发生某种基本反应等;(2)一种试剂可能同时与分子中的两种或几种官能团都发生反应。
(一)羧基的性质
1.酸性
羟基酸的羧基能电离,能与碱反应生成盐。例如:
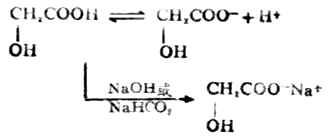
羟基能增强羧基的酸性,但影响不大。
2.酯化
在酸性催化剂存在时,羟基酸与醇发生酯化作用。例如:
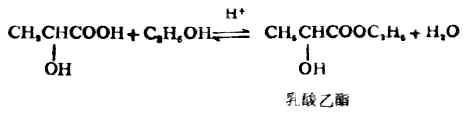
但由于酸的作用及受热的结果,在酯化的同时,往往还有副反应发生。
(二)羟基的性质
羟基酸与氧化剂反应时,根据羟基所连的碳是伯或仲碳原子,而有不同的反应产物。
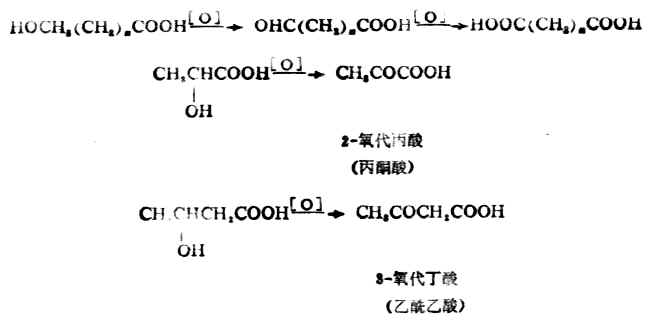
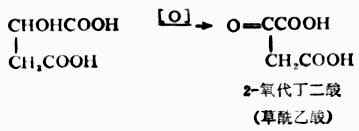
(三)羟基酸受热的反应
1.α-羟基酸
α-羟基酸受热时,发生双分子间的脱水反应,即它们之间交叉酯化,生成环状化合物----交酯。
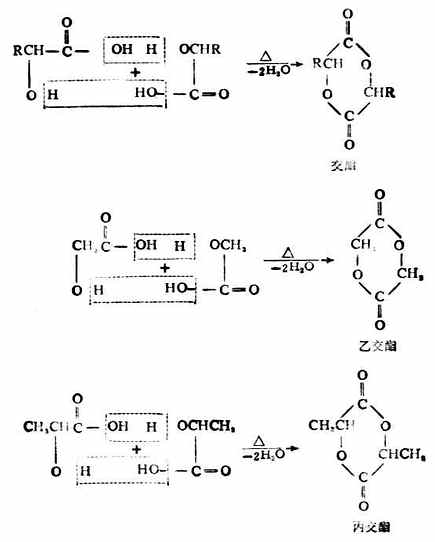
2.β-羟基酸
β-羟基酸受热时,发生消去反应,主产物是α,β-烯酸。
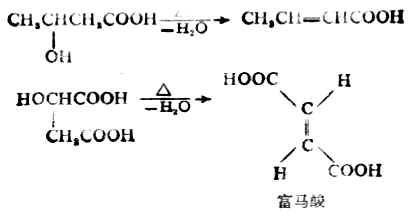
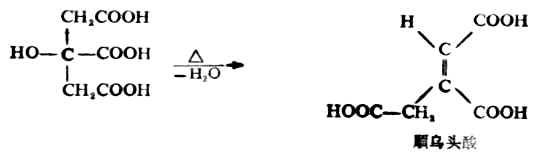
3.γ-及δ-羟基酸
γ-或δ-羟基酸受热时,发生分子内的酯化反应,生成五元或六元的环状内酯。
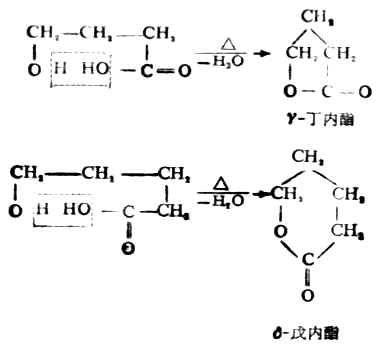
γ-内酯比δ-内酯容易生成。
(四)酚酸的反应
酚酸含有酚式羟基,能与FeCL3发生颜色反应。例如,FeCL3与水杨酸呈紫红色,与没食子酸显蓝黑色。
酚酸的羧基处于羟基的邻位或对位时,受热后易脱羧。
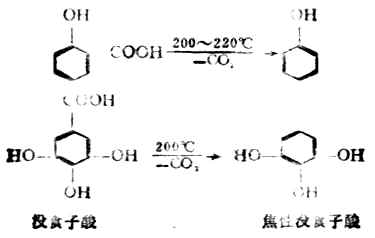
五、个别羟基酸
(一)乳酸
乳酸![]() 存在于酸牛奶中,它也是肌肉中糖原的代谢产物。纯净的乳酸是无色粘稠液体,熔点18℃,有强的吸水性,溶于水、乙醇和乙。醚乳酸的用途极广泛,在医药上可用于空气消毒,其钙盐用作治疗佝偻病等缺钙症,钠盐用为解除酸中毒的药物。乳酸还大量用在食品、饮料及皮革工业中。
存在于酸牛奶中,它也是肌肉中糖原的代谢产物。纯净的乳酸是无色粘稠液体,熔点18℃,有强的吸水性,溶于水、乙醇和乙。醚乳酸的用途极广泛,在医药上可用于空气消毒,其钙盐用作治疗佝偻病等缺钙症,钠盐用为解除酸中毒的药物。乳酸还大量用在食品、饮料及皮革工业中。
(二)β-羟基丁酸
β-羟基丁酸
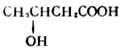
是无色晶体,熔点49-50℃,吸湿性强一
般为糖浆状;易溶于水、乙醇和乙醚,不溶于苯。它是人体脂肪酸代谢的中间产物,易氧化为乙酰乙酸。受热时,脱水为α,β-丁烯酸。
(三)酒石酸
酒石酸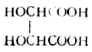
(二羟基丁二酸)存在于各种水果中,葡萄中含量
较多。从自然界得到的酒石酸是无色晶体,熔点170℃,易溶于水。其盐酒石酸锑钾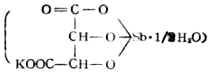
用于治疗血吸虫病,酒石酸钾钠
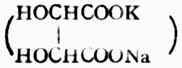
用以配制费林溶液。
(四)柠檬酸
柠檬酸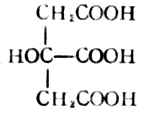
(枸椽酸)存在于柑桔类果实中。它是无色透明
晶体,熔点137℃,易溶于水、乙醇和乙醚。柠檬酸是糖代谢的中间产物。它常用于配制饮料。其钠盐为抗血凝药,铁铵盐可用于儿童缺铁性贫血。
(五)水杨酸
水杨酸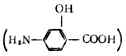
的钠盐(PAS-Na)有抑制结核菌的作用。
第二节 氧代酸
氧代酸可以看作是羧酸分子中烃基上的两个氢原子被氧原子取代后的生成物,包括醛酸和酮酸两类。
一、氧代酸的构造及命名
分子中含有醛基或酮基的羧酸分别叫做醛酸或酮酸。最简单的醛酸是乙醛酸,最简单的酮酸是丙酮酸。
醛酸和酮酸的系统命名是以羧酸为母体,以包括羧基及醛基(或酮基)碳原子都在内的最长碳链作为主链,称为某酸,氧原子作为取代基并指出其位置。例如:

有些酮酸尚有医学上的习惯名称,例如丙酮酸、乙酰乙酸及α-酮戊二酸等,它们都是与人体代谢有重要关系的化合物。
二、氧代酸的化学性质
(一)羧基的性质
醛酸和酮酸都含有羧基,具有羧基的基本性质,如酸性、成盐、成酯及生成酰卤等。
(二)羰基的性质
醛酸含有醛基,具有醛基的基本性质,酮酸也同样,都能发生还原应。
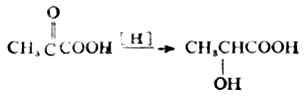
(三)α-酮酸及β-酮酸的特殊反应
α-酮酸与稀硫酸共热时,脱羧后的主产物是醛。
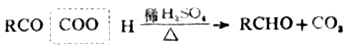
β-酮酸不稳定,受热时很容易脱羧成酮。
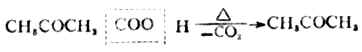
三、酮式-烯醇式互变异构现象
乙酰乙酸乙酯(CH3COCH2COOC2H5)是β-酮酸——乙酰乙酸的酯。它不同于β-酮酸,比较稳定。乙酰乙酸乙酯是无色有香味的液体,沸点180.4℃,微溶于水,易溶于乙醇、乙醚及大多数有机溶剂。它是有机合成的重要原料。
乙酰乙酸乙酯具有酮和羧酸酯的基本性质,能与HCN,NaHSO3,羟胺及苯肼反应,以稀NaOH水解为乙酰乙酸和乙醇。此外,乙酰乙酸乙酯还能使溴溶液裉色,与金属钠作用放出氢气,与FeCL3呈紫红色。这些性质表明乙酰乙酸乙酯还应具有烯醇式构造。
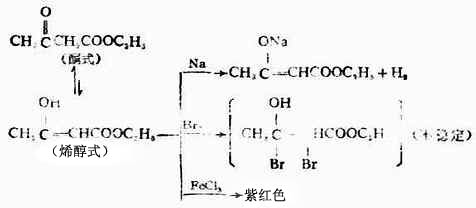
实际上,乙酰乙酸乙酯是其酮式构造与烯醇式构造的平衡混合物。在水溶液中,酮式占优势。
如将此平衡混合物溶解在石油醚中,冷至-78℃,可以得到酮式的晶体。如将平衡混合物与金属钠反应生成的烯醇钠,在-78℃,可以得到酮式的晶体。但是,无论是将酮式的晶体或烯醇式的油状液放置一定时间,或用适当溶剂溶解后再放置,都将成为酮式与烯醇式的平衡混合物。
乙酰乙酸乙酯的酮式与烯醇式是构造异构体,二者的差别仅在于一个双键及一个质子的位置不同。在酮式中是C=O双键,质子连在羧酸酯基的α碳上;在烯醇式中是C=C双键,质子连在羧酸酯基的β碳所连的羟基中。酮式与烯醇式之间很容易相互转化,只要有痕量的酸或碱,甚至玻璃容器的器壁,都能促其转变,建立平衡。因此,把这种构造异构现象叫做互变异构。乙酰乙酸乙酯的酮式与烯醇式异构称为酮式-烯醇式互变异构。
凡含 α-H碳基化合物都有酮式-烯醇式互变异构。酮式与烯醇式的比例与其分子构造及介质等有关。在醛或酮中也有酮式-烯醇式互变异构平衡存在,羰基的α-H作为质子转移,不过在平衡混合物中,烯醇所占的比例太小。
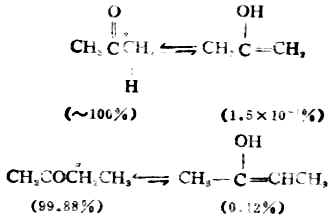
在1,3-二羰基化合物中,烯醇式的比例大大增加,例如,2,4-戊二酮(乙酰丙酮)的水溶液中含16%的烯醇,而其己烷溶液中,烯醇式占92%。
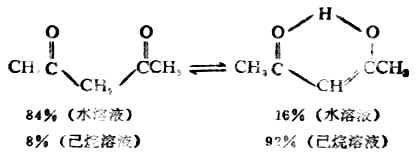
1,3-二酮含有大量烯醇式的原因有二:一是π电子云的离域使烯醇式比较稳定,二是生成的烯醇能借分子内氢键形成六元环。
乙酰乙酸乙酯的烯醇式也能形成分子内氢键,同时与羧酸酯基中的 形成共轭体系,因而也有较多的烯醇式。由于酮基对α-H的作用强于羧酸酯基中的 ,所以α-H移向酮基而不移向羧酸酯基。
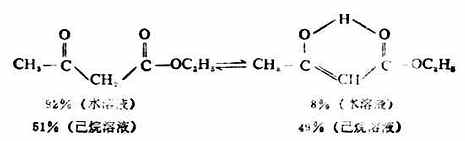
四、个别氧代酸
(一)丙酮酸
丙酮酸CH3COCOOH是无色具刺激性臭味的液体,沸点167℃,能与水混溶。其酸性强于丙酸及乳酸。丙酮酸及其烯醇式(烯醇式丙酮酸![]()
)是人体糖代谢的重要中间产物。在酶的作用下,丙酮酸可还原为乳酸,也可以脱羧为乙醛。
(二)乙酰乙酸
乙酰乙酸CH3COCH2COOH是无色粘稠液体,不稳定,很易脱羧为丙酮,也能还原为β-羟基丁酸。乙酰乙酸、β-羟基丁酸及丙酮是脂肪酸在人体内不完全氧化的中间产物,合称为酮体。正常情况下,人血中酮体的含量很少(0.8-5mg/100ml)。正常人每昼夜从尿中排出约40mg酮体。在某些情况下,例如饥饿、糖尿病等,血液中酮体的含量增加(300-400mg/100ml)。由于乙酰乙酸及β-羟基丁酸的酸性,会使血液的PH值下降乃至引起酸中毒。
(三)草酰乙酸
草酰乙酸HOOCCH2COCOOH是能溶于水的晶体,具有一般二元酸及酮的性质,也有酮式-烯醇式互变异构:它也是人体内糖代谢的中间产物。
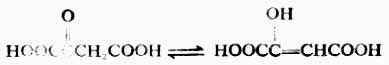
(四)α-酮戊二酸
α-酮戊二酸HOOCCOCH2CH2COOH是晶体,熔点109-111℃,溶于水。它具有α-酮酸的一般性质,也是人体内糖代谢的中间产物。
第三节 对映异构
同分异构现象在有机化合物中十分普遍,它包括构造异构和立体异构两大类: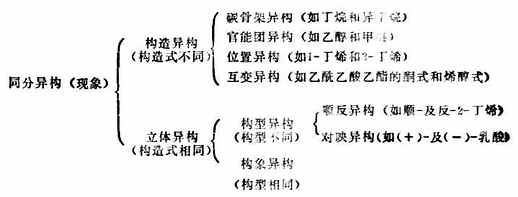
对映异构是立体异构中的一类,表现在各个对映异构体对平面偏振光的作用不同。
一、平面偏振光和物质的旋旋光性
(一)偏振光和偏振光的振动面
光波是电磁波,是横波。其特点之一是光的振动方向垂直于其传播方向。普通光源所产生的光线是由多种波长的光波组成,它们都在垂直于其传播方向的各个不同的平面上振动。图17-1(左)表示普通的单色光束朝我们的眼睛直射过来时的横截面。光波的振动平面可以有无数,但都与其前进方向相垂直。
图17-1 平面偏振光的形成
图17-2 两个尼科耳棱晶平行放置(上)或重直放置(下)时的情况
当一束单色光通过尼科目棱晶(由方解石晶体加工制成,图17-1中)时,由于尼科耳棱晶只能使与其晶轴相平行的平面内振动的光线通过,因而通过尼科耳棱晶的光线,就只在一个平面上振动。这种光线叫做平面偏振光,简称偏振光(图17-1右)。偏振光的振动方向与其传播方向所构成的平面,叫做偏振光的振动面。
当普通光线通过尼科耳棱晶成为偏振光后,再使偏振光通过另一个尼科耳棱晶时,则在第二个尼科耳棱晶后面可以观察到:如果两个尼科耳棱晶平行放置(晶体相互平行)时,光线的亮度最大(图17-2上);如两个棱晶成其他角度时,则光线的亮度发生不同程度的减弱,接近90°时较暗,接近0°时较明亮。
(二)旋光性物质和物质的旋光性
自然界中有许多物质对偏振光的振动面不发生影响,例如水、乙醇、丙酮、甘油及氯化钠等;还有另外一些物质却能使偏振光的振动面发生偏转,如某种乳酸及葡萄糖的溶液。能使偏振光的振动面发生偏转的物质具旋光性,叫做旋光性物质;不能使偏振光的振动面发生偏转的物质叫做非旋光性物质,它们没有旋光性。
当偏振光通过旋光性物质的溶液时,可以观察到有些物质能使偏振光的振动面向左旋转(逆时针方向)一定的角度(图17-3),这种物质叫做左旋体,具有左旋性,以“-”表示;另一些物质则使偏振光的振动面向右旋转(顺时针方向)一定的角度,叫做右旋体,它们具有右旋性,以“+”表示。以前也曾用“l、d”表示左右旋。
图17-3 左旋体使偏振光的振动面向左旋转
(三)旋光度和比旋光度
如将两个尼科耳棱晶平行放置,并在两个棱晶之间放一种溶液(图17-4),在第一个棱晶(起偏振器)前放置单色可见光源,并在第二个棱晶(检偏振器)后进行观察。可以发现,如在管中放置水、乙醇或丙醇时,并不影响光的亮度。但如果把葡萄糖或某种乳酸的溶液放于管内,则光的亮度就减弱以至变暗。这是由于水、乙醇等是非旋光性物质,不影响偏振光的振动面;而葡萄糖等是旋光性物质,它们能使偏振光的振动面向右或左偏转一定的角度。要达到最大的亮度,必须把检测振器向右或向左转动同一角度。旋光性物质的溶液使偏振光的振动面旋转的角度,叫做旋光度,以α表示。
图17-4 旋光性测定示意图
一种物质的旋光性,主要决定于该物质的分子结构。但在测定物质的旋光度时,还受到测定条件的明显的影响。影响旋光度的因素包括溶液浓度、液层厚度(即盛液管的长度)、所用光线(单色光)的波长、温度以及溶剂等。因此,同一种旋光性物质在不同条件下测定α值时,所得的结果也不一样。但如固定实验条件,则测得的物质的旋光度即为常数,它能反映该旋光性物质的本性,叫做比旋光度,以[α]表示。比旋光度与测得的旋光度(α)有以下的关系:
![]()
式中:λ——测定时所用单色光的波长,通常用钠光的D线(λ=589nm)
c——溶液浓度(g·ml-1)
l——盛液管的长度(dm)
当c和l都等于1时,则[α]= α。因此,物质的比旋光度就是浓度为1g·ml-1的溶液,放在1dm长的管中测得的旋光度。所用溶剂须写在比旋光度值后面的括号中。因为即使在其他条件都相同时,改变溶剂也会使[α]值发生变化。
比旋光度是旋光性物质的一种物理常数。如像每种物质都有一定的熔点、沸点、折射率、密度一样,各种旋光性物质都有其比旋光度。
二、化合物的旋旋光性与结构的关系
(一)三种乳酸
自然界中有许多种旋旋光性物质。例如,人体中肌肉运动时可产生乳酸,
其[α]20D为+3.82°(水);由左旋乳酸杆菌使乳酸发酵得另一种乳酸,[α]20D是-3.82°(水)。这两种乳酸的构造式都是![]() ,它们的性质除旋
,它们的性质除旋
旋光性不同(旋光方向相反,比旋亮度的绝对值相同)外,其他物理、化学性质都一样(表17-1)。这两种乳酸的分子结构可用球棒模型表示(图17-5)。
表17-1三种乳酸性质的比较
| [α]20D(水) | 熔点/℃ | PKa | |
| (+)-乳酸 | +3.82° | 53 | 3.79 |
| (-)-乳酸 | -3.82° | 53 | 3.79 |
| (±)-乳酸 | 18 | 3.86 |
图17-5 (+)-乳酸及(-)-乳酸的球棒模型
从模型可以看出,左旋乳酸与右旋乳酸的分子结构的关系有如物体与其镜象的关系,但二者不能重合,好比人的左手与右手、左脚与右脚一样。(+)-乳酸与(-)-乳酸的构造式相同而构型不同,所以属于立体异构中的构型异构。这两个构型异构体互呈物体与其镜象关系,能对映而不能重合,故把它们叫做对映体。这种立体异构属于对映异构。
一个物质可能有两个、三个或多个具有旋光性的异构体。如果某物质只有两个具有旋光性的异构体,它们一定是对映体。如果某物质有不止两个具有旋光性的异构体,则各异构体之间并不都是对映体的关系,这将在后讨论。
除了上述的(+)-用(-)-乳酸外,人工合成法所得的乳酸没有旋光性,即[α]20D=0。这种乳酸叫做外消旋乳酸,用(±)-乳酸表示(表17-1)。(±)乳酸是由等物质的量的(+)-及(-)-乳酸组成的。
由此可见,乳酸有三种:(+)-、(-)-、及(±)-乳酸。
(二)、分子的手性和手性分子
如将一个物体放在平面镜前使之成像“取”出,则物体与其镜象是否相同,即能否重合呢?这自然只有两种可能,即可以重合或不能重合。如果是人的一只手,则与其镜象不能重合(图17-6)。因为左手的镜象是右手,它们相互是不可能重合的。物体与其镜象不能重合的例子很多,例如螺丝钉(图17-7)、人的耳朵等。
图17-6 左:左、右手不能重合
右:左手的镜象是右手
图17-7 物体与其镜象不能重合(α)右旋弹簧与左旋弹簧;(b)蜗牛壳;(c)左螺纹与右螺纹螺丝钉
上述情况在有机化合物中也存在。许多分子能与其镜象重合,例如甲烷、乙醇、乙醚、丙酮等。但也有许多分子与其镜象不能重合,例如(+)-乳酸及(-)-乳酸的分子结构之间的关系好比人的左手与右手的关系,因此把这种分子叫做手性分子,它们具有手性。凡是手性分子都有旋光性。如果一个分子与其镜象等同,即能重合,则叫做非手性分子,非手性分子没有旋光性。
一个物质的分子是否具有手性是由它的分子结构决定的。最常见的手性分子是含手性碳原子的分子。所谓手性碳原子是指连有四个不同的原子或原子团的碳原子,这种碳原子常以星号“*”标示。例如乳酸分子中有三个碳,但只有C-2才是手性碳原子,它连接的是-H,-OH,-CH3及-COOH这四个原子或原子团。手性碳原子也叫做不对称碳原子。
凡是含有手性碳原子的分子都有对映异构体,但是含手性碳原子的分子不一定是手性分子(见本节四)。
三、含一个手性碳原子的分子
含一个手性碳原子的化合物有一对对映异构体。
(一)外消旋体
两个对映体的等物质的量混合物的比旋亮度为零。这种混合物叫做外消旋体。与各对映体相比较,外消旋体无旋旋光性外,其理化性质也不同,它的生理或药理作用与各对映体往往有明显的差异。
除了用特殊方法外,用通常化学合成的具手性碳原子的化合物,基本上是外消旋体。要想从外消旋体得到旋光纯的异构体,要采用特定的方法把左旋体与右旋体分开,这个过程叫做拆分。
(二)对映异构体的构型
1.
为了方便起见,对映异构体的构型通常采用费歇尔投影式来表示,即把手性碳原子所连的四个原子或原子团按规定的方法投影到纸上。这种方法包括:(1)手性碳原子写在纸平面上,或用一个“+”字形的交叉点代表这个手性碳,四端分别连四个不同的原子或原子团;(2)以垂直与手性碳相连的是伸向纸平面手后方的两个原子或原子团,以水平线与手性碳原相连的是伸向纸平面前方的两上原子或原子团;(3)通常把碳链放在垂直线上,并把命名时编号最小的碳原子放在上端。费歇尔投影式是以两维式来表示含手性碳原子的分子的三维结构。
2.相对构型与绝对构型
物质分子中各原子或原子团在空间的实际排布叫做这种分子的绝对构型。现在已能用X射线衍射等方法测定了许多化合物分子的绝对构型,但在1951年以前还没有解决这个问题。1906年,罗沙诺夫建议把(+)-及(-)-甘油醛作为其他旋光性异构体物质的构型的比较标准,并人为地规定,在费歇尔投影式中,手性碳上的OH排在横线右边的为右旋甘油醛(Ⅰ),作为D型,手性碳上的OH排在横线左边的为左旋甘油醛(Ⅱ),作为L型。D-及L-分别表示它们的构型。应注意,D及L仅表示其构型,与其旋光性(+)、(-)无关。当一个旋光性物质发生化学反应时,只要手性碳上的任何一个键都未断裂,则这个手性碳的构型就没有改变。这样,许多其他物质分子的构型都可以通过直接或间接的化学转变,与D型或L型甘油醛相联系,其条件是相当于甘油分子的手性碳上的每一个键,在转变过程中都不发生断裂。如果该物质与D型甘油醛相联系时,其分子的构型即为D型,如与L型甘油醛相关联时,它的分子构型则属于L型。用这种方法确定的构型是相对于标准物质——甘油醛而来的,所以叫做相对构型。
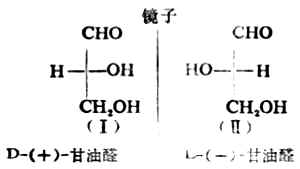
罗沙诺夫所作的上述规定为确定其他一些物质分子的构型带来方便,但这毕竟是人为规定的。直到1951年才有人证明D-(+)-甘油醛的真正构型与罗沙诺夫的规定是一致的。这样一来,无论是甘油醛还是与它们相关联的各旋光性物质的相对构型也都是绝对构型了。现在已有许多旋光性物质用不同的方法确定了绝对构型。关于D型和L型的概念目前在一些化合物如糖类及α氨基酸中仍然应用。
现在认为,构型与旋光性之间没有必然的联系。物质的旋光性仍须通过实验测定。
(三)、对映异构体的系统命名法
对映异构体的系统命名法即IUPAC命名法。这是根据物质分子的绝对构型或其费歇尔投影式来命名的,故无须与其他化合物联系比较。
含一个手性碳的分子C*abcd命名时,首先把手性碳所连的四个原子或原子团按照次序规定排列其优先顺序,如a>b>c>d其次,将此排列次序中排在最后的原子或原子团(即d)放在距观察者最远的地方。这时,其他三个原子或原子团就向着观察者(图17-8)。然后,再观察从最优先基a开始到b再到c的次序,如果是顺时针方向排列的(图17-8左),这个分子的构型即用“R”标示(R取自拉丁方Rectus,右);如果a→b→c是逆时针方向排列的(图17-8右),则此分子的构型用“S”标示(S取自拉丁方Sinister,左)。
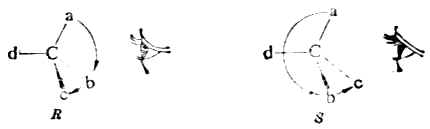
图17-8 R及S构型
例1.
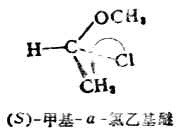
优先顺序
-CL>-OCH3>-CH3>-H
例2.
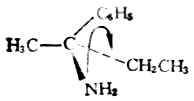
-NH2>C6H5>-C2H5>-CH8
用构型的费歇尔投影式,同样可以确定一个分子是R还是S构型。先要确定C*abcd中,a、b、c及d的优先顺序,如a>b>c>d。在费歇尔投影式中,如最小基d连在垂直方向,即C*-d键伸向纸平面的后方,则当a→b→c为顺时针方向时,此分子为R型;如a→b→c为逆时针方向时,则是S型。如最小基d连在水平方向,即C*-d键伸向纸平面的前方,则当a→b→c为顺时针方向时,此分子为S型;如a→b→c为逆时针方向时,为R型(图17-9)。
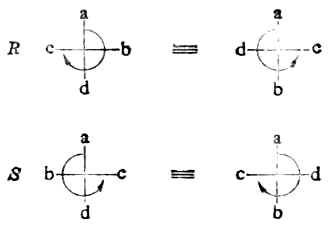
图17-9 用费歇尔投影式确定R/S构型
例1.
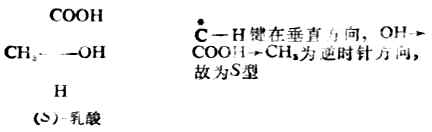
例2.
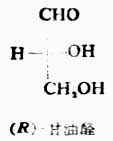
要把R/S构型与D/L构型分开,不能认为D型的分子即R型的,或L型的分子即S型的。例如:
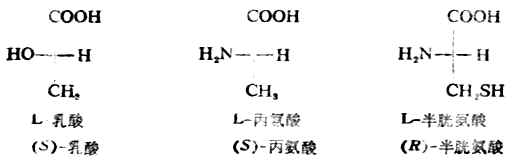
四、含两个手性碳原子的分子
在有机化合物中,随着手性碳原子数目的增加,对映异构现象也愈杂。
(一)含两个不同的手性碳原子的分子
这类分子中,两个手性碳不同,即一个手性碳上所连的四个原子或原子团与另一个手性 碳上所连的不同或不完全相同。这种分子有四种具有旋旋光性的异构体,例如,2-羟基-3-氯丁二酸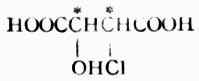 。它的C-2上连的
。它的C-2上连的
是-H,-OH,--COOH及-CHCLCOOH,C-3上连的是-H,CL,-COOH及-CHOHCOOH,这是两个不同的手性碳。它们的费歇尔投影式如下:
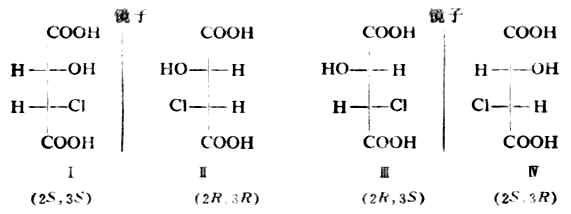
Ⅰ与Ⅱ是一对对映体,Ⅲ与Ⅳ是另一对对映体。Ⅰ(或Ⅱ)与Ⅲ(或Ⅳ)虽是具有旋光性的异构体,但并不是对映体,而是非对映异构体(非对映体)。非对映体之间不仅旋光性不同,理化性质也有一定的差异(表17-2)。
表17-2 2-羟基-3-氯丁二酸的一些物理性质
| 化合物构型 | 熔点/℃ | [α]20D |
| Ⅰ(2S,3S) | 173(±)146 | +31.3(乙酸乙酯) |
| Ⅱ(2R,3R) | 173 (±)146 | -31.3(乙酸乙酯) |
| Ⅲ(2R,3S) | 167 (±)153 | -9.4(水) |
| Ⅳ(2S,3R) | 167 (±)153 | +9.4(水) |
任何含两个不同的手性碳原子的分子都有四个立体异构体,即两对对映体。
含两个或两个以上手性碳的分子中,每个手性碳的构型都须用R/S标示,写在化合物名称之前,并标以该手性碳的位次。例如,Ⅰ为(2S,3S)-2-羟基-3-氯丁二酸。
(二)含两个相同的手性碳原子的分子
这类分子中,两个手性碳相同。例如,酒石酸的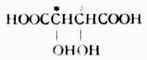
C-2与C-3都是手性碳,且各连有-H,-OH,-COOH及-CHOHCOOH,这是两个相同的手性碳原子。它们的费歇尔投影式如下:
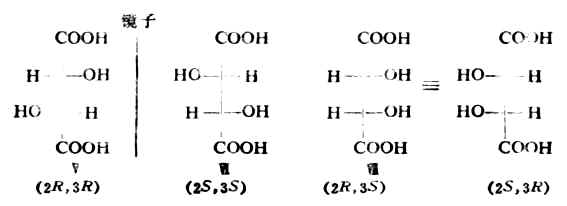
Ⅴ与Ⅵ是一对对映体。Ⅶ的两个费歇尔投影式是等同的。因为将任何一个在纸平面上旋转180°即得另一个。Ⅶ虽有两个手性碳原子,却不具旋光性。这是由于这个分子是对称的,它有一个对称面,即垂直于C(2)-C(3)键的平面。这种异构体叫做内消旋体,用meso-或i-表示。
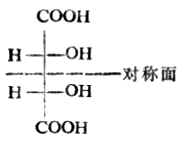
内消旋酒石酸与外消旋酒石酸虽然都不具旋光性,但它们有本质上的不同。内消旋体是纯物质,不能拆分;外消旋体则能拆分为左旋体及右旋体。内消旋体的性质与左旋体或右旋体也有差异(表17-3)。
表17-3 几种酒石酸的性质
| 酒石酸 | 熔点/℃ | [α]25D(水) | 溶解度/g·(100g水)-1 | 相对密度(20℃) | PKa1 | PKa2 |
| (+) | 170 | +12° | 147 | 1.760 | 2.93 | 4.23 |
| (-) | 170 | -12° | 147 | 1.760 | 2.93 | 4.23 |
| i- | 140 | 125 | 1.666 | 3.2 | 4.80 | |
| (±) | 205 | 24.6 | 1.687 | 2.96 | 4.24 |
含n个不同的手性碳原子的分子有2n个立体异构体,成为2n-1对对映体。
五、光学活性物质在医学上的意义
在生物体中存在的许多化合物都是手性的。例如,在生物体中普遍存在的α-氨基酸主要是L-型,从天然产物中得到的单糖多为D-型。生物体对某一物质的要求常严格地限定为某个单一的构型。所以与生物物质有关的合成物质,如果有旋旋光性的异构体,也往往只有其中之一具较强的生理效应,其对映体或是无活性或活性很小,有些甚至产生相反的生理作用。例如;作为血浆代用品的葡萄糖酐一定要用右旋糖酐,因为其左旋体会给病人带来较大的危害;右旋的维生素C具有抗坏血病作用,而其对映体无效。左旋肾上腺素的升高血压作用是右旋体的20倍;左旋氯霉素是抗生素,但右旋氯霉素几乎无抗生作用。
由于旋光性物质的左、右旋体还可能有不同类型的生理作用,所以在临床医学上有不同的应用。例如,右旋四咪唑为抗抑郁药,其左旋体则是治疗癌症的辅助药物;右旋苯丙胺是精神兴奋药,其左旋体则具抑制食欲作用。
临床医学还须考虑对映体之一的毒副作用。例如,(R)-(+)-反应停是镇静剂,用于各种麻疯反应,而其对映体(S)-(-)-反应停则有致畸作用。
第十八章 含氮有机化合物
含氮有机合物主要是指分子中氮原子和碳原子直接相连的化合物,也可看成是烃分子
表18-1 常见的含氮有机化合物
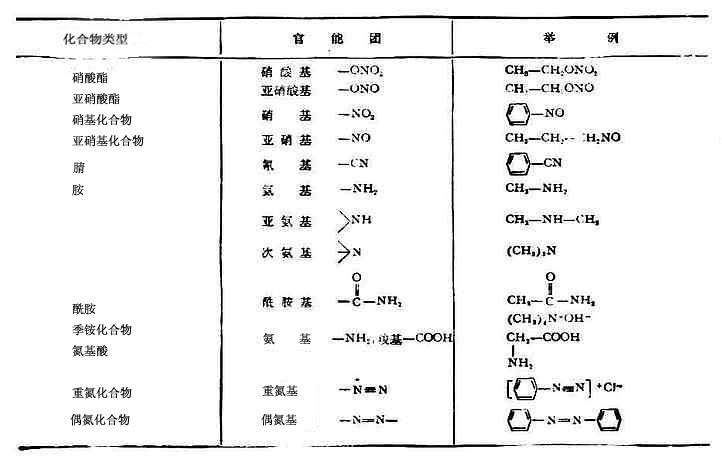
中的一个或几个氢原子被含氮的官能团所取代的衍生物。这类化合物范围广,种类繁多,与生命活动和人类日常生活关系非常密切。常见的比较简单的含氮有机化合物如表18-1。
含氮杂环化合物、生物碱也是为数众多的含氮有机化合物,将在第十九章中讨论。本章主要讨论胺、酰胺、氨基酸等。
第一节 胺类
胺类是比较重要的含氮有机化合物。例如苯胺是合成药物、染料等的重要原料;胆碱是调节脂肪代谢的物质,它的乙酰衍生物——乙酰胆碱是神经传导的递质;乙二胺是制造EDTA的原料等。
一、胺的构造、分类和命名
(一)胺的构造和分类
胺可以看作是氨(NH3)分子中的氢原子被烃基取代所生成的化合物。通式为RNH2,R2NH或R3N,其中R代表脂肪烃基或芳香烃基,它们分别属于伯、仲和叔胺。
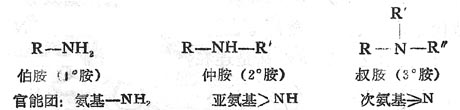
但要注意,这里的伯、仲、叔的含义与醇中的不同,它们分别是指氮原子上连有一个、两个或是三个烃基,而与连接氨基的碳是伯、仲还是叔碳原子没有关系。例如,叔丁醇是叔醇,而叔丁胺却是伯胺。
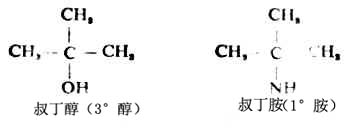
季胺化合物可看作是铵盐(NH4+X-)或氧氧化铵(NH4OH)分子中氮原子上的四个氢原子都被烃基取代生成的化合物,它们分别称为季铵盐和季铵碱。
仲、叔胺或季铵化合物分子中的烃基可以是相同的,也可以是不同的。
在这里,应注意“氨”、“胺”及“铵”的含义。在表示基(如氨基、亚氨基等)时,用“氨”;表示NH3的烃基衍生物时,用“胺”;而铵盐或季铵类化合物则用“铵”。
胺也可以根据NH3分子中的氢原子被不同种类的烃基取代而分为脂肪胺和芳香胺。氨基与脂肪烃基相连的是脂肪胺,与芳香环直接相连的叫芳香胺。
R-NH2Ar-NH2
脂肪胺 芳香胺
胺还可以根据分子中所含氨基数目的不同而分为一元胺、二元胺和多元胺。
(二)命名
1.普通命名法
这种方法是按照分子中烃基的名称及数目叫做“某胺”。
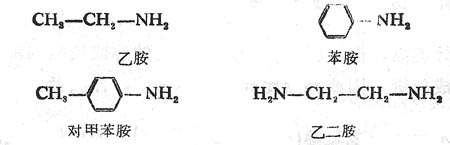
当胺分子中氮原子上所连的烃基不同时,则按次序规则列出,小者在前,“较优”者在后。
CH3-NH-C2H5
甲乙胺
若原子上连有两个或三个相同的烃基时,则须表示出烃基的数目。
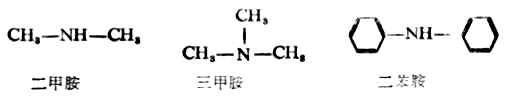
氮原子上同时连有芳香烃基和脂肪烃基的仲胺和叔胺的命名,则以芳香胺为母体,脂肪烃基作为芳胺氮原子上的取代基,将名称和数目写在前面,并在基前冠以“N”字(每个“N”只能指示一个取代基的位置),以表示这个脂肪烃基是连在氮原子上,而不是连在芳香环上。
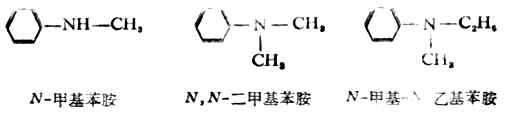
2.系统命名法
烃基比较复杂的胺,以烃为母体,将氨基作为取代基命名。
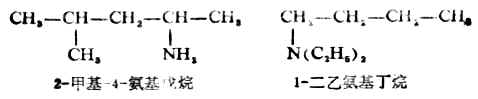
季铵化合物的命名与无机铵的命名相似。
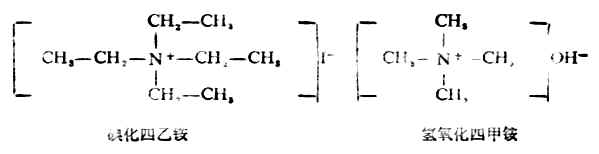
二、胺的性质
(一)物理性质
胺与氨的性质很相似。低级脂肪胺是气体或易挥发的液体,具有难闻的臭味。高级胺为固体。芳香胺为高沸点的液体或低熔点的固体,具有特殊气味,难溶于水,易溶于有机溶剂。芳香胺具有一定的毒性,如苯胺可以通过消化道、呼吸道或经皮肤吸收而引起中毒;联苯胺等有致癌作用。因此,在处理这些化合物时应加以注意。
同氨一样,胺是极性化合物。除叔胺外,都能形成分子间氢键
![]() 。胺的沸点比相对分子质量相近的烃类高,但比相对分子质量相近的醇或羧酸的沸点低。叔胺氮原子上无氢原子,分子间不能形成氢键,因此沸点比其异构体的伯、仲胺低。
。胺的沸点比相对分子质量相近的烃类高,但比相对分子质量相近的醇或羧酸的沸点低。叔胺氮原子上无氢原子,分子间不能形成氢键,因此沸点比其异构体的伯、仲胺低。
伯、仲、叔胺都能与水分子形成氢键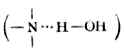 ,因此低级的胺
,因此低级的胺
易溶于水。胺的溶解度随相对分子质量的增加而迅速降低,从6个碳原子的胺开始就难溶于水。一般胺能溶于醚、醇、苯等有机溶剂。
(二)化学性质
1.胺的碱性和成盐反应
胺中的氮原子和氨中一样,有一对未共用电子对。能接受质子,因此胺具有碱性。
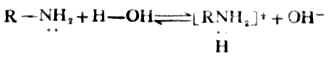
胺的碱性以碱式离解常数Kb或其负对数pKb值表示。Kb值愈大或pKb值愈小则碱性愈强;Kb值愈小或pKb值愈大则碱性愈弱。胺的碱性也可用其共轭酸铵离子的离解常数Ka或pKa来表示。Ka值愈小或pKa值愈大,则胺的碱性愈强。
在水溶液中,脂肪胺一般以仲胺的碱性最强。但是,无论伯、仲或叔胺,其碱性都比氨强。芳香胺的碱性则比氨弱。氨、甲胺、二甲胺、三甲胺和苯胺的碱性强弱次序为:
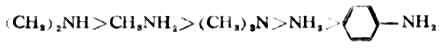
(1)脂肪胺的碱性 影响脂肪胺碱性的因素有三个。①诱导效应——胺分子中与氮原子相连的烷基具有斥电子诱导效应(+I,![]()
,使氮上的电子云密度增加,从而增强了对质子的吸引能力,而生成的铵离子也因正电荷得到分散而比较稳定。因此,氮上烷基数增多,碱性要增强。②水化作用——在水溶液中,胺的碱性还决定于与质子结合后形成的铵离子水化的难易。氮原子上所连的氢愈多,则与水形成氢键的机会就愈多,水化程度亦愈大,铵离子就更稳定,胺的碱性也就增强。③位阻效应——胺分子中的烷基愈多、愈大,则占据空间的位置就愈大,使质子不易靠近氮原子,因而胺的碱性就降低。
因此,脂肪伯、仲、叔胺碱性的强弱是上述三个因素共同影响的结果。
(2)芳香胺的碱性 芳香胺的碱性比脂肪胺弱得多。例如苯胺的pKb=9.40,这是因为苯胺中氮原子的未共用电子对与苯环的π电子相互作用,形成一个均匀的共轭体系而变得稳定,氮原子上的电子云部分地转向苯环,因此氮原子与质子的结合能力降低,故苯胺的碱性比氨弱得多。
芳香胺氮原子上所连的苯环愈多,共轭程度愈大,碱性也就愈弱。?
■[此处缺少一些内容]■
季铵盐是有机化合物中的强碱。它们在固态时即是离子状态,例如(CH3)4N+O-H易溶于水,其碱性与氢氧化钠或氢氧化钾相当。
季铵盐和铵盐不同,前者是强碱的盐,与氢氧化钠等不发生反应。卤化季铵盐的水溶液用氧化银处理时则生成季铵碱。
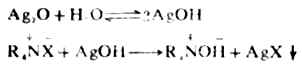
2.酯化反应
伯、仲胺都能与酰化剂(如乙酰氯、乙酸酐)作用,氨基上的氧原子被酰基取代,生成酰胺,这种反应叫做胺的酰化。叔胺因氮上没有氢,故不发生酰化反应。
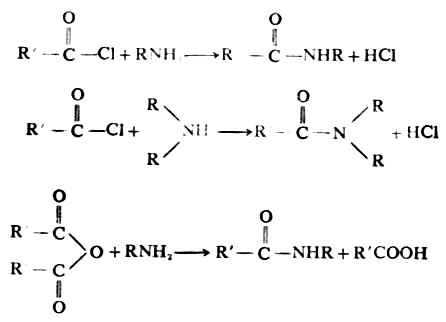
酰胺是晶形很好的固体,有一定的熔点,所以利用酰化反应可以鉴定伯胺和仲胺。叔胺不起酰化反应,故此性质可用来区别叔胺,并可以从伯、仲、叔胺的混合物中把叔胺分离出来。此外,酰胺在酸或碱的催化下,可水解游离出原来的胺。由于氨基活泼,且易被氧化,因此在有机合成中可以用酰化的方法来保护芳胺的氨基。例如:
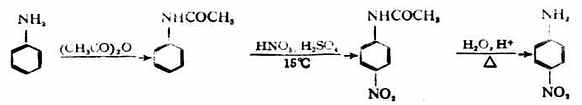
3.与亚硝酸反应
伯、仲、叔胺与亚硝酸反应时,产物各不相同,借此可区别三种胺。
由于亚硝酸(HNO2)是一种很不稳定的酸,所以通常用亚硝酸钠和强酸作用产生。
NaNO2+HCl→HNO2+NaCl
(1)伯胺与亚硝酸反应脂肪伯胺与亚硝酸反应,放出氮气,并生成醇、烯烃等的混合物。其反应式可简单地用下式表示:
R-NH2+HONO→ROH+N2↑+H2O
CH3-NH2+HONO→CH3OH+N2↑+H2O
由于此反应能定量地放出氮气,故可用于伯胺及氨基化合物的分析。
芳香族伯胺与脂肪伯胺不同,在低温和强酸存在下,与亚硝酸作用则生成芳香族重氮盐,这个反应称为重氮化反应。例如:
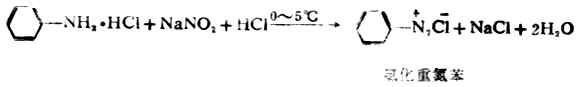
芳香重氮盐比脂肪重氮盐稳定,如在5℃以下,氯化重氮苯在水溶液中不会分解但温度升高,使分解放出氮气,同时生成酚类化合物。
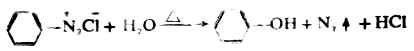
芳香重氮盐化学性质很活泼,是有机合成的重要中间体。例如,通过重氮盐的反应,可以制备许多芳香族化合物。芳香重氮盐的反应主要分为放氮反应和偶合反应两大类。
放氮反应:重氮基(![]() )在不同条件下,可被羟基、卤素、氰
)在不同条件下,可被羟基、卤素、氰
基、氢原子等取代,生成相应的芳香族衍生物,放出氮气。因此,利用这些反应可以从芳香烃开始合成一系列芳香族化合物。
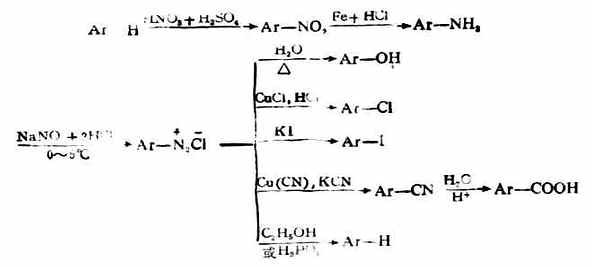
偶合反应:重氮盐与酚类或芳香叔胺作用,生成有颜色的偶氮化合物,这个反应称为偶合反应。
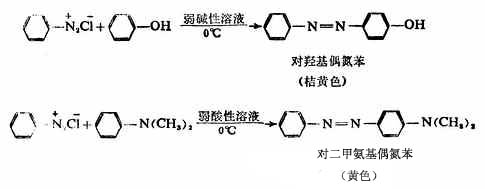
重氮盐与酚或芳香胺偶合时,如果羟基或氨基的对位有其它原子或原子团,则可在邻位偶合;如果对位及邻位都有取代基时,则不发生反应。
偶氮化合物都有颜色。许多偶氮化合物可用作染料,称为偶氮染料,有些偶氮化合物的颜色能随溶液PH值的不同而变化,这些化合物可用作酸碱指示剂。例如甲基橙。
(2)仲胺与亚硝酸反应脂肪仲胺和芳香族仲胺与亚硝酸作用生成N-亚硝基胺。
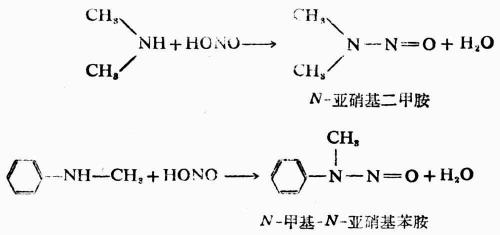
N-亚硝基胺为黄色的中性油状物质,不溶于水,可从溶液中分离出来;与稀酸共热则分解为原来的仲胺,故可利用此性质鉴别、分离或提纯仲胺。
N-亚硝基胺是较强的致癌物质。
(3)叔胺与亚硝酸反应脂肪叔胺因氮上没有氢,与亚硝酸作用时只能生成不稳定的亚硝酸盐。

芳香族叔胺与亚硝酸作用,发生环上取代反应,在芳香环上引入亚硝基,生成对亚硝基取代物,在酸性溶液中呈黄色,若对位上已有取代基,则亚硝基取代在邻位。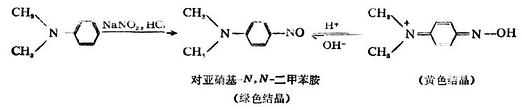
由于三种胺与亚硝酸的反应不同,所以可利用与亚硝酸的反应鉴别伯、仲、叔胺。
三、重要的胺及其衍生物
(一)苯胺
苯胺是最简单也是最重要的芳香伯胺,是合成药物,染料等的重要原料。苯胺为油状液体,沸点184℃,微溶于水,易溶于有机溶剂。新蒸馏的苯胺无色,但久置会因氧化而颜色变深。苯胺有毒,能透过皮肤或吸入蒸气使人中毒。因此,接触苯胺时应加注意。
(二)胆碱
胆碱[(CH3)3N+CH2CH2OH]OH-是一种季铵碱,广泛存在于生物体中,在脑组织和蛋黄中含量较多,是卵磷脂(见第二十章)的组成部分。胆碱为白色结晶,吸湿性强,易溶于水和乙醇,而不溶于乙醚和氯仿等。它在体内参与脂肪代谢,有抗脂肪肝的作用。
胆碱分子中醇羟基的氢原子被乙酰基取代所生成的酯叫做乙酰胆碱[CH3COOCH2CH2N+(CH3)3]OH-,是神经传导的递质。
(三)新洁尔灭
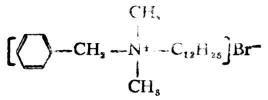
新洁尔灭(溴化二甲基十二烷基苄基铵)
在常温下,新洁尔灭为微黄色的粘稠液,吸湿性强,易溶于水和醇。水溶液呈碱性。新洁尔灭是具有长链烷基的季铵盐,属阳离子型表面活性剂,也是消毒剂。临床上上用于皮肤、器皿及手术前的消毒。
第二节 酰胺
一、酰胺的构造和命名
酰胺是羧酸的衍生物。在构造上,酰胺可看作是羧酸分子中羧基中的羟基被氨基或烃氨基(-NHR或-NR2)取代而成的化合物;也可看作是氨或胺分子中氮原子上的氢被酰基(![]() )取代而成的化合物。
)取代而成的化合物。
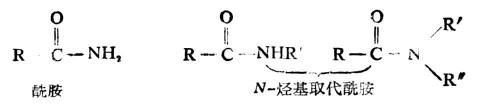
酰胺的命名是根据相应的酰基名称,并在后面加上“胺”或“某胺”,称为“某酰胺”或“某酰某胺”。例如:
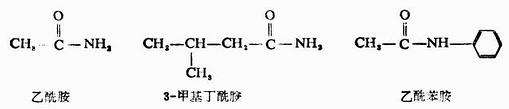
当酰胺中氮上连有烃基时,可将烃基的名称写在酰基名称的前面,并在烃基名称前加上“N-”“N,N-”,表示该烃基是与氮原子相连的。
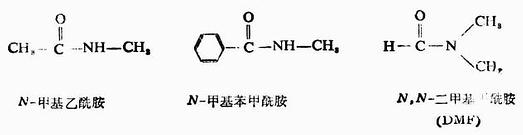
二、酰胺的性质
(一)物理性质
在常温下,除甲酰胺是液体外,其它酰胺多为无色晶体。酰胺分子中含有羰基和氨基,它们分子间能形成氢键。由于酰胺分子间氢键缔合能力较强,因此其熔点、沸点甚至比相对分子质量相近的羧酸还高。
当酰胺中氮原子上的氢被烷基取代后,缔合程度减小,熔点和沸点则降低。脂肪族N-烷基取代酰胺一般为液体。
低给酰胺易溶于水,随着相对分子质量的增大,溶解度逐渐减小。液体酰胺不但可以溶解有机物,而且也可以溶解许多无机物,是良好的溶剂。例如HCON(CH3)2。
(二)化学性质
1.酸碱性
酰胺一般是近中性的化合物,但在一定条件下可表现出弱酸或弱碱性。酰胺是氨或胺的酰基衍生物,分子中有氨基或烃氨基,但其碱性比氨或胺要弱得多。酰胺碱性很弱,是由于分子中氨基氮上的未共用电子对与羰基的π电子形成共轭体系,使氮上的电子云密度降低,因而接受质子的能力减弱。这时C-N键出现一定程度的双键性。
然而,氮上的电子云密度降低,却使N-H键的极性增加,从而表现出微弱的酸性。如果氨分子中有两个氢原子被一个二元酸的酰基取代,则生成环状的亚氨基化合物(酰亚胺)。由于两个羰基的吸电子作用,使亚氨基的N-H键极性明显增加,氮上的氢原子较易变为质子,而呈弱酸性。例如:
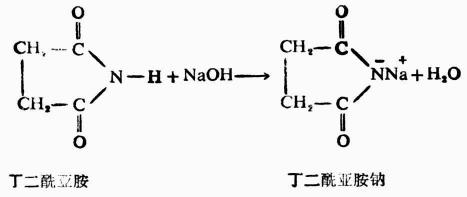
2.水解
酰胺在通常情况下较难水解。在酸或碱的存在下加热时,则可加速反应,但比羧酸酯的水解慢得多。
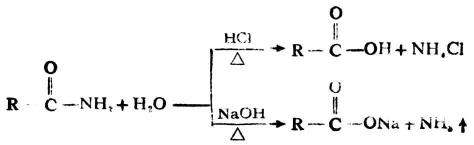
N-取代酰胺同样可以进行水解,生成羧酸和胺。
3.与亚硝酸反应
酰胺与亚硝酸作用生成相应的羧酸,并放出氮气。
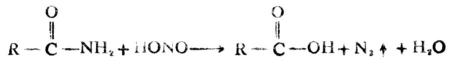
三、重要的酰胺及其衍生物
(一)尿素
尿素又称脲,是碳酸的二酰胺。
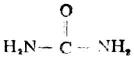
尿素是哺乳动物体内蛋白质代谢的最终产物,存在于动物的尿中。许多含氮化合物在代谢过程中所释放的氨是有毒的,通过转变为尿素从尿中排出而使氨的浓度降低。正常成人每天排泄的尿中约含尿素30g。
尿素为无色晶体,熔点133℃,易溶于水和乙醇,难溶于乙醚。
尿素是很重要的物质,用途广泛。它在农业上用作高效固体氮肥,也是有机合成的重要原料。用于合成药物、塑料等。尿素本身也是药物,对降低脑颅内压和眼内压有显著疗效。
尿素具有酰胺的结构,有酰胺的一般化学性质。但因两个氨基连在一个羰基上,所以它又表现出某些特殊的性质。
1.弱碱性
尿素分子中有两个氨基,其中一个氨基可与强酸成盐,故呈弱碱性。
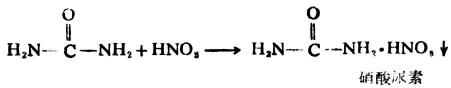
尿素的硝酸盐、草酸盐均难溶于水而易结晶。利用这种性质,可从尿液中提取尿素。
2.水解反应
尿素是酰胺类化合物,在酸、碱或尿素酶的作用下很易水解。
3.缩二脲的生成及缩二脲反应
尿素是一种特殊的酰胺,它的两个氨基连在同一个羰基上,所以它又有与一般酰胺不同的性质。若将尿素加热到稍高于它的熔点时,则发生双分子缩合,两分子尿素脱去一分子氨而生成缩二脲。
![]()
缩二脲是无色针状晶体,熔点190℃,难溶于水,能溶于碱液中。它在碱性溶液中与少量的硫酸铜(CuSO4)溶液作用,即显紫红色,这个颜色反应叫做缩二脲反应。凡分子中含有两个或两上以上酰胺键(![]()
,肽键)合
物如多肽、蛋白质等都能发生这种颜色反应。
(二)丙二酰脲
尿素与酰氯、酸酐或酯作用,则生成相应的酰脲。例如,尿素与丙二酰氯反应生成丙二酰脲。
丙二酰脲是无色晶体,熔点245℃,微溶于水。它的分子中含有
及 的结构,可发生酮式-烯醇式互变异构:
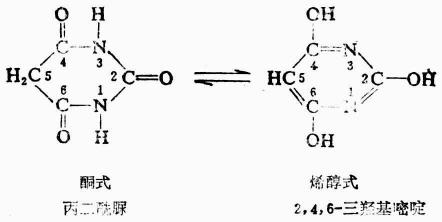
由于丙二酰脲中由酮式转变为烯醇式而呈酸性,所以丙二酰脲又称巴比土酸。
巴比土酸本身没有药理作用,但它的C-5亚甲基上的两个氢原子都被烃基取代(5,5-二取代)后所得许多取代物,却是一类重要的镇静催眠药,总称为巴比妥类药物。其通式为:
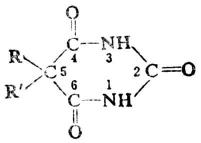
巴比妥类药物很多,主要的有巴比妥、苯巴比妥(鲁米那)、戊巴比妥、异戊巴比妥等。它们是晶体或结晶性粉末,难溶于水,能溶于一般有机溶剂中。
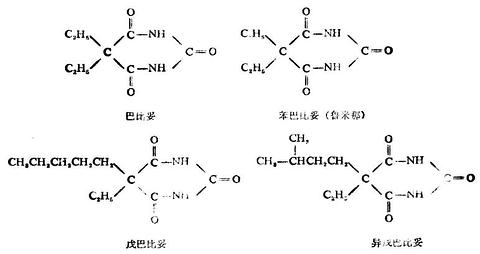
巴比妥类催眠药的钠盐,可作注射用。
(三)磺胺类及氯胺类药物
烃分子中的氢原子被磺基(-SO3H)取代而成的化合物叫磺酸。芳香磺酸最为重要,例如苯磺酸。
![]()
磺酸的化学性质与羧酸类似,但酸性比羧酸强得多。
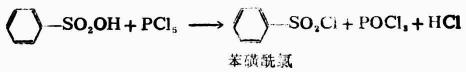
苯磺酰氯与氨或胺作用,可生成磺酰胺。
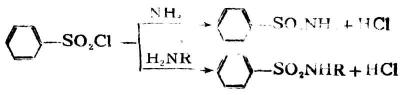
在医药上,重要的磺酰胺类化合物有磺胺类药物及氯胺类药物。
1.磺胺类药物
磺胺类药物是优良的化学治疗剂,开始应用于20世纪30年代。它们能抑制多种细菌,如链球菌、葡萄球菌、肺炎球菌、脑膜炎球菌、痢疾杆菌等的生长和繁殖,因此常用以治疗由上述细菌所引起的疾病。
最简单的磺胺类药物是对氨基苯磺酰胺,简称磺胺(SN)。
![]()
磺胺是无色晶体,熔点163℃,味微苦,微溶于水。磺胺能溶于强酸或强碱溶液中,这是由于它在苯环上连有氨基,因此能与酸作用生成盐;同时。与磺胺基结合的氨基上的氢原子,因受磺酰基的影响而呈酸性,故又能与碱作用。
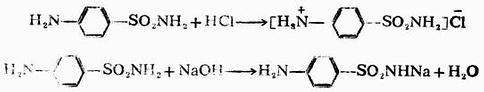
磺胺口服时副作用很大,仅外用以治疗化脓性创伤。为了减少磺胺的副作用,一般采用其它原子团取代磺酰氨基上的氢原子 ,其副作用较小,称为磺胺类药物。
,其副作用较小,称为磺胺类药物。
磺胺类药物的抗菌谱广,性质稳定,口服吸收良好,使用方便。表18-2是一些常见的磺胺类药物。
甲氧芐氨嘧啶(TMP),在化学结构上不属于磺胺类,但它能加强磺胺药的作用,也能增强多种抗生素的疗效,称为磺胺增效剂,常与磺胺类药物或抗生素伍用。
甲氧苄氨嘧啶(TMP)
表18-2 常见的磺胺类药物
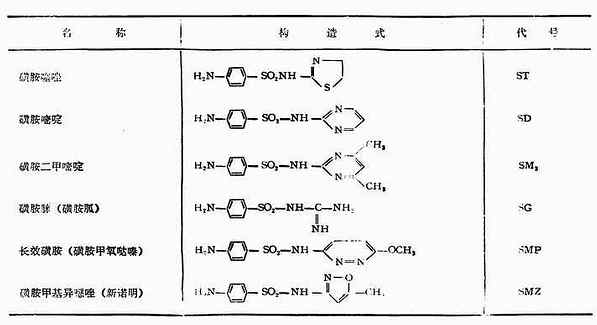
2.氯胺类药物
苯磺酰胺分子中,氨基的氢原子被氯原子取代的化合物叫做氯胺类药物。例如:
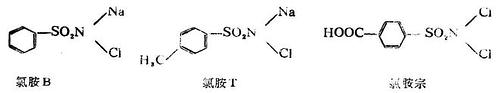
氯胺类药物是白色或黄色结晶性粉末,微具氯气味。能溶于水及乙醇,难溶于乙醚等有机溶剂。
氯胺类药物都是氧化剂,它们与水反应生成次氯酸或次氯酸钠,而有杀菌和对化学毒剂的消毒作用,故在军事医学上有重要意义。
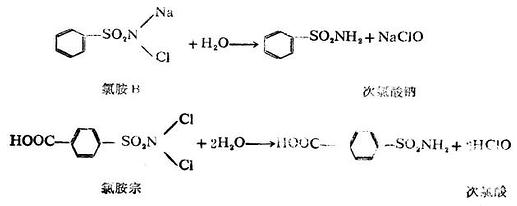
第三节 氨基酸
氨基酸是一类具有特殊重要意义的化合物。因为它们中许多是与生命活动密切相关的蛋白质的基本组成单位,是人体必不可少的物质,有些则直接用作药物。
α-氨基酸是蛋白质的基本组成单位。蛋白质在酸、碱或酶的作用下,能逐步水解成比较简单的分子,最终产物是各种不同的α-氨基酸。水解过程可表示如下:
蛋白质→月示→胨→多肽→二肽→α-氨基酸
由蛋白质水解所得到的α-氨基酸共有20多种,各种蛋白质中所含氨基酸的种类和数量都各不相同。有些氨基酸在人体内不能合成,只能依靠食物供给,这种氨基酸叫做必需氨基酸(见表18-3,*)。
一、氨基酸的构造、构型及分类、命名
(一)氨基酸的构造和构型
分子中含有氨基和羧基的化合物,叫做氨基酸。
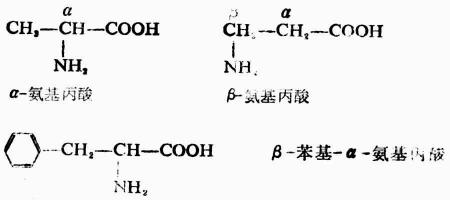
由蛋白质水解所得到的α-氨基酸,可用通式表示如下:
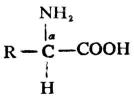
除甘氨酸(R=H)外,所有α-氨基酸中的α碳原子均是手性碳,故有D型与L型两种构型。天然氨基酸均为L-氨基酸。
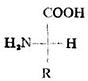
L-氨基酸
(二)α-氨基酸的分类和命名
氨基酸有脂肪族氨基酸、芳香族氨基酸和杂环氨基酸。
在α-氨基酸分子中可以含多个氨基和多个羧基,而且氨基和羧基的数目不一定相等。因此,天然存在的α-氨基酸常根据其分子中所含氨基和羧基的数目分为中性氨基酸、碱性氨基酸和酸性氨基酸。所谓中性氨基酸是指分子中氨基和羧基的数目相等的一类氨基酸。但氨基的碱性和羧基的酸性不是完全相当的,所以它们并不是真正中性的物质,只能说它们近乎中性。分子中氨基的数目多于羧基时呈现碱性,称为碱性氨基酸;反之,氨基的数目少于羧基时呈现酸性,称为酸性氨基酸。
氨基酸的系统命名方法与羟基酸一样,但天然氨基酸常根据其来源或性质多用俗名。例如胱氨酸是因它最先来自尿结石;甘氨酸是由于它具有甜味而得名(见表18-3)。
表18-3 常见的α-氨基酸
| 氨 基 酸 | 构 造 式 | 代号 | 常用符号 | pI |
| 甘氨酸(α-氨基乙酸) | 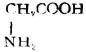 |
甘 | Giy | 5.97 |
| 丙氨酸(α-氨基丙酸) | 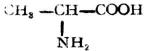 |
丙 | Ala | 6.02 |
| 缬氨酸(β-甲基-α-氨基丁酸) | 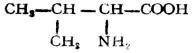 |
缬 | Val | 5.96 |
| 亮氨酸(γ-甲基-α-氨基戊酸) | 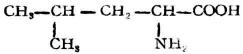 |
亮 | Len | 5.98 |
| 异亮氨酸(β-甲基-α-氨基戊酸) | 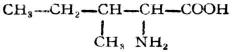 |
异 | Lle | 6.02 |
| 脯氨酸(α-羧基四氢吡咯) | 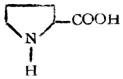 |
脯 | Pro | 6.30 |
| 苯丙氨酸(β-苯基-α-氨基丙酸) | 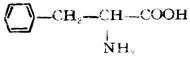 |
苯 | Phe | 5.48 |
| 色氨酸[α-氨基-β-(3-吲哚基)丙酸] | 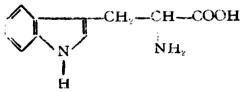 |
色 | Try (Trp) | 5.89 |
| 蛋氨酸(α-氨基-γ-甲硫基丁酸) | 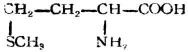 |
蛋 | Met | 5.74 |
| 丝氨酸(α-氨酸-β-羟基西丙酸) | 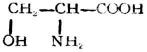 |
丝 | Ser | 5.68 |
| 苏氨酸(α-氨基-β-羟基丁酸) | 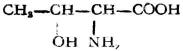 |
苏 | Thr | 6.18 |
| 半胱氨酸(α-氨基-β-巯基丙酸) | 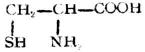 |
半 | Cys | 5.07 |
| 酪氨酸[α-氨基-β-(对羟苯基)丙酸] | 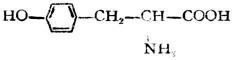 |
酪 | Tyr | 5.66 |
| 天门冬酰胺(α-氨基丁酰胺酸) | 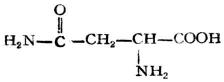 |
天酰 | Asn | 5.41 |
| 谷氨酰胺(α-氨基戊酰胺酸) | 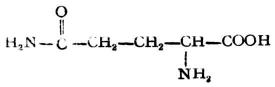 |
谷酰 | Gln | 5.65 |
| 天门冬氨酸(α-氨基丁二酸) | 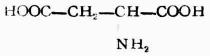 |
天 | Asp | 2.77 |
| 谷氨酸(α-氨基戊二酸) | 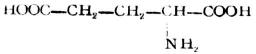 |
谷 | Glu | 3.22 |
| 赖氨酸(α,ε-二氨基已酸) | 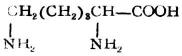 |
赖 | Lys | 9.74 |
| 组氨酸[(α-氨基-β-(4-噗唑基)丙酸] | 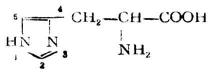 |
组 | His | 7.59 |
| 傅氨酸(α-氨基,δ-胍基戊酸) | 精 | Arg | 10.76 |
二、氨基酸的性质
α-氨基酸都是无色晶体,熔点一般都较高(常在230-300℃之间),熔融时即分解放出二氧化碳。
α-氨基酸都能溶于酸性或碱性溶液中,但难溶于乙醚等有机溶剂。在纯水中各种氨基酸的溶解度差异较大,加乙醇能使许多氨基酸从水溶液中沉淀析出。
(二)化学性质
氨基酸分子内既含有氨基又含有羧基,因此它们具有氨基和羧基的典型性质。但是,由于两种官能团在分子内的相互影响,又具有一些特殊的性质。
1.两性
氨基酸分子中既有碱性-NH2和酸性-COOH,与强酸或强碱都能作用生成盐,因此氨基酸为两性化合物。
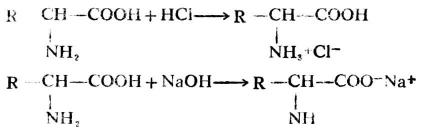
同时,在同一分子内,氨基和羧基也可作用生成盐,这种盐叫内盐。
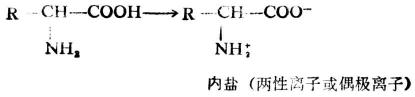
氨基酸在纯水溶液及固态时都以内盐的形式存在。在一般情况下,氨基酸中羧基的电离程度和氨基的电离程度并不相等。因此纯净氨基酸的水溶液并不一定是中性。在中性氨基酸溶液中,由于羧基的电离程度稍大于氨基的电离度,故它的水溶液的PH值一般略小于7。酸性氨基酸水溶液的PH值小于7;碱性氨基酸水溶液的PH值则大于7。但须注意,无论是何种α-氨基酸,其水溶液中两性离子都占绝对多数。
2.等电点
若将氨基酸的水溶液酸化,则两性离子与H+结合而成阳离子,若加碱于氨基酸的水溶液中,则两性离子中氮原子上的一个氢离子与OH-结合成水,而两性离子变成阴离子。
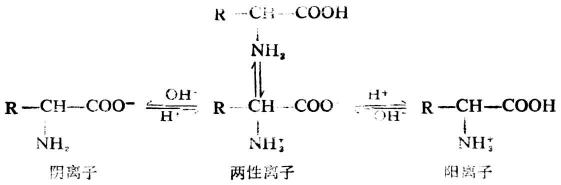
若将氨基酸水溶液的酸碱度加以适当调节,可使羧基与氨基的电离程度相等,也就是氨基酸带有正、负电荷数目恰好相同,此时溶液的PH值称为该氨基酸的等电点,以PI表示。由于各种氨基酸分子中所含基团不同,所以每一个氨基酸中氨基和羧基的电离程度各异,因此不同的氨基酸等电点亦不同(表18-3)。中性氨基酸的等电点一般在5.0-6.5之间;酸性氨基酸为2.7-3.2,碱性氨基酸为9.5-10.7。
如果在不同的PH值的氨基酸溶液中通以直流电,当PH>PI(到一定程度)时,由于氨基酸主要以阴离子存在,它们就向阳极移动;若PH<PI(到一定程度)时,因氨基酸主要以阳离子存在,则它们就向阳极移动;如果PH=PI,则不发生电泳,因为这时的氨基酸主要以两性离子存在,其净电荷为零,故在电场中不会向任何一极移动。所以,电泳是可以用来分离子或鉴定氨基酸、蛋白质等的混合物的一种技术,也可作为医学诊断的手段。
3.脱水生成肽
两分子α-氨基酸(相同或不同)可借一个分子中的羧基和另一分子中的氨基脱去一分子水,缩合成为一个简单的肽,即二肽。
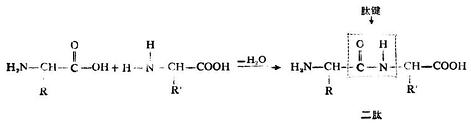
二肽分子中含有的酰胺键
叫做肽键。二肽分子中的末其端
仍含有自由的氨基和羧基,因此还可以继续与氨基酸缩合成为三肽、四肽以至多肽。
多肽
多肽类物质在天然界中存在很多,它们在生物体中起着各种不同的作用。例如,存在于大部分细胞中的谷胱甘肽(三肽),参与细胞的氧化还原过程。
4.脱羧作用
某些氨基酸在一定条件下,可脱去羧基,生成相应的胺。
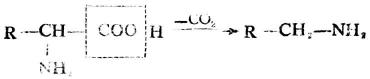
脱羧反应是人体内氨基酸代谢的形式之一,例如在肠道细菌作用下,组氨酸可脱羧生成组胺。
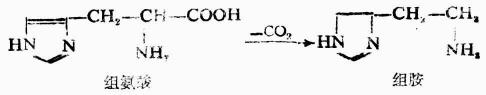
脱羧反应也可在蛋白质腐败时发生。例如在某些细菌作用下,蛋白质中的赖氨酸可变成毒性很强的尸胺(戊二胺)。
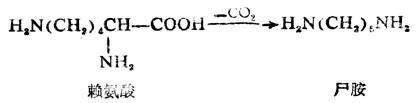
5.与亚硝酸的反应
氨基酸中的氨基具有伯胺的性质,与亚硝酸作用时生成羟基酸,同时定量的放出氮气。
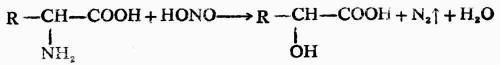
6.与茚三酮的显色反应
α-氨基酸与茚三酮的水合物在水溶液中加热时,生成蓝紫色或紫色化合物,同时产生醛、二氧化碳和氨。这个反应非常灵敏,是鉴定氨基酸最迅速、最简单的方法,常用于α-氨基酸的比色测定或纸层析、薄层层析时的显色。
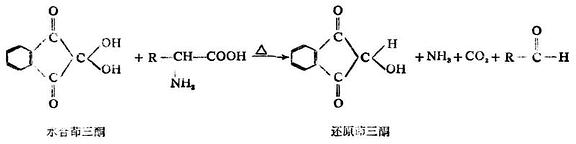
多肽和蛋白质也有此显色反应。
第十九章 杂环化合物和生物碱
杂环化合物在自然界分布很广,其数量几乎占已知有机化合物的三分之一,用途也很多。许多重要的物质如叶绿素、血红素、核酸以及临床应用的一些有显着疗效的天然药物和合成药物等,都含有杂环化合物的结构。生物碱多是中草药的有效成分,绝大多数是含氮的杂环化合物。本章内容与医学关系密切,具有重要意义。
第一节 杂环化合物
在环状有机化合物中,组成环的原子除碳原子外,还有其它非碳原子时,这类化合物称为杂环化合物。这些非碳原子叫做杂原子,常见的杂原子有氮、氧、硫。
根据以上定义,杂环化合物似乎应包括内酯、交酯和环状酸酐等,但由于它们与相应的开链化合物性质相似,又容易开环变成开链化合物,所以不包括在杂环化合物之内。本章主要讨论那些环系比较稳定,并且有不同程度芳香性的杂环化合物。所谓芳杂环化合物是保留芳香结构即6π电子闭合共轭体系的杂环。这类化合物比较稳定,不易开环,而且它们的结构和反应活性与苯有相似之处,即有不同程度的芳香性,所以称为芳杂环化合物。
一、杂环化合物的分类和命名
杂环化合物可按杂环的骨架分为单杂环和稠杂环。单杂环又按环的大小分为五元杂环和六元杂环;稠杂环按其稠合环形式分为苯稠杂环和稠杂环。如表19-1所示。
杂环化合物的命名主要采用外文译音法,把杂环化合物的英文名称的汉字译音加“口”字旁表示。例如:

呋喃(furan) 吡啶(pyridine)
外文译音法是根据国际通用名称译音的,使用方便,缺点是名称和结构之间没有任何联系。
杂环化合物的环上原子编号,除个别稠杂环如异喹啉外,一般从杂原子开始。
环上只有一个杂原子时,杂原子的编号为1。有时也以希腊字母α、β及γ编号,邻近杂原子的碳原子为α位,其次为β位,再次为γ位。
当杂环上连有-R,-X,-OH,-NH2等取代基时,以杂环为母体,标明取代基位次;如果连有-CHO,-COOH,-SO3H等时,则把杂环作为取代基。环上有两个或两个以上相同杂原子时,应从连接有氢或取代基的杂原子开始编号,并使这些杂原子所在位次的数字之和为最小。环上有不同杂原子时,则按氧、硫、氮为序编号。例如:
表19-1 常用杂环化合物的构造式和名称
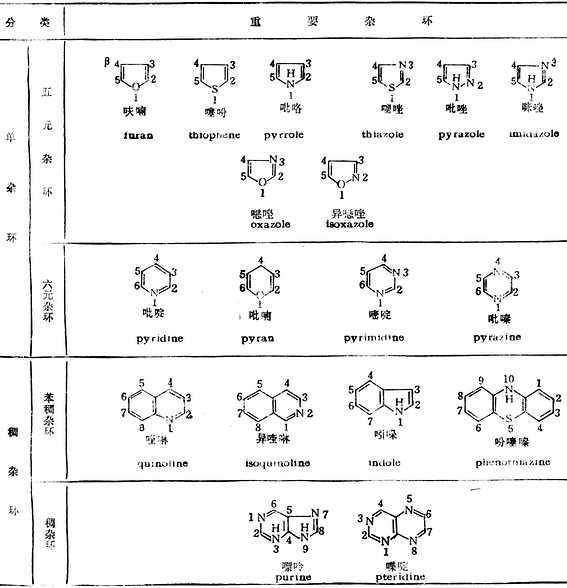
另有特殊编号的,如嘌呤等(见表19-1)。
二、杂环化合物的结构
五元杂环化合物呋喃、噻吩、吡咯的结构和苯相类似。构成环的四个碳原子和杂原子(N,S,O)均为sp2杂化状态,它们以σ键相连形成一个环面。每个碳原子余下的一个p轨道有一个电子,杂原子(N,S,O)的p轨道上有一对未共享电子对。这五个p轨道都垂直于五元环的平面,相互平行重叠,构成一个闭合共轭体系,即组成杂环的原子都在同一平面内,而p电子云则分布在环平面的上下方,如图19-1所示。
图19-1 呋喃、噻吩和苯的分子结构
从上图可看出呋喃、噻吩、吡咯的结构和苯结构相似,都是6电子闭合共轭体系,因此,它们都具有一定的芳香性,即不易氧化,不易进行加成反应,而易起亲电取代反应。由于共轭体系中的6个π电子分散在5个原子上,使整个环的π电子云密度较苯大,比苯容易发生亲电取代。同时,α位上的电子云密度较大,因而亲电取代反应一般发生在此位置上,如果α位已有取代基,则发生在β位。
与苯比较,环的芳香稳定性不如苯环,电子云密度分布也不完全平均化。由于杂原子电负性大小不同(O>N>S),电子云离域有差异,所以它们的芳香性强弱有差异,环的稳定性也不同。
含有两个杂原子(其中至少有一个氮原子)的五元杂环称为唑。常见的有咪唑、吡唑和噻唑。

咪唑、吡唑、噻唑的电子结构与上述几个环系类似,同样具有闭合的6个电子共轭体系,所以这些杂环也都具有一定的芳香性。例如,咪唑可以看作是吡咯环上氮原子的间位“-CH=”被“-N=”取代的衍生物。这个“-N=”的氮原子上未共用电子对参与环的共轭体系,可与质子结合并保持闭合的6电子共轭体系,所以咪唑也有芳香性,并且显弱碱性(ψKb=6.9)。
六元杂环的结构可以吡啶为例来说明。吡啶在结构上可看作是苯环中的-CH=被-NH=取代而成。5个碳原子和一个氮原子都是sp2杂化状态,处于同一平面上,相互以σ键连接成环状结构。每一个原子各有一个电子在p轨道上,p轨道与环平面垂直,彼此“肩并肩”重叠形成一个包括6个原子在内的,与苯相似的闭合共轭体系。氮原子上的一对未共用电子对,占据在sp2杂化轨道上,它与环平面共平面,因而不参与环的共轭体系,不是6电子大π键体系的组成部分,而是以未共用电子对形式存在,如图19-2所示。
图19-2吡啶分子结构
吡啶分子中的C-C键长(0.139-0.140nm)与苯分子中的C-C键长(0.140nm)相似;C-N键长(0.134nm)较一般的C-N键长(0.147nm)短,但比一般的C=N双键(0.128nm)长。这说明吡啶的键长平均化程度较高,但并不像苯一样是完全平均化的。所以吡啶具有芳香性。然而又由于吡啶环中氮原子的电负性大于碳原子,所以环上的最子云密度因向氮原子转移而降低,亲电取代比苯难。此环上氮原子具有与间位定位基-NO2相仿的电子效应,钝化作用使亲电性取代较苯困难,取代基进入间位,且收率偏低。
吡啶环上的氮原子有一对未共用电子对参与6电子共轭体系,可与质子结合,故其碱性(PKb=8.8)较吡咯(pKb=13.6)强,也比苯胺(pKb=9.3)强,能与强酸作用生成较稳定的盐。但比氨(pKb=4.75)弱,也比脂肪叔胺(三甲胺的pKb=4.22)弱。原因在于吡啶环上未参与共轭体系的这一对未共用电子对处于sp2杂化轨道上,其s成分较sp3杂化轨道多,受原子核束缚强,因而较难与H+结合。
吡啶与水能以任意比例混溶,同时又能溶解大多数极性及非极性有机化合物,它是一个良好的溶剂。吡啶具有高水溶性的原因,除分子极性外,是由于其氮原子上一对未参与环共轭体系的未共用电子对与水分子易形成氢键。而吡啶、呋喃和噻吩杂原子的未共用电子对是6电子闭合共轭体系的组成部分,失去形成氢键的条件,因此难溶于水。
三、重要的杂环化合物及其衍生物
(一)吡咯、咪唑及其衍生物
吡咯存在于煤焦油和骨焦油中,为无色液体,沸点131℃。吡喀的蒸气可使浸有盐酸的松木片产生红色,称为吡咯的松木片反应。
吡咯的衍生物广泛分布于自然界,叶绿素、血红素、维生素B12及许多生物碱中都含有吡咯环。
四个吡咯环的α碳原子通过四个次甲基(-CH=)交替连接构成的大环叫卟吩环,旧称环。卟吩的成环原子都在同一平面上,是一个复杂的共轭体系。卟吩本身在自然界中不存在,它的取代物称为卟啉类化合物,却广泛存在。卟吩能以共价键和配位键与不同的金属原子结合,如血红素的分子结构中结合的是亚铁原子。
血红素与蛋白质结合成为血红蛋白,存在于哺乳动物的红细胞中,是运输氧气的物质。
卟吩 血红素
咪唑的衍生物广泛存在于自然界,如蛋白质组成成分之一的组氨酸。组氨酸经酶的作用或体内分解,可脱羧变成组胺。
组氨酸组胺
组胺有收缩血管的作用。人体内组胺含量过多时会发生过敏反应。
(二)吡啶的重要衍生物
吡啶的重要衍生物有烟酸、烟酰胺、异烟肼等。
烟酸和烟酰胺两者组成维生素PP。它们是B族维生素之一,体内缺乏时能引起糙皮病。烟酸还具有扩张血管及降低血胆固醇的作用。
异烟肼又叫雷米封(Rimifon),为无色晶体或粉末,易溶于水,微溶于乙醇而不溶于乙醚。异烟肼具有较强的抗结核作用,是常用治疗结核病的口服药。
(三)嘧啶及其衍生物
嘧啶是含有两个氮原子的六元杂环化合物。它是无色固体,熔点22℃,易溶于水,具有弱碱性。
嘧啶
嘧啶可以单独存在,也可与其它环系稠合而存在于维生素、生物碱及蛋白质中。许多合成药物如巴比妥类药物、磺胺嘧啶等,都含有嘧啶环。
嘧啶的衍生物如胞嘧啶,尿嘧啶和胸腺嘧啶是核酸的组成成分。
上述嘧啶衍生物有酮式和烯醇式的互变异构现象。如尿嘧啶的互变异构:
(四)嘌呤及其衍生物
嘌呤是咪唑环和嘧啶环稠合而成的稠杂环。嘌呤环共有四个氮原子,环的编号比较特殊,它有两种互变异构体,常用标氢法区别。
结晶态嘌呤为(Ⅰ)式,在水溶液中(Ⅰ)式与(Ⅱ)式则以等比例共存。药物分子中一般多为7H-嘌呤(Ⅰ式)衍生物,生物体中则9H-嘌呤(Ⅱ式)更为常见。
嘌呤为无色晶体。熔点216-217℃,易溶于水,能与强酸或强碱成盐。
嘌呤本身在自然界并不存在,但它的衍生物分布广,而且重要,如腺嘌呤、鸟嘌呤等都是核酸的组成成分。

腺嘌呤(A) 鸟嘌呤(G)
(6-氨基嘌呤) (2-氨基-6-羟基嘌呤)
次黄嘌呤、黄嘌呤和尿酸是腺嘌呤和鸟嘌呤在体内的代谢产物,存在于哺乳动物的尿和血中。
次黄嘌呤黄嘌呤尿酸
(6-氧嘌呤) (2,6-二氧嘌呤)(2,6,8-三氧嘌呤)
尿酸为无色晶体,极难溶于水,有弱酸性。健康的人每天尿酸的排泄量约为0.5-1g。如代谢紊乱而致尿酸含量过高时,可能沉积形成尿结石。当血中的尿酸含量过高时,可能沉积在关节等处,形成痛风石。
上述嘌呤衍生物均有酮式和烯醇式的互变异构现象。如尿酸和黄嘌呤。
尿酸:

酮式烯醇式
黄嘌呤:
酮式 烯醇式
第二节 生物碱
一、 概述
在生物体内成分中,含氮碱基的有机化合物,能与酸反应生成盐类,将此类化合物称为生物碱。它是一类存在于生物(主要是植物)体内、对人和动物有强烈生理作用的含氮的碱性物质。生物碱的分子构造多数属于仲胺、叔胺或季胺类,少数为伯胺类。它们的构造中常含有杂环,并且氮原子在环内。生物碱常常是很多中草药中的有效成分,例如,麻黄中的平喘成分麻黄碱、黄连中的抗菌消炎成分小檗碱(黄连素)和长春花中的抗癌成分长春新碱等。
生物碱大多数来自植物界,少数也来自动物界,如贤上腺素等。生物体内生物碱含量一般较低。至今分离出来的生物碱已有数千种,其中用于临床的近百种。
二、生物碱的分类和命名
生物碱的分类方法有多种。较常用和比较合理的分类方法是根据生物碱的化学构造进行分类,如麻黄碱属有机胺类,一叶萩碱、苦参碱属吡啶衍生物类,莨菪碱属莨菪烷衍生物类,喜树碱属喹啉衍生物类,常山碱属喹唑酮衍生物类,茶碱属嘌呤衍生物类,小檗碱属异喹啉衍生物类,利血平、长春新碱属吲哚衍生物类等。
生物碱多根据它所来源的植物命名,例如,麻黄碱是由麻黄中提取得到而得名,烟碱是由烟草中提取得到而得名。生物碱的名称又可采用国际通用名称的译音,例如烟碱又叫尼古丁(nicotine)。
三、生物碱的一般性质
(一)一般性状
游离的生物碱为结晶形或非结晶形的固体,也有液体,如烟碱。多数生物碱无色,但有少数例外,如小檗碱和一叶萩碱为黄色。多数生物碱味甚苦,具有旋旋光性,左旋体常有很强的生理活性。
(二)酸碱性
大多数生物碱具有碱性,这是由于它们的分子构造中都含有氮原子,而氮原子上又有一对未共享电子对,对质子有一定吸引力,能与酸结合成盐,所以呈碱性。各种生物碱的分子结构不同,特别是氮原子在分子中存在状态不同,所以碱性强弱也不一样。分子中的氮原子大多数结合在环状结构中,以仲胺、叔胺及季胺碱三种形式存在,均具有碱性,以季铵碱的碱性最强。若分子中氮原子以酰胺形式存在时,碱性几乎消失,不能与酸结合成盐。有些生物碱分子中除含碱性氮原子外,还含有酚羟基或羧基,所以既能与酸反应,也能与碱反应生成盐。
(三)溶解性
游离生物碱极性较小,一般不溶或难溶于水,能溶于氯仿、二氯乙烷、乙醚、乙醇、丙酮、苯等有机溶剂,在稀酸水溶液中溶解而成盐。生物碱的盐类极性较大,大多易溶于水及醇,不溶或难溶于苯、氯仿、乙醚等有机溶剂;其溶解性与游离生物碱恰好相反。
生物碱及其盐类的溶解性也有例外的情况。季铵碱如小檗碱、酰胺型生物碱和一些极性基团较多的生物碱则一般能溶于水,习惯上常将能溶于水的生物碱叫做水溶性生物碱。中性生物碱则难溶于酸。含羧基、酚羟基或含内酯环的生物碱等能溶于稀碱溶液中。某些生物碱的盐类如盐酸小檗碱则难溶于水,另有少数生物碱的盐酸盐能溶于氯仿中。
生物碱的溶解性对提取、分离和精制生物碱十分重要。
(四)沉淀反应
生物碱或生物碱的盐类水溶液,能与一些试剂生成不溶性沉淀。这种试剂称为生物碱沉淀剂。此种沉淀反应可用以鉴定或分离生物碱。常用的生物碱沉淀剂有:碘化汞钾(HgI2·2KI)试剂(与生物碱作用多生成黄色沉淀);碘化铋钾(BiI3·KI)试剂(与生物碱作用多生成黄褐色沉淀);碘试液、鞣酸试剂、苦味酸试剂、苦味酸试剂分别与生物碱作用,多生成棕色、白色、黄色沉淀。
(五)显色反应
生物碱与一些试剂反应,呈现各种颜色,也可用于鉴别生物碱。例如,钒酸铵-浓硫酸溶液与吗啡反应时显棕色、与可待因反应显蓝色、与莨菪碱反应则显红色。此外,钼酸铵的浓硫酸溶液,浓硫酸中加入少量甲醛的溶液,浓硫酸等都能使各种生物碱呈现不同的颜色。
四、重要的生物碱
(一)烟碱
烟草中含十余种生物碱,主要是烟碱,约含2%-8%,纸烟中约含1.5%。
烟碱又名尼古丁,属吡啶衍生物类生物碱。
烟碱有剧毒,少量对中枢神经有兴奋作用,能升高血压,大量则抑制中枢神经系统,使心脏麻痹以至死亡。几毫克的烟碱就能引起头痛、呕吐、意识模糊等中毒症状,吸烟过多的人逐渐会引起慢性中毒。
(二)莨菪碱和阿托品
莨菪碱和阿托品属莨菪烷衍生物类生物碱。莨菪烷的构造式如下:
莨菪碱是由莨菪酸和莨菪醇缩合形成的酯,莨菪醇是由四氢吡咯环和六氢吡啶环稠合而成的双环构造。
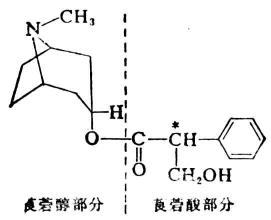
莨菪碱
莨菪碱是左旋体,由于莨菪酸构造中的手性碳原子上的氢与羰基相邻,是α活泼氢,容易发生酮式-烯醇式互变异构而外消旋。当莨菪碱在碱性条件下或受热时均可发生消旋作用,变成消旋的莨菪碱,即阿托品。莨菪酸的互变异构现象如下:
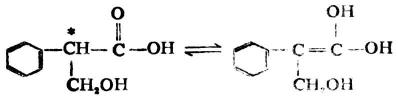
医疗上常用硫酸阿托品作抗胆碱药,能抑制唾液、汗腺等多种腺体的分泌,并能扩散瞳孔;还用于平滑肌痉挛、胃和十二指肠溃疡病;也可用作有机磷、锑剂中毒的解毒剂。
除莨菪碱外,我国学者又从茄科植物中分离出两种新的莨菪烷系生物碱,即山莨菪碱和樟柳碱。两者均有明显的抗胆碱作用,并有扩张微动脉,改善血液循环的作用。用于散瞳、慢性气管炎的平喘等;也能解除有机磷中毒。其毒性比硫酸阿托品小。
(三)吗啡和可待因
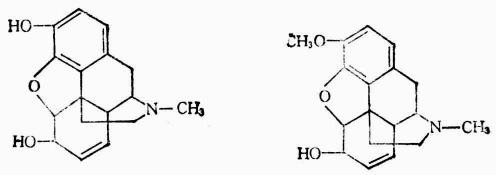
吗啡 可待因
罂粟科植物鸦片中含有20多种生物碱,其中比较重要的有吗啡、可待因等。这两种生物碱属于异喹啉衍生物类,可看作为六氢吡啶环(哌啶环)与菲环相稠合而成的基本结构。
吗啡对中枢神经有麻醉作用,有极快的镇痛效力,但易成瘾,不宜常用。
可待因是吗啡的甲基醚(甲基取代吗啡分子中酚羟基的氢原子)。可待因与吗啡有相似的生理作用,可用以镇痛,但可待因主要用作镇咳剂。
麻醉剂海洛因是吗啡的二乙酰基衍生物,即二乙酰基吗啡(两个乙酰基分别取代吗啡分子中两个羟基的氢原子)。
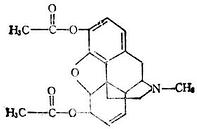
海洛因
海洛因镇痛作用较大。并产生欣快和幸福的虚假感觉,但毒性和成瘾性极大,过量能致死。海洛因被列为禁止制造和出售的毒品。
(四)麻黄碱
麻黄碱是含于中药麻黄中的一种主要生物碱,又叫麻黄素。一般常用的麻黄碱系指左旋麻黄碱,它与右旋的伪麻黄碱互为旋光异构体。它们在苯环的侧链上都有两个手性碳原子,应有四个旋光异构体,但在中药麻黄植物中只存在(-)-麻黄碱和(+)-伪麻黄碱两种,并且二者是非对映异构体。
麻黄碱和伪麻黄碱都是仲胺类生物碱,不具含氮杂环,因此它们的性质与一般生物碱不尽相同,与一般的生物碱沉淀剂也不易发生沉淀。
(-)-麻黄碱具有兴奋中枢神经、升高血压、扩大支气管、收缩鼻粘膜及止咳作用,也有散瞳作用,临床上常用盐酸麻黄碱(即盐酸麻黄素)治疗气喘等症。
(五)小檗碱
小檗碱又名黄连素,存在于小檗属植物黄柏、黄连和三颗针中,它属于异喹啉衍生物类生物碱,是一种季铵化合物。
小檗碱(黄连素)
黄连素具有较强的抗菌作用,在临床上常用盐酸黄连素治疗菌痢、胃肠炎等疾病。
(六)长春新碱
长春新碱又名醛基长春碱,存在于夹竹桃科植物长春花中,属于双聚吲哚类生物碱。
长春新碱
长春新碱对白血病、癌症均有效,且毒性较低。
第二十章 脂类和甾族化合物
在人体和动植物组织成分中,含有油脂和类脂,它们总称为脂类。油脂(脂肪和油)是甘油和高级脂肪酸生成的酯。类脂是构造或理化性质类似油脂的物质,主要包括磷脂、糖脂、蜡和甾族化合物。脂类化合物的共同特征是:难溶于水而易溶于乙醚、氯仿、丙酮、苯等有机溶剂;都能被生物体所利用,是构成生物体的重要成分。
脂类在生理上具有非常重要的意义。脂肪在体内氧化时放出大量热量,作为能源的储备物;它在脏器周围能保护内脏免受外力撞伤;在皮下有保温作用。脂肪还是维生素A,D,E和K等许多活性物质的良好溶剂。类脂是组织细胞的重要成分,它们在细胞内和蛋白质结合在一起形成脂蛋白,构成细胞的各种膜,如细胞膜和线粒体膜等。
甾族化合物是一类重要的天然产物,广泛地存在于动植物组织中。例如存在于动物体内的胆甾醇、胆汁酸、维生素D、肾上腺皮质激素和性激素;存在于植物中的强心苷和甾族生物碱等。它们在生理活动中都起着十分重要的作用。
第一节 油脂
一、油脂的组成
油脂是油和脂肪的总称,习惯上把在常温下为液体的叫做油,为固体的叫做脂肪。从化学构造来看,它们都是高级脂肪酸甘油酯。
组成油脂的脂肪酸,已知的约有50多种。常见的高级脂肪酸见表20-1。
表20-1 组成常见油脂的重要脂肪酸
| 类别 | 名称 | 构造式 |
| 泡和脂肪酸 | 月桂酸(十二烷酸) | CH3(CH2)10COOH |
| 肉豆蔻(十四烷酸) | CH3(CH2)12COOH | |
| 棕榈酸(十六烷酸、软脂酸) | CH3(CH2)14COOH | |
| 硬脂酸(十八烷酸) | CH3(CH2)16COOH | |
| 二十四烷酸 | CH3(CH2)22COOH | |
| 不饱和脂肪酸 | 棕榈油酸(9-十六碳烯酸) | CH3(CH2)5CH=CH(CH2)7COOH |
| 油酸(9-十八碳俙酸) | CH3(CH2)5CH=CH(CH2)7COOH | |
| 蓖麻油酸(12-羟基-9-十八碳烯酸) | CH3(CH2)5CHOHCH2CH=CH(CH2)7COOH | |
| 亚油酸(9,12-十八碳二烯酸) | CH3(CH2)3(CH2CH=CH)2(CH2)7COOH | |
| γ-亚油酸(6,9,12-十八碳三烯酸) | CH3(CH2)3(CH2CH=CH)2(CH2)4COOH | |
| 亚麻酸(9,12,15-十八碳三烯酸) | CH3(CH2CH=CH)3(CH2)7COOH | |
| 桐油酸(9,11,13-十八碳三烯酸) | CH3(CH2)3(CH=CH)3(CH2)7COOH | |
| 花生四烯酸(5,8,11,14-二十碳四烯酸) | CH3(CH2)3(CH2CH=CH)4(CH2)3COOH | |
| 神经酸(15-二十四碳烯酸) | CH3(CH2)7CH=CH(CH2)13COOH |
组成油脂的天然脂肪酸的共同特点是:(1)绝大多数是含偶数碳原子的直链羧酸,其中以C16和C18为多;(2)大多数含有一个、两个或三个双键,基中以C18不饱和酸为主;(3)几乎所有的不饱和脂肪酸都是顺式构型。
多数脂肪酸在人体中内都能合成,只有亚油酸、亚麻酸和花生四烯酸等多双键的不饱和脂肪酸,它们不能在人体内合成,必须由食物供给,故称为必需脂肪酸。
在油脂分子中,若三个脂肪酸部分是相同的,称为单甘油酯(简单三酰甘油);若不同则叫做混甘油酯(混合三酰甘油)。
甘油酯命名时将脂肪酸名称放在前面,甘油的名称放在后面,叫做某酸甘油酯(或某脂酰甘油)。如果是混合甘油酯,则需用α,α`和β分别表明脂肪酸的位次。例如:
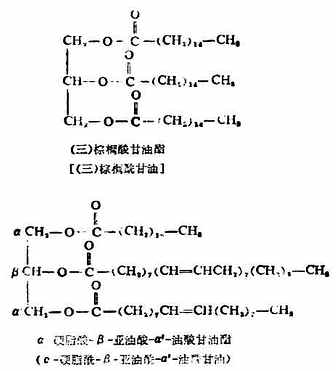
天然油脂是各种混合甘油酯的混合物。一些脂肪和油的脂肪酸组成列于表20-2。
表20-2 一些脂肪和油的脂肪酸组成
| 脂肪或油 | 脂肪酸(质量百分数) | ||||||
| 月桂酸 | 肉豆蔻酸 | 棕榈酸 | 硬脂酸 | 油酸 | 亚油酸 | 亚麻酸 | |
| 猪油 | 1~2 | 25~30 | 12~16 | 40~50 | 5~10 | 1 | |
| 奶油① | 2~5 | 8~14 | 25~30 | 9~12 | 25~35 | 2~5 | |
| 牛油 | 3~5 | 25~30 | 20~30 | 40~50 | 1~5 | ||
| 椰子油② | 45~48 | 16~18 | 8~10 | 2~4 | 5~8 | 1~2 | |
| 橄榄油 | 8~16 | 2~3 | 70~85 | 5~15 | |||
| 豆油 | 10 | 3 | 25~30 | 50~55 | 4~8 | ||
| 棉子油 | 1 | 20~25 | 1~2 | 20~30 | 45~50 | ||
| 红花油 | 6 | 3 | 13~15 | 75~78 | |||
| 亚麻子油 | 20~35 | 15~25 | 40~60 | ||||
① 也含3%-4%丁酸和C6,C8和C10酸各1%-3%
② C8和C10酸各含水5%-9%
二、油脂的性质
(一)物理性质
纯净的油脂是无色、无臭、无味的。但是一般油脂,尤其是植物油,有的带有香味或特殊的气味,并且有色。这是因为天然油脂中往往溶有维生素和色素之故。油脂比水轻,相对密度在0.9-0.95之间。难溶于水,易溶于有机溶剂,如热乙醇,乙醚、石油醚、氯仿、四氯化碳和苯等,可以利用这些溶剂从动植物组织中提取油脂。因为油脂是混合物,所以没有恒定的熔点和沸点。
(二)化学性质
1.
一切油脂都能在酸、碱或酶(如胰脂酶)的作用下发生水解反应。1mol油脂水解生成1mol甘油和3mol脂肪酸。
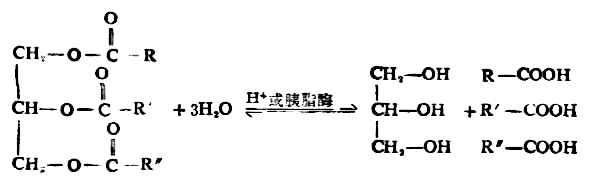
如果在碱性溶液中使油脂水解,则生成甘油和高级脂肪酸的盐类(肥皂),因此油脂在碱性溶液中的水解叫做皂化。例如:
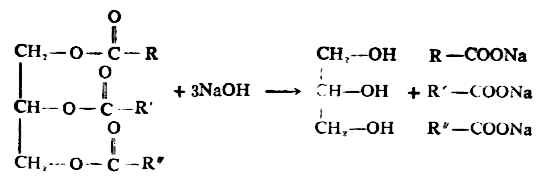
普通肥皂是各种高级脂肪酸钠盐的混合物。油脂用氢氧化钾皂化所得的高级脂肪酸钾盐质软,叫做软皂。医学上常以洗净皮肤。“来苏儿”就是由煤酚和软皂制成的。
1g油脂完全皂化时所需氢氧化钾的质量(单位毫克)称为皂化值。根据皂化值的大小,可以判断油脂所含油脂的平均相对分子质量。油脂中甘油酯的平均相对分子质量越大,则1g 油脂所含甘油酯物质的量越少,皂化时所需碱的量也越少,即皂化值越小。反之,皂化值越大,表示甘油酯的平均相对分子质量越小,即1g油脂所含甘油酯的物质的量越多。
人体摄入的油脂主要在小肠内进行催化水解,此过程叫做消化。水解产物透过肠壁被吸收(少量油脂微粒同时被吸收),进一步合成人体自身的脂肪。这种吸收后的脂肪除一部分氧化供给能量(每克脂肪在体内完全氧化放出38.9kJ热能)外,大部分贮存于皮下,肠系膜等处脂肪组织中。
脂肪乳剂一般用精制植物油(如豆油等)与磷脂酰胆碱、甘油及水混合,用物理方法制成白色而稳定的脂肪乳剂,供静脉注射,广泛用于晚期癌症和术后康复等。
2.酸败
油脂在空气中放置过久,就会变质产生难闻的气味,这种变化叫做酸败。酸败是由空气中的氧、水分或微生物作用引起的。油脂中不饱酸的双键部分受到空气中氧的作用,氧化成过氧化物,后者继续分解或进一步氧化,产生有臭味的低级醛或羧酸。光、热或湿气都可以加速油脂的酸败。
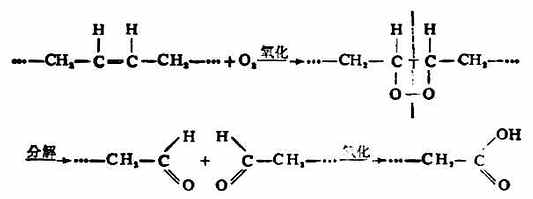
油脂酸败的另一原因是由于微生物或酶的作用。油酯先水解为脂肪酸,脂肪酸在微生物或酶的作用下发生β氧化,即羧酸中的β碳原子被氧化为羰基,生成β-酮酸,后者进一步分解则生成含碳较少的酮或羧酸。
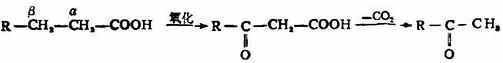
油脂酸败的产物有毒性和刺激性,因此酸败的油脂不能食用或药用。
第二节 类脂
一、磷脂
磷脂是含磷的类脂化合物,广泛地分布在动植物中,是细胞原生质的固定组成成分。磷脂主要存在于脑、神经组织、骨髓、心、肝及肾等器官中。蛋黄、植物种子、胚芽及大豆中都含有丰富的磷脂。最常见的磷脂是磷脂酰胆碱、磷脂酰乙醇胺和神经鞘磷脂。它们的构造与油脂相似,但组成较为复杂。它们的水解产物有醇(甘油或其它醇)、脂肪酸、磷酸和含氮的有机碱。
(一)磷脂酰胆碱(卵磷脂)
纯的磷脂酰胆碱是吸水性的白色蜡状物,在空气中由于不饱和脂肪酸的氧化而变为黄色或棕色。磷脂酰胆碱不溶于水及丙酮,易溶于乙醚、乙醇及氯仿中。磷脂酰胆碱在脑、神经组织、肝脏、肾上腺及红细胞中含量较多,蛋黄中含量特多(约占8%-10%),所以叫做卵磷脂。
磷脂酰胆碱根据磷酸与甘油连接位置的不同,有α-及β-两种异构体,自然界的磷脂酰胆碱是α型的。磷酯酰胆碱中与磷酸相结合的含氮有机碱是胆碱。磷脂酰胆碱分子中,甘油部分的β碳原子是手性碳原子,因而有D型和L型两种构型。自然界存在的是L型的。
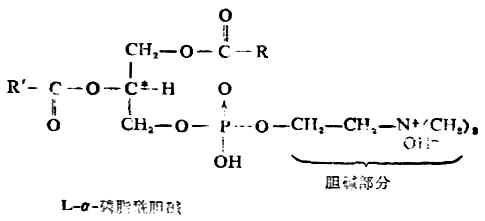
自然界的磷脂酰胆碱是几种磷脂酰胆碱的混合物,主要是组分中的脂肪酸不同,经水解后得到甘油、脂肪酸、磷酸和胆碱。常见于磷脂酰胆碱中的脂肪酸有棕榈酸、硬脂酸、油酸、亚油酸、亚麻酸及花物四烯酸等。某些毒蛇的毒汁中含有一种磷脂酶,能使β位脂肪酰基水解脱落,生成溶血磷脂酰胆碱,从而破坏了细胞膜,引起溶血。
(二)磷脂酰乙醇胺(脑磷脂)
磷脂酰乙醇胺在脑组织中含量甚多,故又称脑磷脂。它和磷脂酰胆碱并存于机体各组织及器官中,它的构造和理化性质均与磷脂酰胆碱相似,只是在磷脂酰乙醇胺中,与磷酸结合的是胆胺(HO=CH2-CH2-NH2)。
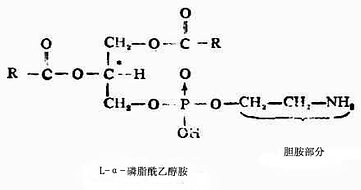
磷脂酰乙醇胺性质与磷脂酰胆碱相似,也不稳定,易吸收水分,在空气中氧化成棕黑色。磷脂酰乙醇胺能溶于乙醚,但难溶于乙醇,这是与磷脂酰胆碱在溶解性方面的不同点。
磷脂酰乙醇胺与血液凝固有关。凝血激酶是由磷脂酰乙醇胺与蛋白质组成的,它存在于血小板内,能促使血液凝固。
(三)神经鞘磷脂(鞘磷脂)
脑和神经组织中含有大量的鞘磷脂,脾、肝及其它组织中含量较少。鞘磷脂的组成和结构与磷脂酰胆碱、磷脂酰乙醇胺不同,其分子中不含甘油部分,而是含有一个长链的不饱醇——鞘氨醇。1mol鞘磷脂完全水解后,可得到鞘氨醇、脂肪酸、磷酸和胆碱各1mol。
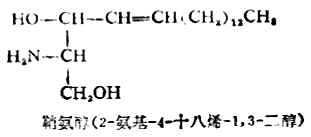
鞘磷脂分子中的脂肪酸连接在鞘氨醇的氨基上,磷酸以酯的形式与鞘氨醇及胆碱相结合。
鞘磷脂是无色晶体,在光的作用下或在空气中不易氧化,比较稳定,不溶于丙酮及乙醚,而溶于热乙醇中。
二、糖脂
糖脂是细胞结构包括神经髓鞘的组成部分,也是构成血型物质及细胞抗原的重要组分。重要的糖脂有脑苷脂、神经节苷脂等。脑苷脂是含糖、脂肪酸和鞘氨醇的类脂,其构造如下:
脑苷脂
脑苷脂为白色蜡状物,溶于热乙醇、丙酮和苯中,不溶于乙醚,冷的乙醇和丙酮中。
三、甾族化合物
甾族化合物是一类广泛存在于动植物体内的天然有机化合物,如胆甾醇、胆汁酸、维生素D、肾上腺皮质激素及性激素等。许多甾族化合物具有重要的生理作用。
(一)甾族化合物的结构
甾族化合物都含有一个由四个环组成的基本骨架,即由三个六元环的一个五元环稠合的17碳结构。这个骨架是甾族化合物的母核,即环戊烷多氢菲。四个环用字母A,b ,C和D表示,并将17个碳原子按特定顺序编号。
大多数甾族化合物在环戊烷多氢菲的母核上还有三个侧链,它们分别连在C-10,C-13和C-17的碳原子上。
在C-10和C-13上常是甲基(有时是-CHO或-CH2OH),叫做角甲基,这两个甲基的碳原子分别标为C-19及C-18;C-17上连接的是较长的碳链、含氧原子团或其它原子团。这三个原子团都在环平面的上方故用实线表示。环上若有其它取代基,则它们在空间有两种取向。环上的取代基与角甲基取向相同的(即在环平面的上方),称为β构型,用实线表示;如环上取代基与角甲基取向相反(即在环平面的下方),则称为α构型,用虚线表示。
(二)重要的甾族化合物
1. 甾醇类
甾醇是甾环上连有醇羟基的固态物质,故又叫做固醇。从化学结构上看,甾醇是一类饱和的或不饱和的仲醇,C-3上的羟基都是β型的,它们常以游离状态或高级脂肪酸酯的形式存在于动植物体内。
(1)胆甾醇胆甾醇是从胆石中发现的固体状醇,故又称胆固醇。存在于人体的各组织中。
胆甾醇
胆甾醇的结构特点是C-3上有一个β-构型的羟基,C-5和C-6之间有一个双键,C-17上有一个含8个碳原子的烃基侧链。
胆甾醇为无色或略带黄色的蜡状物,熔点148℃,难溶于水,易溶于有机溶剂。
在体内胆甾族C-3上-OH常与脂肪酸结合成胆甾醇脂。
人体中的胆甾醇一部分从食物中摄取,一部分由体内组织细胞自己合成。当人体内胆甾醇代谢发生障碍时,血液中胆甾醇的含量就会增多,并从血清中析出,引起血管变窄,降低血液流速,造成高血压、动脉硬化;在胆汁液中,若有胆甾醇沉积,则形成胆石。
(2)7-脱氢胆甾醇 7-脱氢胆甾醇也是一种动物甾醇,存在于人体皮肤中。当受到紫外线照射时,它的B环打开转变为维生素D3。
7-脱氢胆醇 维生素D3
因此,多晒太阳是获得维生素D3的最简单方法。
(3)麦角甾醇麦角甾醇存在于酵母及某些植物中,属于植物甾醇,和7-脱氢胆甾醇比较,它在C-17的侧链上多一个甲基和一个双键。在紫外线照射下,它的B环打开生成维生素D2。
麦角甾醇 维生素D2
维生素D也叫抗佝偻病维生素,因为缺乏时,儿童会得佝偻病,成人则患软骨症。因此,儿童需要多服用一些维生素D,同时需要多晒太阳。维生素D广泛存在于动物体中,含量最多的是脂肪丰富的鱼类肝脏;也存在于牛乳、蛋黄中等。
维生素D包括几种生理作用相同的物质,其中以维生素D2和D3的作用最强,由于维生素D能促进肠道对钙、磷的吸收,使血液中钙、磷浓度增加,有利于钙、磷沉着,所以能防治佝偻病和软骨病。维生素D是脂溶性维生素,对热和空气中的氧都比较稳定。
2.胆甾酸
在人和动物的胆汁中,含有几种结构与胆甾醇类似的酸,称为胆甾酸。例如胆酸和脱氧胆酸。
它们的结构 特征是:C-17上的侧链较短,只有五个碳原子,末端有一个羧基;胆酸的C-3、C-7和C-12上的羟基为α构型,用虚线表示,和胆酸相比较,脱氧胆酸只是在C-7上少一个氧原子;它们的环上都无双键。
胆酸和脱氧胆酸与甘氨酸(H2N-CH2-COOH)或牛磺酸(H2N-CH2-CH2-SO3H)以酰胺键相结合,这种结合胆酸总称为胆汁酸。在碱性胆汁中,胆汁酸以钠盐或钾盐形式存在,称为胆盐。
分泌到肠中的胆盐是一种乳化剂,对脂肪的消化起着重要作用。胆盐是一种表面活性物质,能降低水的界面张力,使脂肪乳化为微粒并稳定地分散于消化液中,增加了脂肪与脂肪酶的接触机会,从而加速脂肪的水解,以利于脂肪的消化吸收。乳化的脂肪不仅容易消化,而且一部分高度乳化的脂肪微粒,可不经消化而直接由肠粘膜吸收。
3.甾体激素(类甾醇激素)
激素是由动物体内各种内分泌腺分泌的一类化学活性物质,具有很强的生理作用,主要是控制生长、调节代谢和性的功能等。激素分为两大类,一类是含氮激素,如肾上腺素、甲状腺素和胰岛素等;另一类就是甾体激素。根据来源甾体激素又可分肾上腺皮质激素和性激素两类。
(1)肾上腺皮质激素 肾上腺皮质激素是产生于肾上腺皮质部分的一类激素。现已从肾上腺皮质中提出30多种甾族化合物,其中有七种活性较大的激素。这七种化合物的结构特征是:C-3上均有酮基;C-4,5为双键;C-17上有β-羟甲基羰基。它们区别在于,C-11上有无含氧基团和
C-17上有无α-羟基。一般规律是C-11上有含氧基团的肾上腺皮质激素是调节糖代谢的(醛固酮例外),C-11上无含氧基团的为调节水及无机盐代谢的;C-17上有α-羟基的,其生理功能加强。
具有调节糖代谢作用的肾上腺皮质激素有
具有调节水及无机盐代谢作用的有:
在药物方面,可的松和氢化可的松具有抗炎症、抗过敏、抗病毒、抗休克等药理作用,临床上多用以控制严重中毒性感染和风湿病等。目前医药常用比可的松更有效的药物——醋酸可的松和强的松。
(2)性激素性激素可分为雄性激素和雌性激素两类。它们分别是由睾丸和卵巢分泌的物质,对生育功能及第二性征如声音、体型的改变都有决定性作用。
性激素的结构特征是:C-3含有氧;C-4,5间大多数有双键;C-17上没有较长的侧链;环的骨架基本相同,只是取代基或它们的空间排布不同。
睾丸酮是雄性激素,能促进雄性器官和第二性征的发育。临床上多用它的衍生物,如甲基睾丸酮、睾丸酮丙酸酯等。
睾丸酮 甲基睾丸酮 睾丸酮丙酸酯
黄体酮是雌性激素之一,它的生理作用是抑制排卵,并使子宫内的受精卵和胎儿正常发育,临床上用于治疗习惯性流产、子宫功能性出血、痛经和月经失调等。
黄体酮
雌二醇是另一类雌性激素,其结构特征是A环为苯环,C-3上有酚羟基;C-10上无角甲基,C-17上有羟基。由于C-17上羟基构型不同,生理作用也有很大差异,如β-雌二醇的生理活性比α-雌二醇强得多。因此,临床上都采用β-雌二醇。
β-雌二醇是白色或乳白色粉末,临床上用于卵巢机能不全引起的病症,如子宫发育不全、月经失调等的治疗。
β-雌二醇 α-雌二醇
第二十一章 糖类
糖类化合物亦称碳水化合物,是自然界存在最多、分布最广的一类重要的有机化合物。葡萄糖、蔗糖、淀粉和纤维素等都属于糖类化合物。
糖类化合物是一切生物体维持生命活动所需能量的主要来源。它不仅是营养物质,而且有些还具有特殊的生理活性。例如:肝脏中的肝素有抗凝血作用;血型中的糖与免疫活性有关。此外,核酸的组成成分中也含有糖类化合物——核糖和脱氧核糖。因此,糖类化合物对医学来说,具有更重要的意义。
糖类化合物由C,H,O三种元素组成,分子中H和O的比例通常为2:1,与水分子中的比例一栗,可用通式Cm(H2o )n表示。因此,曾把这类化合物称为碳水化合物。但是后来发现有些化合物按其构造和性质应属于糖类化合物,可是它们的组成并不符合Cm(H2o )n 通式,如鼠李糖(C6H12O5)、脱氧核糖(C5H10O4)等;而有些化合物如乙酸(C2H4O2)、乳酸(C3H6O3)等,其组成虽符合通式Cm(H2o )n,但结构与性质却与糖类化合物完全不同。所以,碳水化合物这个名称并不确切,但因使用已久,迄今仍在沿用。
从化学构造上看,糖类化合物是多羟基醛、多羟基酮以及它们的缩合物。例如:
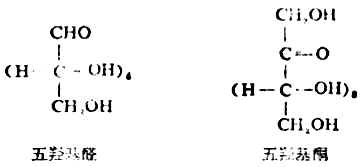
糖类化合物可根据能还被水解及水解产物的情况分为三类。
单糖:不能水解的多羟基醛或多羟基酮。如葡萄糖、果糖等。
二糖:水解后生成两分子单糖的糖。如蔗糖、麦芽糖等。
多糖:能水解生成许多分子单糖的糖。如淀粉、糖原、纤维素等。
糖类常根据其来源而用俗名。
第一节 单糖
单糖一般是含有3-6个碳原子的多羟基醛或多羟基酮。最简单的单糖是甘油醛和二羟基丙酮。

按碳原子数目,单糖可分为丙糖、丁糖、戊糖、己糖等。自然界的单糖主要是戊糖和己糖。根据构造,单糖又可分为醛糖和酮糖。多羟基醛称为醛糖,多羟基酮称为酮糖。例如,葡萄糖为己醛糖,果糖为己酮糖。单糖中最重要的与人们关系最密切的是葡萄糖等。
一、单糖的结构
葡萄糖的分子式为C6H12O6,分子中含五个羟基和一个醛基,是己醛糖。其中C-2,C-3,C-4和C-5是不同的手性碳原子,有16个(α4=16)具有旋旋光性的异构体,D-葡萄糖是其中之一。存在于自然界中的葡萄糖其费歇尔投影中,四个手性碳原子除C-3上的-OH在左边外,其它的手性碳原子上的-OH都在右边。
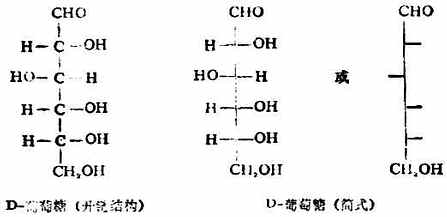
单糖构型的确定仍沿用D/L法。这种方法只考虑与羰基相距最远的一个手性碳的构型,此手性碳上的羟基在右边的D型,在左边的L型。自然界存在的单糖多属D型糖。例如:
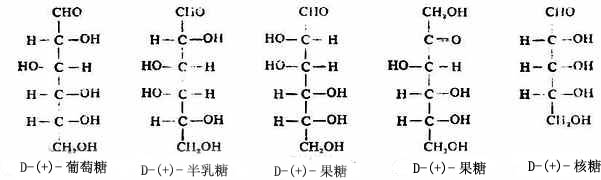
六碳以下的D型醛见表21-1。
(二)葡萄糖的环状结构和变旋现象
结晶葡萄糖有两种,一种是从乙醇中结晶出来的,熔点146℃。它的新配溶液的[α]D为+112°,此溶液在放置过程中,比旋光度逐渐下降,达到+52.17°以后维持不变;另一种是从吡啶中结晶出来的,熔点150℃,新配溶液的[α]D为+18.7°,此溶液在放置过程中,比旋光度逐渐上升,也达到+52.7°以后维持不变。糖在溶液中,比旋光度自行转变为定值的现象称为变旋现象。显然葡萄糖的开链结构不能解释此现象。
从葡萄糖的开链结构可见,它既具有醛基,也有醇羟基,因此在分子内部可以形成环状的半缩醛。
成环时,葡萄糖的羰基与C-5上的羟基经加成反应形成稳定的六元环。葡萄糖分子虽然具有醛基,但在反应性能上与一般的醛有许多差异,例如对NaHSO3的加成非常缓慢,其原因是在溶液中,葡萄糖几乎以环状的半缩醛结构存在的缘故。
表21-1 六碳以下的D型醛糖
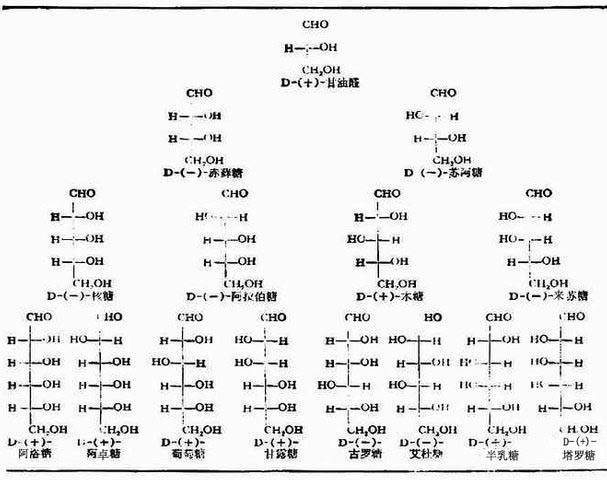
成环后,使原来的羰基碳原子(C-1)变成了手性碳原子,C-1上新形成的半缩醛羟基在空间的排布方式有两种可能。半缩醛羟基与决定单糖构型的羟基(C-5上的羟基)在碳链同侧的叫做α型,在异侧的称为β型。α型和β型是非对映异构体。它们的不同点是C-1上的构型,因此又称为异头物(端基异构体)。它们的熔点和比旋光度都不同。
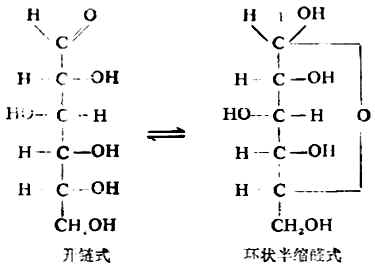
葡萄糖的变旋现象,就是由于开链结构与环状结构形成平衡体系过程中的比旋光度变化所引起的。在溶液中α-D-葡萄糖可转变为开链式结构,再由开链结构转变为β-D-葡萄糖;同样β-D-葡萄糖也变转变为开链式结构,再转变为α-D-葡萄糖。经过一段时间后,三种异构体达到平衡,形成一个互变异构平衡体系,其比旋光度亦不再改变。
不仅葡萄有变旋现象,凡能形成环状结构的单糖,都会产生变旋现象。
(三)环状结构的哈沃斯式和构象式
上述直立的环状费歇尔投影式,虽然可以表示单糖的环状结构,但还不能确切地反映单糖分子中各原子或原子团的空间排布。为此哈沃斯提出用透视式来表示。哈沃斯将直立环式改写成平面的环式。因为葡萄糖的环式结构是由五个碳原子和一个氧原子组成的杂环,它与杂环化合物中的吡喃相似,故称作吡喃糖。连在环上的原子或原子团分别写在环的上方和下方以表示其位置的排布。现将开链的费歇尔投影式改写为哈斯沃式的过程表示如下:
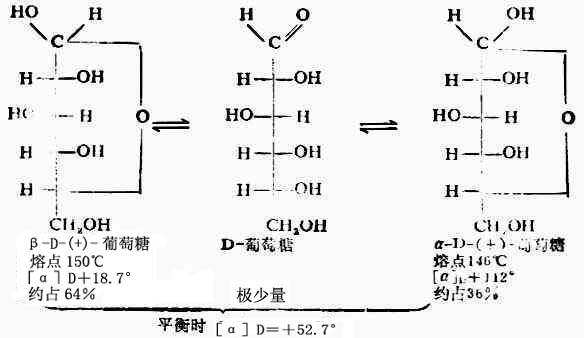
书写哈斯沃式时常省略成环的碳原子,并把朝前面的三个C-C键用粗实线表示。
对D型葡萄糖来说,直立环式右侧的羟基,在哈 斯式中处在环平面下方;直立环式中左侧的羟基,在环平面的上方。成环时,为了使 C-5上的羟基与醛基接近。C(4)-C(5)单键须旋转120°。因此,D型糖末端的羟甲基即在环平面的上方了。C-1上新形成的半缩醛羟基在环平面下方者为α型;在环平面上方者称为β型。
几种重要单糖的哈 沃斯式如下:
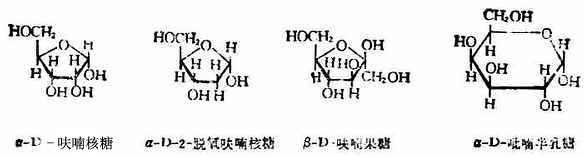
把具有呋喃环结构
的糖称为呋喃糖。
事实丰,形成吡喃环的各个原子,并不完全在一个平面上,而是以较稳定的椅型构象存在。因此,为了更合理地反映其结构,现在常用构象式来表示。α-D-和β-D-葡萄糖的构象式如下:
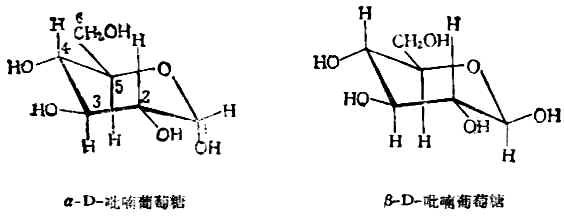
α-D- 吡喃葡萄糖除C-1上的-OH连在α键上,其它三个碳上的-OH和-CH2OH都连在e键上,而β-D吡喃葡萄糖C-1上的-OH及所有比较大的原子团(-OH,-CH2OH)都连在e键上,因而β型的构象更为稳定。故在溶液中达到平衡时,β型占64%,而α型仅占36%。
二、单糖的性质
(一)物理性质
单糖都是无色晶体,味甜,有吸湿性。极易溶于水,难溶于乙醇,不溶于乙醚。单糖有旋旋光性,其溶液有变旋现象。
(二)化学性质
单糖主要以环状结构形式存在,但在溶液中可与开链结构反应。因此,单糖的化学反应有的以环式结构进行,有的以开链结构进行。
1.差向异构化
葡萄糖用稀碱液处理时,会部分转变为甘露糖和果糖,成为复杂的混合物。这咱变化是通老祖宗醇式中间体来完成的。
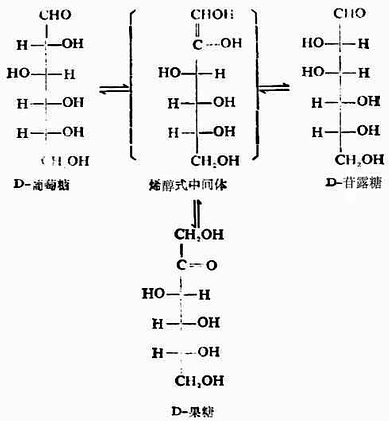
D-果糖、D-甘露糖和D-葡萄糖的C-3、C-4,C-5和C-6的结构完全相同,只有C-1和C-2的结构不同,但是它们的C-1,C-2的结构互变成烯醇型时,其结构完全相同的。因此,不单是D-葡萄糖,而D-果糖或D-甘露糖在稀碱催化下,都能互变为三者的混合物。
在含有多个手性碳原子的具有旋光性的异构体之间,凡只有一个手性碳原子的构型不同时,互称为差向异构体。D-葡萄糖和D-甘露糖就是C-2差向异构体。因此,用稀碱处理D-葡萄糖得到D-葡萄糖、D-果糖三种物质的平衡混合物的反应叫做差向异构化。
2.氧化作用
单糖无论是醛糖或酮糖都可与弱的氧化剂叶伦试剂、费林试剂和本尼迪特试剂作用,生成金属或金属的低价氧化物。上述三种试剂都是碱性的弱氧化剂。单糖在碱性溶液中加热,生成复杂的混合物。
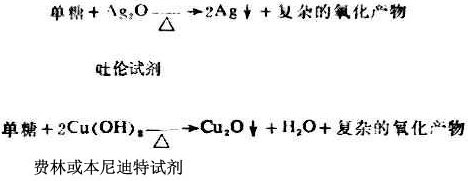
单糖易被碱性弱氧化剂氧化说明它们具有还原性,所以把它们叫做还原糖。
单糖在酸性条件下氧化时,由于氧化剂的强弱不同,单糖的氧化产物也不同。例如,葡萄糖被溴水氧化时,生成葡萄糖酸;而用强氧化剂硝酸氧化时,则生成葡萄糖二酸。
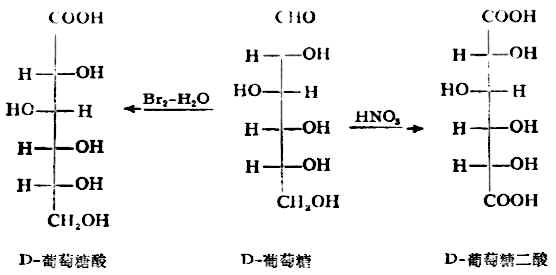
溴水氧化能力较弱,它把醛糖的醛基氧化为羧基。当醛糖中加入溴水,稍加热后,溴水的棕色即可褪去,而酮糖则不被氧化,因此可用溴水来区别醛糖和酮糖。
3.成苷作用
单糖环状半缩醛结构中的半缩醛羟基与另一分子醇或羟基作用时,脱去一分子水而生成缩醛。糖的这种缩醛称为糖苷。例如α-和β-D-吡喃葡萄糖的混合物,在氯化氢催化下同甲醇反应,脱去一分子水,生成α-和β-D-甲基吡喃葡萄糖苷的混合物。
![]()
α-和β-D-吡喃葡萄混合液 β-D-甲基吡喃葡萄糖苷 α-D-甲基吡喃葡萄糖苷
苷由糖和非糖部分组成。非糖部分称为糖苷配基或苷元。糖和糖苷配基脱水后通过过“氧桥”连接,这种键称为苷键。由于单糖的环式结构有α-和β-两种构型,所以可生成α-和β-两种没构型的苷。天然苷多为β-构型。苷的名称是按其组成成分而命名的,并指出苷键和糖的构型。天然苷常按其来源而用俗名。
糖苷结构中已没有半缩醛羟基,在溶液中不能再转变成开链的醛式结构,所以糖工苷无还原性,也没有变旋现象。糖苷在中性或碱性环境中较稳定,但在酸性溶液中或在酶的作用下,则水解生成糖和非糖部分。
糖苷是中草药的有效成分之一,多为无色、无臭、有苦涩味的固体,但黄酮苷和蒽醌苷为黄色。
苷中含有糖部分,所以在水中有一定的溶解性。苷类都有旋光性,天然苷多为左旋体。
4.成酯作用
单糖分子中含多个羟基,这些羟基能与酸作用生成酯。人体内的葡萄糖在酶作用下生成葡萄糖磷酸酯,如1-磷酸吡喃葡萄糖和6-磷酸吡喃葡萄糖等。
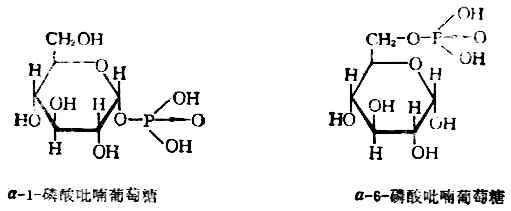
单糖的磷酸酯在生命过程中具有重要意义,它们是人体内许多代谢的中间产物。
5.成脎反应
单糖分子与三分子苯肼作用,生成的产物叫做糖脎。例如葡萄糖与进量苯肼作用,生成葡萄糖脎。
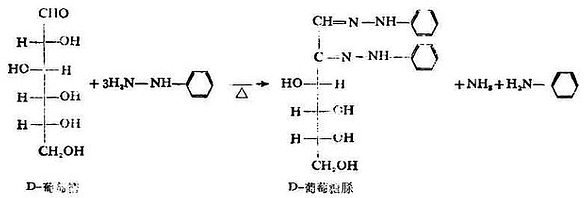
无论是醛糖还是酮糖都能生成糖脎,成脎反应可以看作是α-羟基醛或α-羟基酮的特有反应。
糖脎是难溶于水的黄色晶体。不同的脎具有特征的结晶形状和一定的熔点。常利用糖脎和这些性质来鉴别不同的糖。
成脎反应只在单糖分子的C-1和C-2上发生,不涉及其它碳原子,因此除了C-1和C-2以外碳原子构型相同的糖,都可以生成相同的糖脎。例如:D-葡萄糖和D-果糖都生成相同的脎。
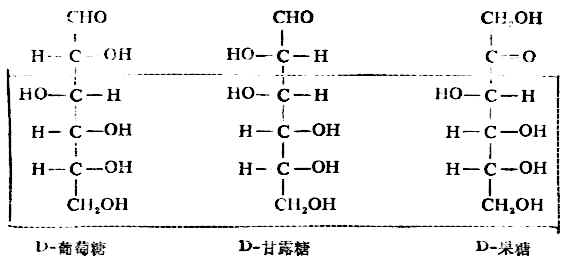
三、重要的单糖及其衍生物
自然界已发现的单糖主要是戊糖和己糖。常见的戊糖有D-(-)-核糖、D-(-)-2-脱氧核糖、D-(+)-木糖和L-(+)-阿拉伯糖。它们都是醛糖,以多糖或苷的形式存在于动植物中。常见的己糖有D-(+)-葡萄糖、D-(+)-甘露糖、D-(+)-半乳糖和D-(-)-果糖,后者为酮糖。己糖以游离或结合的形式存在于动植物中。
(一)D-(-)-核糖和D-(-)-2-脱氧核糖
核糖以糖苷的形式存在于酵母和细胞中,是核酸以及某些酶和维生素的组成成全分。核酸中除核糖外,还有2-脱氧核糖(简称为脱氧核糖)。
核糖和脱氧核糖的环为呋喃环,故称为呋呋喃糖。

β-D -(-)-呋喃核糖β-D-(-)-脱氧呋喃核糖
核酸中的核糖或脱氧核糖C-1上的β-苷键结合成核糖核苷或脱氧核糖核苷,统称为核苷。
核苷中的核糖或脱氧核糖,再以C-5或C-3上的羟基与磷酸以酯键结合即成为核苷酸。含核糖的核苷酸统称为核糖核苷酸,是RNA的基本组成单位;含脱氧核糖的核苷酸统称为脱氧核糖核苷酸,是DNA的基本组成单位。
(二)D-(+)-葡萄糖
D-(+)-葡萄糖在自然界中分布极广,尤以葡萄中含量较多,因此叫葡萄糖。葡萄糖也存在于人的血液中(389-555umol/l)叫做血糖。糖尿病患者的尿中含有葡萄糖,含糖量随病情的轻重而不同。葡萄糖是许多糖如蔗糖、麦芽糖、乳糖、淀粉、糖原、纤维素等的组成单元。
葡萄糖是无色晶体或白色结晶性粉末,熔点146℃,易溶于水,难溶于酒精,有甜味。天然的葡萄糖具有右旋性,故又称右旋糖。
在肝脏内,葡萄糖在酶作用下氧化成葡萄糖醛酸,即葡萄糖末端上的羟甲基被氧化生成羧基。
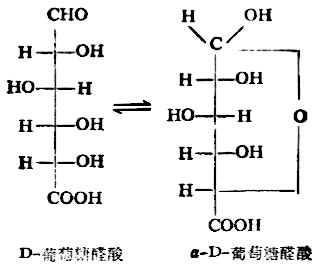
葡萄糖醛酸在肝中可与有毒物质如醇、酚等结合变成无毒化合物由尿排出体外,可达到解毒作用。
(三)D-(+)-半乳糖
半乳糖与葡萄糖结合成乳糖,存在于哺乳动物的乳汁中,。脑髓中有些结构复杂的脑苷脂中也含有半乳糖。
半乳糖是己醛糖,是葡萄糖的非对映体。两者不同之处仅在于C-4上的构型正好相反,故两者为C-4的差向异构体。半乳糖也有环状结构,C-1上也有α-和β-两种构型。
α-D-吡喃半乳糖β-D-吡喃半乳糖
半乳糖是无色晶体,熔点165-166℃。半乳糖有还原性,也有变旋现象,平衡时的比旋光度为+83.3°。
人体内的半乳糖是摄入食物中乳糖的水解产物。在酶的催化下半乳糖能转变为葡萄糖。
半乳糖的一些衍生物广泛分布于植物界。例如,半乳糖醛酸是植物粘液的主要成分;石花菜胶9也叫琼脂)的主要组成是半乳糖衍生物的高聚体。
(四)D-(-)-果糖
D-果糖以游离状态存在于水果和蜂蜜中,是蔗糖的一个组成单元,在动物的前列腺和精液中也含有相当量的果糖。
果糖为无色晶体,易用溶于水,熔点为105℃。D-果糖为左旋糖,也有变旋现象,平衡时的比旋光度为-92°。这种平衡体系是开链式和环式果糖的混合物。
β-D-(-)-吡喃果糖 β-D-(-)-呋喃果糖
果糖在游离状态下时,主要以吡喃环形式存在:在结合状态时则多以呋喃环形式存在。
![]() 果糖也可以形成磷酸酯,体内有果糖-6-磷酸酯,(用F-6-表示)和果糖-1,6-二磷酸F-1,6-二 )。
果糖也可以形成磷酸酯,体内有果糖-6-磷酸酯,(用F-6-表示)和果糖-1,6-二磷酸F-1,6-二 )。
![]() 果糖磷酸酯体内糖代谢的重 要中间产物,在糖代谢中有其重要的地位。F-1,6-二 在酶的催化下,可生成甘油醛-3-磷酸酯和二羟 基的丙酮磷酸酯。
果糖磷酸酯体内糖代谢的重 要中间产物,在糖代谢中有其重要的地位。F-1,6-二 在酶的催化下,可生成甘油醛-3-磷酸酯和二羟 基的丙酮磷酸酯。
体内通过此反应将己糖变为丙糖,这是糖代谢过程中的一个中间步骤。此反应类似于羟醛缩合反应的逆反应。
(五)氨基糖
自然界的氨基糖是己醛糖分子中C-2上的羟基被氨基取代的衍生物。

β-D-氨基葡萄糖β-D-氨基半乳糖
氨基糖常以结合状态存在于粘蛋白和糖蛋白中,但游离的氨基半乳糖对肝脏有毒性。
第二节 二糖
二糖是由两分子单糖脱水而成的化合物,也可以看成是苷,不过是苷元部分是另外一分子的单糖。常见的二糖有蔗糖、麦芽糖、纤维二糖和乳糖,它们的分子式都是C12H22O11。
二糖的物理性质类似于单糖。易溶于水,多数具有甜味。
一、二糖的结构和性质
二糖既然是苷,则形成苷键的两个羟基中,必有一个是半缩醛羟基,另一个可以是半缩醛羟基或醇羟基。这样,两上单糖分子以苷键结合成二糖时,就有两种情况:
一种是两个单糖分子都 以其半缩醛羟基脱水形成二糖,如蔗糖。这样的二糖,分子中不再含半缩醛羟基,不能开环再出现醛基,无变旋现象,也无还原性,称为非还原性二糖。
另一种是一个单糖分子以半缩醛羟基和另一个单糖的醇羟基之间脱水形成二糖。这样的二糖分子中还有一个半缩醛羟基未参与形成苷键,在溶液中可以开环,因此有变旋现象,有还原性,称为还原性二糖。重要的还原性二糖有麦糖、纤维二糖和乳糖。
单糖的环状结构有α-和β-两种构型,因此由α型的半缩醛羟基形成的苷键,称为α-苷键;由β型半缩醛羟基形成的苷键,称为β-苷键。麦芽糖和纤维二糖就是由两个葡萄糖分子通过不同的苷键组成的二糖。
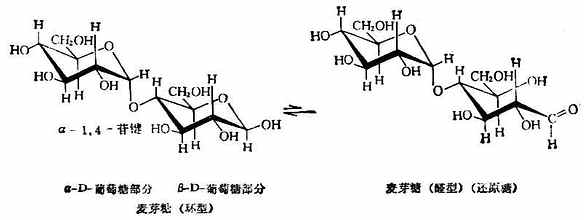
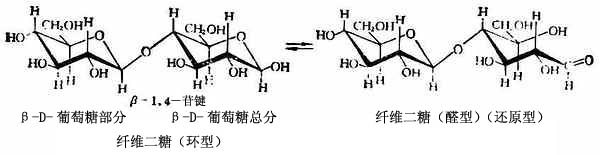
上二式中,麦芽糖分子中的苷键是α-1,4-苷键(α-1是指糖的部分在C-1上的α-型半缩醛羟基,4是指苷元C-4上的羟基),纤维二糖的苷键是β-1,4-苷键。α-苷键和β-苷键都可被酸水解,也可被某些有立体特异性的酶水解。人体内的麦芽糖只能水解α-苷键而不能水解β-苷键。苦杏仁苷酶则只能水解β苷键而不能水解α-苷键。
二、重要的二糖
(一)蔗糖
蔗糖广泛地分布在各种植物中,甘蔗中约含26%,甜菜中含20%,故又称甜菜糖,各种植物的果实中几乎都含有蔗糖。平时食用的就是蔗糖。我国是世界上用甘蔗制糖最早的国家。
蔗糖为无色晶体,熔点186℃,易溶于水,水溶液的比旋亮度为+66.7°.蔗糖水解后得到等分子的D-葡萄糖和D-果糖的混合物,其比旋亮度为-19.65°,与水解前的旋光方向相反,因而把蔗糖的水解过程称为转化,水解后的混合液称为转化糖。促使蔗糖水解的酶称为转化酶。
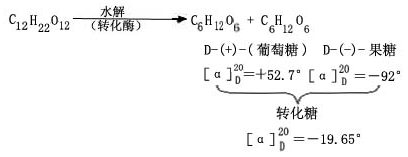
蔗糖是α-D-葡萄糖用C-1的半缩醛羟基与β-D-果糖C-2的半缩醛羟基脱水而组成的二糖,故蔗糖分子中的苷键既是α-1,2-苷键,又是β-2,1-苷键。
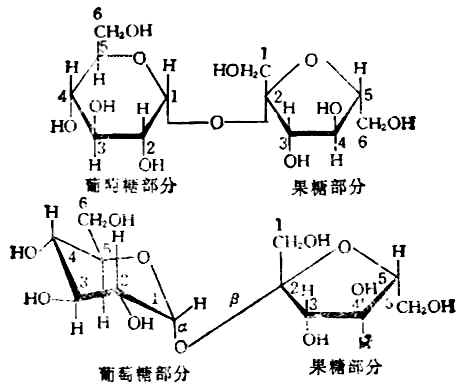
由于蔗糖分子中已无半缩醛羟基,故蔗糖无变旋现象,也无还原性,是非还原性二糖。
(二)麦芽糖
麦芽糖因存在于麦芽中而得此俗名。麦芽中的淀粉可将淀粉水解成麦芽糖。
在人体内,摄入食物中的淀粉被淀粉水解成麦芽糖,再经麦芽糖酶水解为D-葡萄糖。所以,麦芽糖是淀粉水解的中间产物。麦芽糖在酸作用下也能水解。
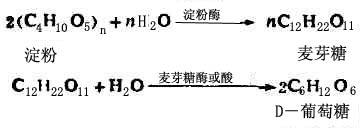
麦芽糖是由一分子α-D-葡萄糖用其半缩醛羟基与另一分子D-葡萄糖C-4上的醇羟基脱水,通过α-1,4-苷键组成的二糖。因此,麦芽糖有变旋现象,能还原费林试剂和吐伦试剂,属于还原性二糖。
麦芽糖是无色晶体,通常含一分子结晶水,熔点102℃,易溶于水,比旋光度为+136。
(三)乳糖
乳糖存在于哺乳动物的乳汁中,人乳中含5%-8%,牛乳中含4%-6%,有些水果中也含有乳糖。乳糖是含一分子结晶水的白色结晶性粉末,熔点202℃,易溶于水,比旋光度为+53.5°。
乳糖是β-D-葡萄糖用半缩醛羟基与α-D-葡萄糖的C-4羟基脱水,通过β-1,4-苷键形成的二糖。因此,乳糖有变旋现象,有还原性,是还原性二糖。
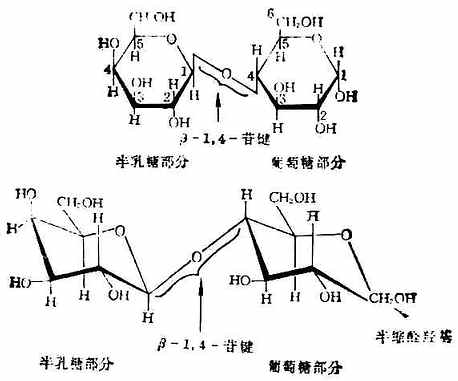
乳糖被人体小肠中乳糖酶9一种能水解β-半乳糖苷的酶)水解生成半乳糖和葡萄糖。
第三节 多糖
多糖是由很多分子单糖以苷键结合而成的高分子碳水化合物,可用通式(C6H10O5)n表示。组成多糖的单糖可以相同也可以不同。由相同的单糖组成的多糖称为均多糖,如淀粉、纤维素和糖原;以没的单糖组成的多糖称为杂多糖,如阿拉伯胶是由戊糖和半乳糖等组成。多糖不是一种纯粹的化学物质,而昌聚合程度不同的物质的混合物。
多糖在自然界分布极广,亦很重要。有的是构成动植物骨架结构的组成成分,如纤维素;有的是作为动植物储藏的养分,如糖原和淀粉;有的具有特殊的生物活性,像人体中的肝素有抗凝血作用,肺炎球菌细胞壁中的多糖有抗原作用。
多糖大部分为无定形粉末,没有甜味,无一定熔点,大多数不溶于水,个别能与水形成胶体溶液。多糖没有还原性和变旋现象,尽管多糖末端含有半缩醛羟基,但因相对分子质量很大,其还原性和变旋现象极不显著。多糖也是糖苷,所以可以水解,在水解过程中,往往产生一系列的中间产物,最终完全水解得到单糖。
一、多糖的结构
多糖的结构单位是单糖,多糖相对分子质量从几万到几千万。结构单位之间以苷键相连接,常见的苷键有α-1,4-、β-1,4-和α-1,6-苷键。结构单位可以连成直链,也可以形成支链,直链一般以α-1,4-苷键(如淀粉)和β-1,4-苷键9如纤维素)连成;支链中链与链的连接点常是α-1,6-苷键。
二、重要的多糖
(一)淀粉
淀粉广泛地存在于许多植物的种子、块茎和根中,如大米中约含70%-80%,小麦中约含60%-65%,马铃薯中约含20%。
淀粉是白色无定形粉末,没有还原性,不溶于一般有机溶剂。淀粉可分为糖淀粉(又称直链淀粉)胶淀粉(又称支链淀粉)。糖淀粉和胶淀粉在结构和性质上有一定区别,它们在淀粉中所占比例随植物品种而不同,一般糖淀粉的含量为20%-30%,胶淀粉含量为70%-80%。两者经酸水解后最终产物都是D-葡萄糖。
纯的糖淀粉不易溶于冷水,在热水中不成糊状。糖淀粉的相对分子质量约为150000-600000,它是由许多D-葡萄糖单位通过α-1,4-苷键连接而成的链状化合物。
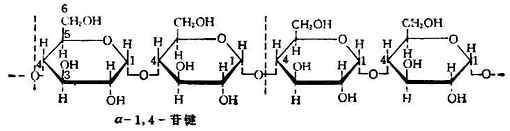
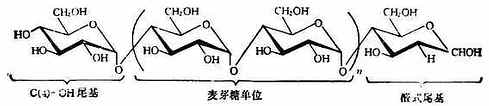
糖淀粉的结构
由于糖淀粉分子链很长,因此不可能以线型分子存在,而是在分子内氢键的作用下,卷曲盘旋成螺旋状,每个螺圈约含六个D-葡萄糖单位。此外,在主链上还有少数短分支。
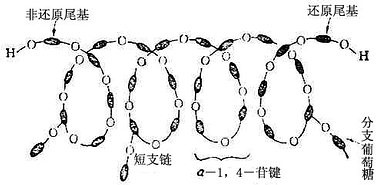
糖淀粉分子的基间状态
糖淀粉遇碘呈蓝色,这并不是碘与淀粉之间形成了化学键,而是由于糖淀粉螺旋状结构的中空穴部分恰好能容纳碘分子,二者之间借助于范德华力形成一种蓝色的包合物,如图21-1所示。此显色反应常用来检验淀粉或碘的存在。
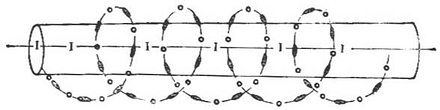
图21-1 碘-淀粉包合物结构示意图
胶淀粉与糖淀粉相比,具有高度分支,且所含葡萄糖单位要多得多,胶淀粉相对分子质量可高达1000000-6000000。纯的胶淀粉不溶于冷水,在热水中膨胀而成糊状。它的主链同样是由D-葡萄糖以α-1,4-苷键相连,此外每隔20-25个葡萄糖单位,还有一个以α-1,6-苷键相连的支链。
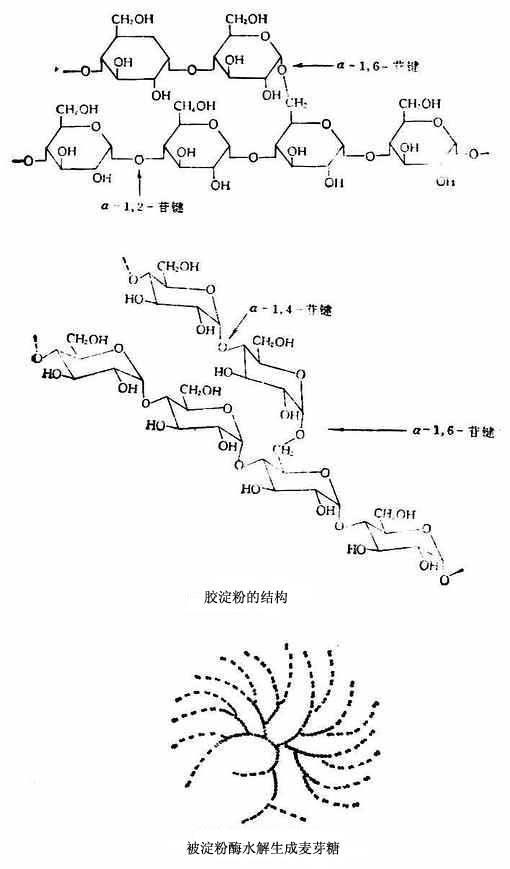
图21-2 胶淀粉的分支状结构示意图
淀粉在水解过程中可生成各种糊精和麦芽糖等一系列中间产物,最终产物是D-葡萄糖。糊精是相对分子质量较小的多糖,包括紫糊精、红糊精和无色糊精等。淀粉和糊精与碘溶液作用可产物不同颜色,此种颜色煮沸时消失,放冷又重现。淀粉水解可用酶或酸来催化,水解进程可用碘液与其作用的颜色变化来判断。
(C6H10O5)n→(C6H10O5)n-x→C12H22O11→C6H12O6
淀粉→紫糊精→红糊精→无色糊精→麦芽糖→葡萄糖
(蓝色)(紫糊精)(红色)(无色)(无色)(无色)
(二)糖原
糖原是动物体内贮存的一种多糖,双称为动物淀粉,主要存在于肝脏和肌肉中,因此有肝糖原和肌糖原之分。正常情况下,肝脏中糖原的含量达10%-20%,肌肉中的含量达4%。人体约含糖原400g,糖原在体内的贮存有重要意义,它是机体活动所需能量的重要来源。当血液中葡萄糖含量增高时,多余的葡萄糖就转变成糖原贮存于肝脏中,当血液中葡萄糖含量降低时,肝糖原就分解为葡萄糖进入血液中,以保持血液中葡萄糖的一定含量。
糖原是葡萄糖多分子缩合物,在结构上与胶原淀粉相似,其结构单位D-葡萄糖之间以α-1,4-苷键结合,链和链之间的连接点以α-1,6-苷键结合。在糖原中每隔8-10个葡萄糖单位就出现α-1,6-苷键 。糖原的分子比胶淀粉更大,分支更多,结构更复杂(图21-3),相对分子质量可高达1×108。

图21-3 糖原的分去状结构示意图
糖原是无定性粉末,溶于热水,溶解后呈胶体溶液。糖原溶液遇碘呈紫红色。糖原水解的最终产物是D-葡萄糖。
(三)纤维素
纤维素是植物细胞壁的主要成分,是构成植物支撑组织的基础。棉花几乎全部是由纤维素所组成(占98%),亚麻中约含80%,木材中纤维平均含量约为50%,此外,发现某些动物体内也有动物纤维素。
纤维素的结构单位也是D-葡萄糖,和糖淀粉相似也是无分支的链状分子,但结构单位之间以β-1,4-苷键结合而成长链。经X射线测定,纤维素分子的链和链之间借助于分子间的氢键拧成像绳索状的结构(图21-4),这咱绳索状的结构具有一定的机械强度和韧性,故在植物体内起着支撑的作用。
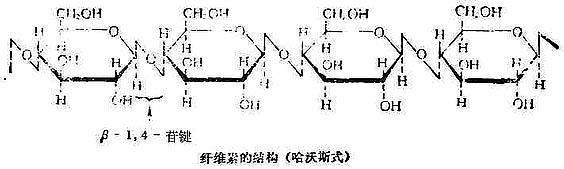
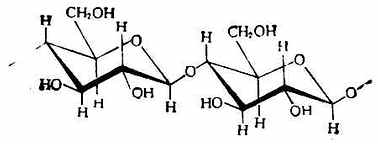
纤维素的结构(构象式)
图21-4 绳索状纤维素链示意图
纤维素是白色物质,不溶于水,无还原性。纤维素比淀粉难水解,一般需要在浓酸中或用稀酸在加压下进行。在水解过程中可以得到纤维四糖、纤维三糖、纤维二糖、最终产物是D-葡萄糖。人的消化道中水解淀粉酶只能水解α-1,4-苷键,而不能水解β-1,4-苷键,所以纤维素不能作为人的营养物质,但食物中的纤维素能促使肠蠕动,具有通便作用。
纤维素与氯乙酸钠CH2CLCOONa反应生成羧甲基纤维素钠(CMC)。它是白色吸湿性粉末,可溶于冷、热水中,是性能良好的混悬剂、乳化剂、粘合剂和延效剂。
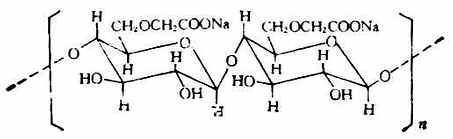
羧甲基纤维素钠结构
(四)粘多糖
粘多糖是由氨基己糖与糖醛酸两种己糖衍生物所组成的二糖单元聚合而成的直链高分子化合物。因其中很多具有粘性,所以称为粘多糖(又称氨基多糖0。粘多糖是结缔组织的主要成分,组织间质及腺体分泌的粘液中均含有。生物体内粘多糖往往与蛋白质结合成粘蛋白,粘蛋白分子常同时连接多外粘多糖,因而粘多糖的比例常超过蛋白质部分,因此粘蛋白又称为蛋白多糖。
1.透明质酸
透明质酸与蛋白质结合,存在于眼球玻璃体、角膜及脐带中,结缔组织中也含有。它与水形成粘稠凝胶,有润滑和保护细胞的作用。
透明质酸是由β-D-葡萄糖醛酸和N-乙酰基-D-氨基葡萄糖通过β-1,3-苷键连接成二糖衍生物,并以此为重复单元再通过β-1,4-苷键互相连接成透明质酸。其结构如下:
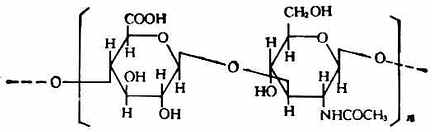
β-D-葡萄糖醛醛酸 N-乙酰基-D-氨基葡萄糖
透明质酸的水溶液具有高度粘性,它可被透明质酸酶水解而降低其粘性。在某些毒蛇和细菌中含有这种透明质酸酶,可使组织中的透明质酸水解,使毒液或病原体容易侵入。在精液中也含有多量透明质酸酶,它可使卵子外表的透明质酸水解,使精子易与卵子结合而受精。
2.硫酸软骨腩
硫酸软骨质存在于大多数结缔组织中,是软骨、腱和骨的主要结构成分,软骨中的软骨粘蛋白是硫酸软骨质与蛋白质结合而成的。已知的硫酸软骨质有A,B,C三种。硫酸软骨质A的结构与透明质酸相似,只是在重复结构单元中的氨基糖为N-乙酰基半乳糖,并在其C-4或C-6上的羟基与硫酸成酯。其结构如下:
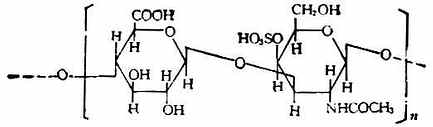
β-D-艾杜糖醛酸 N-乙酰基-D-氨基半乳糖-6-硫酸酯
硫酸软骨质A
上述结构中,如醛酸为D-艾杜糖醛酸即为硫酸软骨质B;若4-硫酸酯变为6-硫酸酯即为硫酸软骨质C。

β-D-艾杜糖醛酸 N-乙酰基-D-氨基半乳糖-6-硫酸酯
近年来在临床上用硫酸软骨质治疗肾炎、急慢性肝炎、偏头痛、动脉硬化及冠心病等。
3.肝素
肝素是一种比较简单的粘多糖,相对分子质量为3000-35000。肝素存在于动物的肝、肺、血管壁、肌肉和肠粘膜等部们,因最初在肝中发现,所以叫做肝素。肝素是凝血酶的对抗物质,能使凝血酶失去作用,因而血液在体内的不致凝固。临床上应用肝素的抗凝血作用,以防止某些手术后可能发生的血栓形成及脏器的粘连。
肝素的结构较复杂,一般认为它是由α-L-艾杜糖醛酸-2-硫酸酯、N-磺基-α-D-氨基葡萄6-硫酸酯、β-D-葡萄醛酸和N-磺基-α-D-氨基葡萄糖-6-硫酸酯以苷键结合成“四糖”作为结构单元,再由“四糖”聚合成多糖。
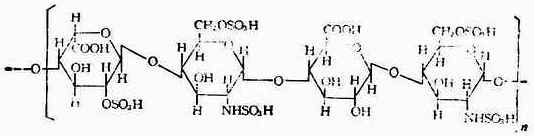
α-L-艾杜糖 N-磺基-α-D-氨基 β-D-葡萄糖 N-磺基-α-D-氨基
醛酸-2-硫酸酯 葡萄糖-6-硫酸酯 醛酸 葡萄糖-6-硫酸酯
肝 素
(五)右旋糖酐
右旋糖酐是一种合成的葡萄糖物,为一重要的血容量扩充剂,用于大量失血后补充血液容量,提高血浆胶体渗透压,有改善微循环等作用。临床上应用的右旋糖酐相对分子质量约在75000左右,大约含有400~500个葡萄糖单位,它们主要通过α-1,6-苷键相连接,杂有少量的α-1,3-苷键和α-1,4-苷键相连接的分支。
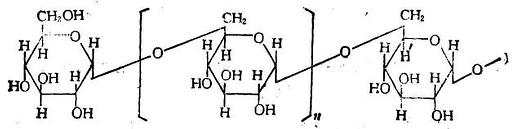
临床上一般用其6%的生理盐水溶液,因为它和血浆等渗,粘度也和血浆相同。
近年来,发现有些多糖,特别是多聚葡萄糖具有显著的抗癌活性,因此引起各国家者的广泛研究。这类多糖主要在D-葡萄糖通过β-1,3-苷键相互缩合而成,对某些实验动物肿瘤有明显的抵制作用,而且毒性很低。例如,从香菇中分离出的香菇多糖具有β-1,3-葡萄糖苷键,是一种直链多糖,呈显著的抗癌活性。由茯苓中分离的茯苓多糖具有β-1,3-葡萄糖苷键与少量β-1,6-葡萄糖苷键,也有显著的抗癌活性。
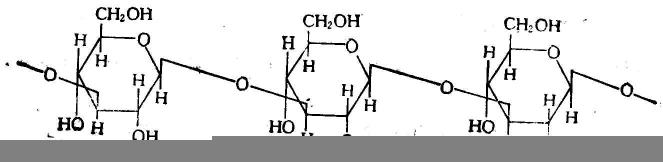
香菇多糖
