固定酶反应的其它条件,在不同pH处测定酶反应速度,可得各种类型的酶活性与pH关系见图17-3A。
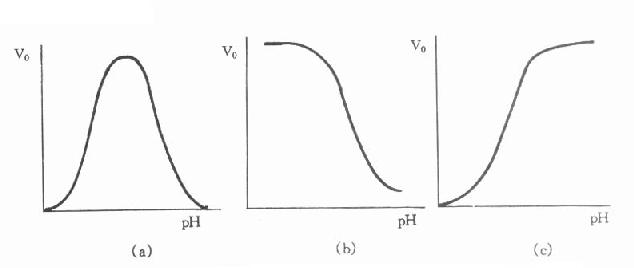
图17-3A 酶活性与pH的函数关系曲线可能具有的几种形状
最常见的是(a)的对称钟形曲线,少数的如(b)(c)在一侧即偏酸或偏碱处活性最高。生化学家将酶活性最高处的pH称为最适pH。一般来说,血清中大多数酶最适pH接近中性(pH6.5-7.5)。有些酶在最适pH处活性变化尖锐明显,也有些平坦宽广。测定酶活性浓度时一定要选择在最适pH处,不仅因为此处酶反应速度最大,测定灵敏度最高,还因为此处酶活性变化的斜率最小,如反应体系中出现pH变化时,对测定结果影响最小。
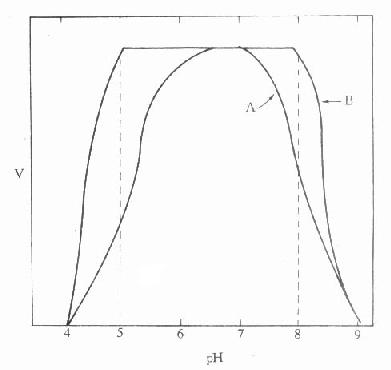
图17-3B pH对酶活性及稳定性的作用
曲线A:V对pH作图曲线B:酶先在pH5及pH8预孵育后,在pH6.8测活性
氢离子可以通过多种途径影响酶催化反应。如在脱氢酶反应中往往需要氢离子参加,也可能产生氢离子,从理论上可以将氢离子看成是该反应的底物和产物之一。此外,当pH变化时,可影响到底物、酶、酶-底物复合物的解离状态和构型,甚至还可能影响到各种辅因子,从而影响酶活性。
PH对酶还有一个重要的作用,就是影响酶的稳定性。图17-3B介绍一个有关实验。
图中曲线A是最适pH实验的结果,出现典型的钟形曲线,其最适pH为6.8,高于或低于6.8时,酶反应速度下降,下降原因可能与上述诸因素有关,但也可能由于酶稳定性下降失活所致,或者是二类原因之总和。通过曲线B的实验,可将上述二类原因分清。此时先将酶与不同pH底物缓冲液温育一段时间,此时间一般与测定时间相当,然后再将pH调回最适pH处测其活性。从曲线B可以说在pH5-6.8以及pH6.8-8.0之间酶活性的下降与酶灭活关系不大,酶在最适pH处储存常数稳定。但有些酶贮存在最适pH时,并不一定比在其它pH处更稳定。
最适pH并非是酶的特征性常数,易受多种因素影响而改变,如缓冲液的种类、底物浓度、温度等,在研究pH对酶稳定性影响还应注意到酶浓度高低,在低浓度时,酶易解离为单体,常比多聚体更易灭活。还应注意试剂中各种防腐剂和其它添加剂的影响。
最后必须强调的是本节讨论的pH并不是指底物缓冲液的pH,而是底物和标本混合后的pH对反应速度的影响,由于实验室所测的标本很少是纯酶样品,多为体液或组织粗提液。它们也是有一定pH值和缓冲能力的缓冲液,和底物缓冲液混后后,不一定维持住原来pH,特别是当二溶液的pH相差甚远时,变化更大。例如碱性磷酸酶最适pH为10.2,虽然底物pH也是10.2,但血清标本pH为中性,混合液的pH必然低于10.2,降低程度取决于血清的pH和缓冲能力。从而影响酶测定结果,临床观察证实:当血清标本放置过夜后用金氏法再测碱性磷酸酶时,结果常升高。有人认为这与血清放置过长,由于CO2逸出引起血清pH偏碱有关。
在下列情况极易引起混合液pH偏离底物缓冲液的pH:一是标本用量太大,如以前有些方法,为节省底物,底物缓冲液用量和血清用量相等,此时混合液pH可能在此二液pH之间,有可能引起较大测定误差。所以在文件中规定“标本在总体积中的比例应在10%以下”。就是要尽量减少标本中各种物质对测定结果的影响。二是底物缓冲液缓冲能力太低。如金氏法测碱性磷酸酶时使用的碳酸盐缓冲液的浓度为0.01mol/L,浓度这样低的缓冲液,必定要受标本pH的影响。
过去长期以来,认为缓冲液作用就是维持酶反应的最适pH,忽视了缓冲物质对酶反应的其它作用和影响,Howell等研究了酶活性在三种不同缓冲液的变化情况见图17-4。
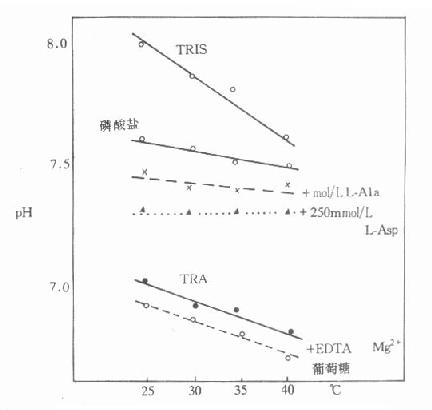
图17-4 各种缓冲液的温度及pH的关系
TRIS:三羟甲基氨基甲烷0.1mol/L
TRA:三乙醇胺0.1mol/L
三种不同缓冲液不仅最适pH不一样,最大反应速度也有差异,从测定酶活性浓度角度,应该选用枸橼酸缓冲液,类似现象在大多数酶都能观察到,仅是程度不同,其中以碱性磷酸酶活性受到缓冲液种类影响最为显著,在二乙醇胺缓冲液所测酶活性约比在碳酸盐缓冲液所测的高2倍。
由于缓冲液含有大量离子,或影响酶蛋白的构型,或影响底物的解离程度等等,从而影响酶活性。Allert曾拟定了一种作用模式,并进行数学计算,得出相应方程式来说明反应体系中电解质会影响最大反应速度V,且不同浓度电解质的影响有差异。因此在方法设计时,选完缓冲物质后,还必须了解不同浓度缓冲液对酶活性的影响。一般而言,随缓冲液浓度增加,电解质干扰酶和底物结合,酶活性将逐步下降,所以选择缓冲液浓度时,常需在浓度较高以保持足够缓冲能力和浓度较低以免抑制酶活性两个相矛盾作用之间取得平衡。
在目前酶测定常用的一大类所谓生物缓冲物质,如图中的Tris、三乙醇胺受温度影响较大。因此在我国学会文件中指出“配制缓冲液时不仅要指出其pH值,还应说明配制温度,以避免因温度不同而引起的误差。”在此图中还可看到,即使是同一种缓冲液,随其它物质存在,也有可能改变温度的影响。因此在实际配制缓冲液时,应首先将配制溶液温度调节到规定温度,然后在pH计监测下加入相应的酸或碱将溶液pH调到要求范围。不控制温度,不用pH计盲目按一些书提供的量配制缓冲液是不可取的。
