CD4和CD8分子分别与MHCⅡ类和Ⅰ类抗原结合,不仅可增强T淋巴细胞与APC或靶细胞结合的程度,而且与刺激信号的传递有关。CD4阳性细胞是MHCⅡ类抗原限制的细胞群,CD8阳性细胞是MHCⅠ类抗原限制的细胞群。有关CD4和CD8抗原在胸腺细胞分化过程中的变化以及CD4、CD8T细胞亚群见第七章“淋巴细胞群及其亚群”。
1.CD4分子的结构 为细胞膜表面单链糖蛋白,人CD4分子由458个氨基酸残基组成,包括信号肽23氨基酸残基,胞膜外区374个氨基酸残基,含2个糖基化点,穿膜区21氨基酸残基,胞浆内区含有40氨基酸残基。胞膜外区具有4个IgV样结构域,属免疫球蛋白超家族成员。
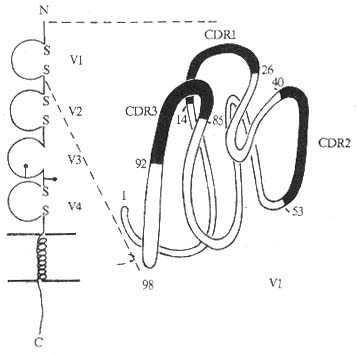
图1-5 CD4分子结构模式图
第一个V样区与Igκ链的V区有很高同源性,有3个互补决定区(complementarity-determining region, CDR)。其余3个V样区功能区与Poly IgR的同源性最接近,其中第2和4个V样区中两个半胱氨酸的距离分别为28和42个氨基酸残基,第3个V样区无二硫键。CD4跨膜区与MHCⅡ类分子β链的跨膜区高度同源。编码人CD4基因位于第2号染色体,小鼠第6号染色体,小鼠CD4分子的分子量为55kDa,由457个氨基酸残基组成,信号肽有22个氨基酸残基,N端功能区110个,胞膜外还有一个长序列(long sequence)的区域,含262氨基酸残基,有4个糖基化点,穿膜区25氨基酸残基,胞浆内区含38个氨基酸残基。人和小鼠CD4分子约有55%序列相同,尤以胞浆内区为显。在胞浆部位有3个丝氨酸残基,可能作为PKC磷酸化的底物。CD4胞浆部分功能区高度的保守性表明这一区域的功能是重要的。
2.CD4分子的分布 分布于部分T淋巴细胞和胸腺细胞表面,也发现于某些B淋巴细胞、EBV转化和B细胞、单核吞噬细胞和脑细胞。在人类,OKT4和Leu3McAb可检测CD4抗原。小鼠L3T4是人OKT4的类同物。
3.CD4分子的功能 在成熟的胸腺细胞、外周血和周围淋巴器官中,CD4阳性细胞一般为辅助性T淋巴细胞诱导细胞/抑制性T淋巴细胞诱导细胞(helper inducer/suppressor inducer)。
(1)作为细胞与细胞之间的粘附分子:CD4第1、2功能区与MHCⅡ类分子的非多态部分结合以稳定MHCⅡ类分子限制的T细胞与带有MHCⅡ类分子与抗原复合物的APC细胞相互作用。抗CD4McAb可封闭T细胞的辅助活性。
(2)转导信号:CD4分子胞浆区与蛋白酪氨酸激酶p56lck相联,对T细胞信号的转导起重要作用(详见第八章)。
CD4分子胞膜外第1个结构区域是HIV外壳蛋白gp120的识别部位,其中CDR2与gp120结合的亲合力最高,CDR3可能与HIV感染靶细胞膜融合有关。可溶性 gp120结合到CD4的反应可被下列试剂所阻断:(1)针对CD4V1区中CDR2、CDR3的McAb;(2)CDR2、CDR3肽段;(3)可溶性CD4 V1肽段;(4)抗gp120抗体。HIV感染机体可引起选择性CD4+细胞的数量减少和功能降低,主要通过以下不同的机理:(1)HIVgp120与T细胞表面CD4分子结合后通过病毒芽生破坏细胞膜,在感染细胞浆内产生大量非整合的病毒RNA直接损伤细胞膜、干扰细胞代谢,影响CD4分子在细胞膜上的表达以及形成短命的合胞体;(2)阻断CD4+T细胞与Mψ细胞表面MHCⅡ类抗原的结合,影响Th细胞对抗原的识别过程;(3)产生抗体损伤CD4细胞,机体产生抗gp120或其他HIV成份的抗体,通过激活补体或ADCC效应损伤CD4阳性细胞;(4)特异性CTL也可通过识别CD4细胞表面的gp120分子而杀伤CD4阳性细胞。最近发现,CD26可能是HIV的另一类受体。
应用基因工程生产的重组可溶性CD4(rsCD4)治疗ARC(AIDsrelated complexes)、艾滋病正在进行Ⅱ期临床试验;抗CD4McAb(Leu3a)也已开始治疗HIV感染的I期临床试验。此外,应用CD4-IgG、CD4-PE(绿脓杆菌外毒素)、CD4-RA(蓖麻毒毒A)等杂交分子杀伤HIV感染的T细胞,作为抗爱滋病的新药也已进入临床验证。1991年美国风湿病学年会上报道了用抗CD4McAb治疗类风湿性关节炎(RA),经治疗后临床症状明显改善,PBMC中CD4阳性细胞的比例和CD4抗原密度明显下降,血清可溶性CD4(sCD4)水平明显升高,血沉、CRP、RF、和总免疫球蛋白水平明显降低。抗CD4嵌合抗体(Centocor公司)治疗类风湿性关节炎、多发性硬化症也已进入Ⅱ期临床验证。抗CD4McAb(Ortho Biotech公司)预防器官移植排斥反应已开始临床验证。
