有报道,血浆HDL含量过高导致高HDL血症,也属于病理状态,HDL具有抗动脉粥样硬化作用,是人们公认的,然而并非血浆HDL含量越高越好,血浆HDL-胆固醇(HDL-C)含量超过2.59mmol/dl定义为高HDL血症,现已查明,高HDL血症是因为有CETP和HTGL等活性异常所致,高HDL血症又分为原发性和继发性,原发性高HDL血症的病因有以下几种①CETP缺损;②HTGL活性降低;③以及其他不明原因。继发性高HDL血症病因有:运动失调;饮酒过量;④原发性胆汁性肝硬化;⑤治疗高脂血症的药物引起;⑥其他原因。总之,CETP及HTGL活性降低是引起高HDL血症主要的原因。CETP缺陷,HDL上的CE蓄积,使HDL增多;若HTGL活性降低,HTGL与HDL被肝细胞摄取并使HDL2→HDL3转换过程有关。HTGL活性降低使HDL被肝细胞摄取量减少而停留在血液中并使其浓度增加,出现高HDL血症。血清中总胆固醇轻度或中度升高,HDL-C高达正常人3~5倍的高值,血清ApoAⅠ、CⅢ,E明显增加,ApoB呈低值。CE量增加,因为CETP活性低,从HDL转运到含ApoB的脂蛋白的CE量减少,即运输障碍所致。高HDL血症多见于CETP缺乏者,易出现多分散LDL,而HDL颗粒变大,有实验表明,CETP活性低的动物作胆固醇负荷实验很容易形成动脉粥样硬化,对人而言,高HDL血症与动脉粥样硬化的关系有待进一步研究。
HDL按超速离心法可分为HDL2和HDL3,Blanche及Albers等报道,用聚丙烯酰胺梯度凝胶电泳可将HDL分为HDL1,2a,2b,3a,3b,3c六种亚组份颗粒,如图10-4所示。健康人HDL3c Stokes直径7.8nm;HDL3b为8.4mn;HDL3a为9.0mn,HDL2a为9.6nm和HDL2b为10.8nm。并报道冠心病患者大型颗粒HDL2b减少,小颗粒HDL3b增加,认为HDL2b的上升有抗动脉粥样硬化的作用,HDL3b颗粒的增加与动脉粥样硬化形成有关,进而推测高HDL3b血症中若是HDL3b组份增加者,则可以引起脂质代谢障碍。
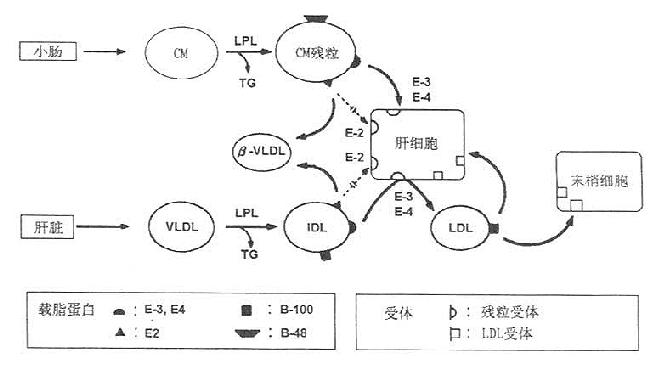
图10-3 富含TG脂蛋白的代谢与Ⅲ型高脂血症发病机制
近期有作者提出HDL-C与长寿的问题。Jeffery等于1996年报告的一例59岁的妇女,血胆固醇为9.1mmol/L,HDL-C为5.7mmol/L、LDL-C为2.8mmol/L,TC与HDL-C的比值为1.6(心血管病危险因素比值为5.0),ApoAⅠ含量超过正常对照者。该患者经其他有关的物理检查,未发现有任何动脉粥样硬化的征兆。将患者血浆ApoAⅠ提纯作体内的代谢研究提示,患者血浆ApoAⅠ的清除率是正常的,并诊断为高α-脂蛋白(HDL)血症。经家族史调查,该妇女父母亲及外祖父均为长寿者,尚未发现与脂代谢有关的疾患。
该例提示了长寿的遗传倾向问题。导致动脉粥样硬化形式的因素是多方面的,环境因素与遗传因素对其病理生理的过程具有重要影响。众所周知,环境因素与吸烟、饱和脂肪酸和食物胆固醇消耗以及营养过剩,均与症状性心血管病的发生有关。同样,基因变异所致的LDL-C极度增高HDL-C总量低下均可加速动脉粥样硬化的形成。1988年leaf报道百岁老人的共同特点是每日体力劳动和低饱和脂肪饮食。Schaefer等于1989年报导,80岁以上的长者均无血浆HDL-C含减少,并认为HDL-C与长寿有关。Gofman报导,提高HDL-C基因可以防止动脉粥样硬化的发生,为此提出,通过基因能否预防动脉粥样硬化的问题。流行病学研究表明HDL-C浓度愈高,发生心血管病的危险性愈低。根据Framingham的1988年的报道,HDL-C含量为1.5mmol/L或更高者,即使同时有HDL-C的增高,对心血管病的发生LDL-C仍属于阴性危险因素。此外,降低LDL-C浓度的干预试验提示,HDL-C可以提供相对的保护作用,LDL-C浓度降1%,可使心血管危险性降低2%;然而HDL-C浓度增加1%,则使心血管病发病率至少降低2%~3%。该研究表明,HDL-C对心血管疾病确实有预防作用。
临床已注意到HDL-C的预防作用。HDL的生理功能是通过HDL中各组份介导的。HDL的主要载脂蛋白是ApoAⅠ、AⅡ,ApoAⅠ在肝和肠内合成,ApoAⅡ仅在肝内合成。HDL中各不同密度的颗粒,其载脂蛋白组成是有差异的。含有AⅠ颗粒而不含AⅡ颗粒,称为脂蛋白AⅠ唯一颗粒,代号为LpAⅠ-Only particles,该颗粒可以防止心血管疾病。其他各种蛋白质,也可影响HDL颗粒的成份和代谢,LCAT和HL是HDL中脂质代谢调节中心,CTP在该颗粒核心内,以TG从易致粥样硬化的含有ApoB的脂蛋白中交换胆固醇酯。血小板活化因子酰转移酶能使HDL和LDL中的磷脂生成具有生物活性的溶血磷脂酰胆碱及小板活化因子(PAF)。还有系列活性代谢酶,可以保护HDL的脂质受氧化性损伤,从而增强HDL对心脏的保护功能。
目前所知,HDL-C浓度升高有三种遗传原因。其一是遗传性ApoAⅠ基因过度表达;其二是家族性高α脂蛋白血症,这两种遗传因素导致HDL-C浓度升高,ApoAⅠ含量增加,使心血管发病率降低;其三是CTP基因突变,使胆固醇酯在血浆脂蛋白中与甘油三酯交换能力降低,进而导致HDL-C浓度增高。有报导,CTP缺乏的纯合子个体,HDL-C浓度可超过3.9mmol/L,与此相反,在ApoAⅠ产生过多的患者,HDL浓度过高则是HDL从血液循环中清除过缓所致。然而HDL浓度增高可防止早发性心血管病,还有待证实。
HDL可以通过不同的机理发挥作用。它能影响血管舒缩力或诱导内皮细胞增殖,有助于动脉壁对抗内皮下组织直接暴露于血循环所致的损伤;HDL又能缓冲LDL的氧化;HDL能清除自由基保护LDL免遭氧化的损害。HDL可清除细胞内过多的胆固醇,以减少粥样硬化斑的形成。其中的ApoAⅠ基因过表达可使HDL-C浓度增加并减弱粥样化的发展。ApoAⅠ基因可能是一种杂交基因(Methuselah genes),该基因可以改变动脉粥样硬化的慢性病的多种遗传因子的性状。ApoAⅠ基因过度表达能降低心血管疾病发病率的事实,指示可以通过基因传递技术的使用,使人们可以采用各种杂交基因治疗甚至预防心脑血管性疾病。
Fredrickson于1963年将高脂蛋白血症分为六型,在临床诊治疾病过程中有一定的意义,然而从临床实验室诊断方法学考虑,作脂蛋白检测有一定难度,电泳分离法欠准确,按超速离心法,操作时间过长,难以快速定量。另外,高脂蛋白血症多数与遗传有关,目前可采用载脂蛋白基因分型。载脂蛋白的基因分型是目前研究脂质代谢及探讨动脉粥样硬化发病机制的热门话题。
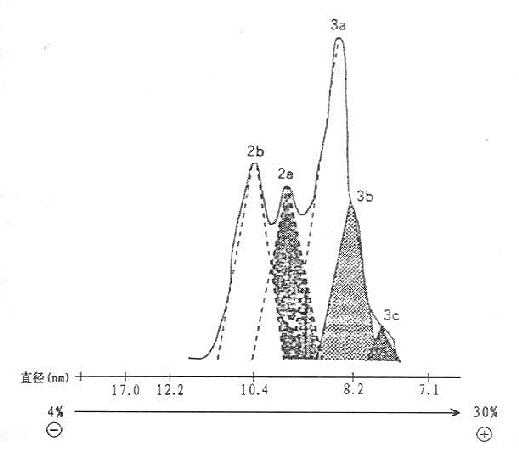
图10-4 健康人HDL亚组份颗粒的聚丙烯酰胺梯度(4%~30%PAG)电泳图
(源自:Blanche,P.J.et al B.B.A,1981)
