细菌、病毒、螺旋体、高热、抗原抗体复合物、休克时持续的缺血、缺氧和酸中毒、败血症时的细菌内毒素等,在一定条件下皆可使血管内皮细胞发生损伤,使其下面的胶原暴露。胶原、内毒素等均为表面带负电荷的物质,当无活性的凝血因子Ⅻ与这些物质表面发生接触后,其精氨酸残基上的胍基在负电荷影响下分子构型发生改变,它的活性部分——丝氨酸残基暴露,所以因子Ⅻ被激活(此种激活方式称接触激活或固相激活)。另外,也可能在激肽释放酶、纤溶酶或胰蛋白酶等可溶性蛋白水解酶的作用下,因子Ⅻ或Ⅻa通过酶性水解(酶性激活或液相激活)而生成Ⅻf。胶原等激活因子Ⅻ的过程开始时进行得较为缓慢,但因Ⅻ的碎片(Ⅻf),即激肽释放酶原激活物(predallidreinactivator, PKA)可把血浆激肽释放酶原(prekallikrein)激活成激肽释放酶(kallikrein),后者又能反过来使因子Ⅻ进一步活化,从而使内源性凝血系统的反应加速(图9-1)。Ⅻa和Ⅻf还可相继激活纤溶、激肽和补体系统,从而进一步促进DIC发展。
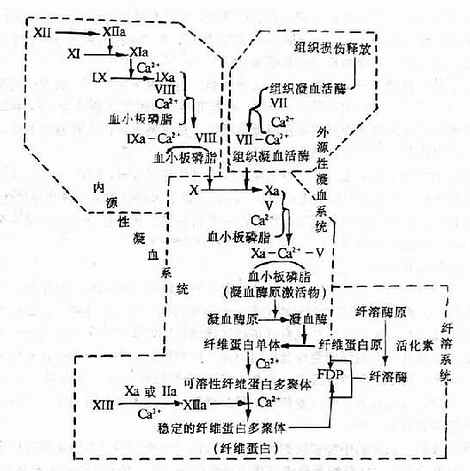
图9-1 血液凝固过程及纤溶系统
以内毒素血症为例,此时,除内毒素可直接激活因子Ⅻ外,内毒素还可引起血管内皮细胞损伤,基底膜暴露后,胶原、胶原与某些糖蛋白的复合物或另一些结缔组织成分也可激活因子Ⅻ。此外,还有某些酸糖脂(acidic glycolipids),硫酸脂(sulfatides),氨基葡聚糖(glycosaminoglycans)或另外一些特殊的因子Ⅻ激活物也可自损伤的内皮细胞释放,因此内源性凝血系统启动。在家兔内毒素引起的DIC中常可有内皮细胞脱落,在循环血中有内皮细胞出现。抗原抗体复合物粘附在肾小球等微血管壁上时,可引起血管内皮细胞损伤。血管炎时也可继发血管内皮细胞损伤,进一步触发DIC。
此外,在内皮细胞受损时,血小板与内皮下结缔组织中的胶原接触后可以产生胶原诱导的促凝活性,此时,因子Ⅺ可不通过Ⅻa而直接被激活,从而推动凝血连锁反应,引起DIC。
表9-1不同的人体组织中凝血因子Ⅲ的含量
| 组织 | 含量 (μ/mg) |
| 肝 | 10 |
| 肌肉 | 20 |
| 脑 | 50 |
| 肺 | 50 |
| 胎盘 | 2,000 |
| 蜕膜 | 2,000 |
